Optimization of Flavonoid Extraction from Ganoderma lucidum by Response Surface Methodology and Antioxidant Activities of Extracts
-
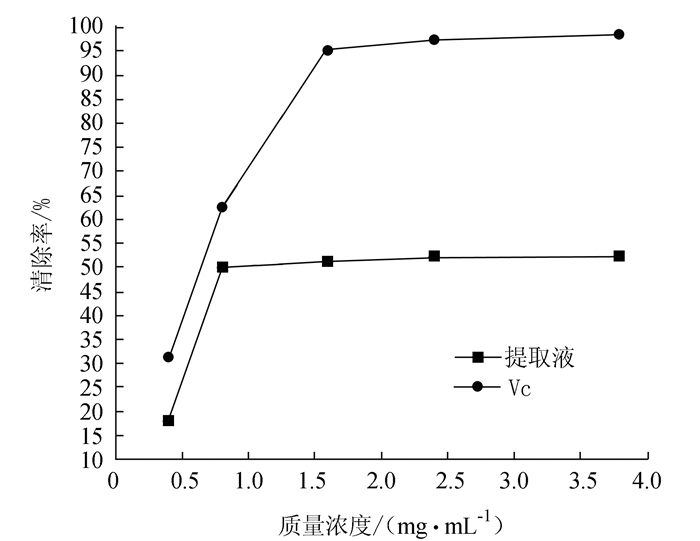
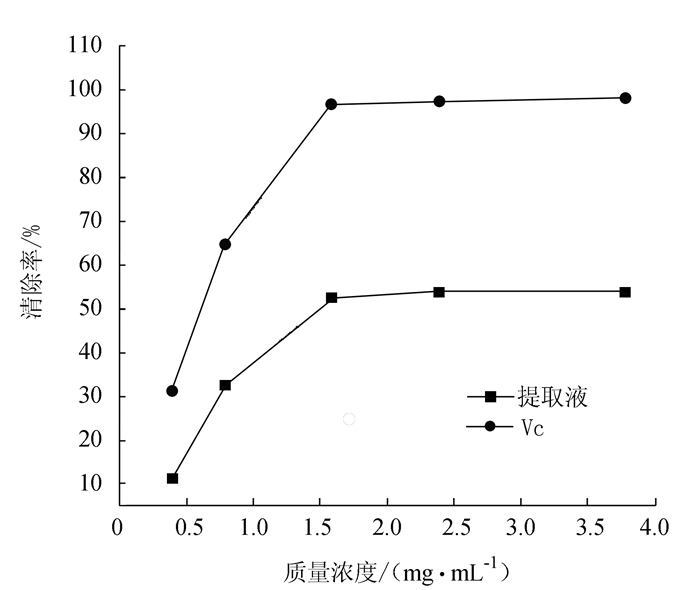
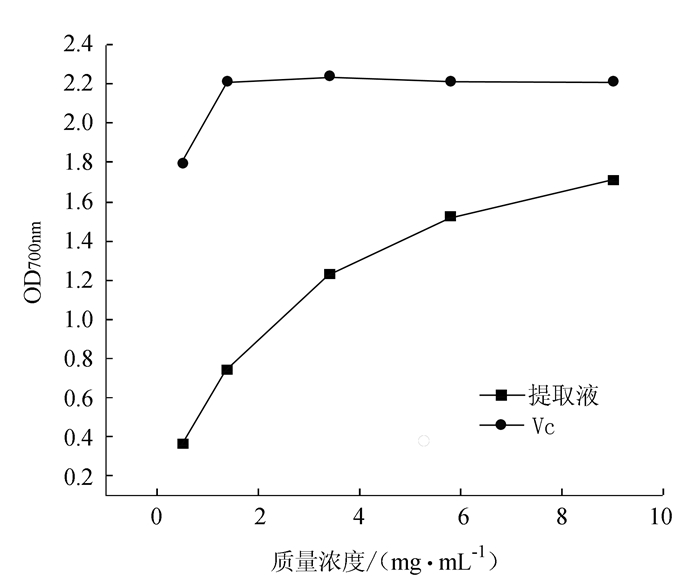
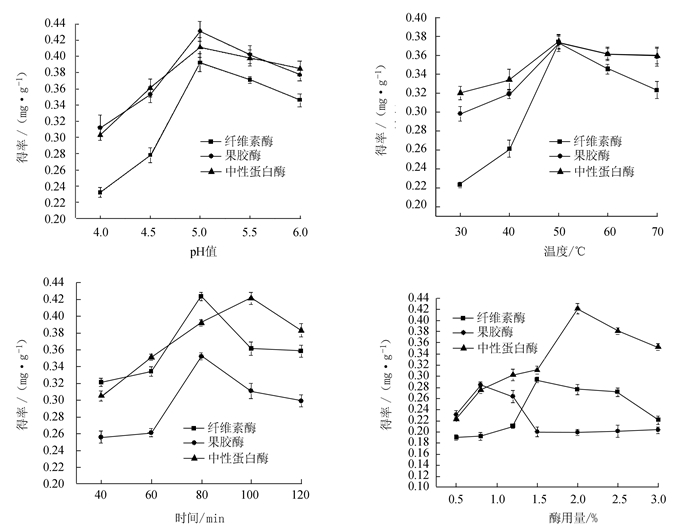
摘要: 利用响应面法优化酶辅助提取灵芝黄酮工艺。在酶解温度、酶解时间和酶用量3个单因素的基础上,利用Box-Benhnken实验设计原理对复合酶的最佳配比进行优化。同时对灵芝提取液的抗氧化活性进行研究。结果表明:在80 min、50℃、pH值为5.0的酶解条件下,最佳酶比例为纤维素酶:果胶酶:中性蛋白酶=2.07:0.86:2.11。在该条件下,灵芝黄酮实际提取率可达0.75 mg·g-1;并且灵芝提取液对DPPH自由基和羟自由基有一定的清除能力,同时具有较强的还原力。Abstract: Enzyme addition in the hot water extraction of flavonoids from Ganoderma lucidum was investigated for improvements on the extraction efficiency and/or enhancement on the antioxidant activity of the extract. The single factor test and the response surface methodology were used to optimize the processing conditions. It was found that a maximized yield of flavonoids of 0.75 mg/g could be obtained with the use of a combination of cellulase, pectinase and neutral proteinase in the ratio of 2.07:0.86:2.11 for the extraction at pH 5.0 and 50oC for 80 min. The resulting extract exhibited a high reducing power as well as free radical scavenging activities on DPPH and hydroxyl free radicals.
-
Keywords:
- Ganoderma lucidum /
- enzyme combinations /
- response surface /
- flavonoids
-
-
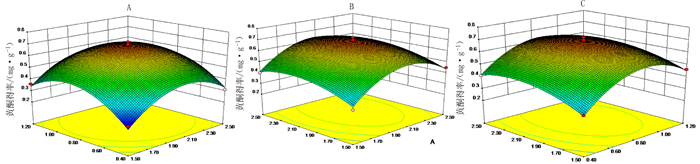
表 1 响应面试验设计
Table 1 Response surface experimental design
因素 水平 -1 0 1 X1纤维素酶/% 1.5 2 2.5 X2果胶酶/% 0.4 0.8 1.2 X3中性蛋白酶/% 1.5 2 2.5 表 2 响应面试验结果
Table 2 Response surface experimental results
试验
号X1
纤维素酶/%X2
果胶酶/%X3
中性蛋白酶/%黄酮得率
/(mg·g-1)1 1.50 0.80 2.50 0.4 2 2.00 0.80 2.00 0.63 3 1.50 1.20 2.00 0.36 4 2.00 0.80 2.00 0.72 5 2.50 1.20 2.00 0.4 6 2.00 1.20 1.50 0.46 7 2.00 0.80 2.00 0.67 8 2.00 0.80 2.00 0.7 9 2.50 0.40 2.00 0.31 10 2.50 0.80 1.50 0.45 11 1.50 0.80 1.50 0.3 12 1.50 0.40 2.00 0.24 13 2.00 1.20 2.50 0.5 14 2.00 0.40 2.50 0.41 15 2.00 0.40 1.50 0.32 16 2.50 0.80 2.50 0.53 17 2.00 0.80 2.00 0.69 表 3 黄酮得率回归系数及显著性检验
Table 3 Regression coefficient and significance test on flavone yield
变异来源 平方和 自由度 均方差 F值 P值 模型 0.3643 9 0.0405 26.01 0.0001** X1 0.0190 1 0.0190 12.22 0.0101* X2 0.0242 1 0.0242 15.55 0.0056** X3 0.0120 1 0.0120 7.72 0.0274* X1X2 0.0002 1 0.0002 0.14 0.7151 X1X3 0.0001 1 0.0001 0.06 0.8072 X2X3 0.0006 1 0.0006 0.40 0.5464 X12 0.1282 1 0.1282 82.38 <0.0001** X22 0.1246 1 0.1246 80.03 <0.0001** X32 0.0266 1 0.0266 17.10 0.0044** 残差 0.0109 7 0.0016 失拟项 0.0040 3 0.0013 0.77 0.5697 纯误差 0.0069 4 0.0017 总差 0.3752 16 R2=0.9710,RAdj2=0.9336,CV=8.33%,*P < 0.05,差异显著;**P < 0.01,差异极显著。 -
[1] 刘志恒.现代微生物学[M].北京:科学出版社, 2002. [2] 彭晓青, 程轩轩, 张旭红, 等.复合酶法提取龙眼核总黄酮的工艺研究[J].中国医院用药评价与分析, 2014, (2):134-138. http://www.cnki.com.cn/Article/CJFDTOTAL-YYPF201402014.htm [3] 王文渊, 周振华, 龙红萍.复合酶法提取苦瓜叶总黄酮的研究[J].中国食品添加剂, 2011, (4):107-112. http://www.cnki.com.cn/Article/CJFDTOTAL-ZSTJ201104020.htm [4] 张天笑, 刘红兵, 张文竹, 等.复合酶提取灵芝多糖工艺及其抗氧化能力研究[J].安徽农业科学, 2011, 39(8):4496-4498. http://www.cnki.com.cn/Article/CJFDTOTAL-AHNY201108036.htm [5] 白生文, 汤超, 田京, 等.沙棘果渣总黄酮提取工艺及抗氧化活性分析[J].食品科学, 2015, (10):59-64. http://www.cnki.com.cn/Article/CJFDTOTAL-SPKX201510014.htm [6] 李飞, 任清, 季超, 等.苦荞籽粒黄酮的提取纯化及抗氧化活性研究[J].食品科学技术学报, 2015, (6):57-64, 82. http://www.cnki.com.cn/Article/CJFDTOTAL-BQGB201506010.htm [7] 袁带秀, 舒丽霞, 黄蓉.杜仲黄酮对H22小鼠的抑瘤作用及其机制[J].中国老年学杂志, 2016, (2):291-293. http://www.cnki.com.cn/Article/CJFDTOTAL-ZLXZ201602016.htm [8] 李月娇, 王雪青, 陈亚蓝, 等.板栗花黄酮的提取工艺及其抑菌活性研究[J].食品工业科技, 2016, (10):298-302. http://www.cnki.com.cn/Article/CJFDTOTAL-SPKJ201610055.htm [9] 宿世震, 项东宇, 孟繁伟, 等.翻白草黄酮对2型糖尿病大鼠胰岛细胞的保护作用及机制研究[J].环球中医药, 2016, (2):145-148, 216. http://www.cnki.com.cn/Article/CJFDTOTAL-HQZY201602007.htm [10] 王昌涛, 孙啸涛, 周雪.响应面分析法优化雪灵芝黄酮提取工艺[J].食品科学, 2013, 34(14):91-95. http://www.cnki.com.cn/Article/CJFDTOTAL-SPKX201314019.htm [11] 任少红, 王峰, 丁静, 等.灵芝中总黄酮的含量测定[J].中国科技信息, 2009, (14):214. http://www.cnki.com.cn/Article/CJFDTOTAL-XXJK200914116.htm [12] HUA S Z, YINA J Y, NIEA S P, et al. In vitro evaluation of the antioxidant activities of carbohydrates[J].Bioactive Carbohydrates and Dietary Fibre, 2016, 7(2):19-27. DOI: 10.1016/j.bcdf.2016.04.001
[13] HUANG X Q, TU Z C, JIANG Y, et al. Dynamic high pressure microfluidization-assisted extraction and antioxidant activities of lentinan[J]. International Journal of Biological Macromolecules, 2012, 51(5):926-932. DOI: 10.1016/j.ijbiomac.2012.07.018
[14] YAMAGUCHI T, TAKAMURA H, MATOBA T, et al. HPLC method for evaluation of the free radical-scavenging activity of foods by using 1, 1-diphenyl-2-picrylhydrazyl[J]. Bioscience, biotechnology, and biochemistry, 1998, 62(6):1201-1204. DOI: 10.1271/bbb.62.1201
-
期刊类型引用(4)
1. 陈芳,温艳,姜小帆. 响应面法优化超声辅助提取灵芝黄酮工艺研究. 湖北农业科学. 2022(14): 113-118 .  百度学术
百度学术
2. 宋林晓,邵娟娟. 黄酮类化合物提取方法研究进展. 粮食与油脂. 2020(01): 21-22 .  百度学术
百度学术
3. 邱梦媛,胡亚林,林春穆,林立,范剑明,邹双全. 圆齿野鸦椿不同部位类黄酮与总三萜含量的比较及采收. 亚热带农业研究. 2019(03): 179-183 .  百度学术
百度学术
4. 肖建中,邹湘月,颜新培,邵元元,叶添梅,李霞. 桑枝基质的灵芝优质高效栽培配方研究. 四川蚕业. 2018(03): 20-23 .  百度学术
百度学术
其他类型引用(5)




 下载:
下载: