Effects of Nitrogen Fertilization on Growth and Grain Yield of Ratoon-rice, Tianyouhuazhan
-
摘要: 以天优华占为材料,头季设置5个氮肥水平(N0:0 kg·hm-2、N1:69.00 kg·hm-2、N2:138.00 kg·hm-2、N3:207.00 kg·hm-2、N4:276.00 kg·hm-2),再生季统一施用氮肥160.50 kg·hm-2,研究其对再生稻头季光合物质生产、两季产量及其构成因素的影响。结果表明,施用氮肥增加头季分蘖数和干物质积累,促进贮藏物质向籽粒的转运,过量施用氮肥会降低氮素农学利用效率。与N0处理相比,施用氮肥处理头季产量增加了12.12%~23.35%,N3处理最高。穗数随氮肥用量增加而增加,穗粒数则先增加后减少。再生季产量N4处理较0 kg·hm-2氮肥处理减少4.73%,其余处理产量增加1.61%~5.54%。再生季产量结构表现为穗数随头季氮肥增加呈减少趋势,穗粒数逐渐增加。试验表明,在福建中部山区条件下,天优华占再生季施用氮肥160.50 kg·hm-2条件下,头季氮肥用量为174.12 kg·hm-2最佳,可以充分发挥头季产量潜力,同时对再生季产量无显著影响,实现两季高产目标。Abstract: A ratoon-rice, Tianyouhuazhan, was used to study the effects of N application rates on the photosynthetic products and grain yield of the first-season and ratoon crops. Five rates of N fertilization, i.e., N0 at 0 kg·hm-2 (control), N1 at 69.00 kg·hm-2, N2 at 138.00 kg·hm-2, N3 at 207.00 kg·hm-2, and N4 at 276.00 kg·hm-2, were applied on the first crop. The fields were followed with a 160.50 kg·hm-2 application rate for the ratooning. The results showed that higher N fertilizations increased the tiller number, dry matter accumulation, and transporting of storage substances to the grains, but large amount nitrogen use decreased the N agricultural use efficiency (NAUE) on the first crop. The grain yields increased by 12.12% to 23.35% over that of N0 due to the fertilizations, with the greatest production achieved by N3. The panicle count and spikelets per panicle increased with the rate increases before reaching N4 level. For the ratoon crop, the increases on grain yield ranged from 1.61% to 5.54% as compared with N0. N4 also caused a yield reduction of 4.73% over control. The panicle count of the ratoon crop decreased with rising N application, while the spikelets per panicle increased. It appeared that a N fertilization of 174.12 kg·hm-2 for the first crop followed by 160.50 kg·hm-2 for the ratoon crop could maximize the combined grain production.
-
Keywords:
- nitrogen /
- ratoon-rice /
- growth /
- grain production
-
再生稻栽培可以减少育苗移栽等中间生产技术环节,节省种子和整地等费用,降低人力成本;再生稻生育期短,从头季收割到再生季成熟仅需60~80 d,为其他经济作物的种植争取了空间和时间,提高了光热和土地资源的利用效率[1],随着适合做再生稻栽培品种的育成和相应栽培技术的完善,再生稻产量不断提高,经济效益上与双季稻的差距呈减小甚至超过趋势[2],据统计我国再生稻适宜种植区面积为333.33万hm2,随着农业人口的减少,再生稻作为轻简高效栽培技术发展前景广阔[3]。再生稻区别于其他稻作方式的栽培措施主要是头季适宜的收获时期、留桩高度和再生季氮肥施用方式[4-8],其中氮素是再生季腋芽萌发与产量形成的重要影响因子。头季总施氮量固定的情况下,增加头季中后期氮肥施用比例,可以提高再生季叶片硝酸还原酶活性、叶绿素含量、净光合速率及根系活力,提高氮素利用率,增加干物质产量和头季产量[9-10]。头季施氮量不变的情况下,促芽肥可以提高再生季叶片光合生产能力,增加干物质积累,在一定氮素范围内,再生季促芽氮肥用量与产量呈抛物线相关关系,且不同品种再生稻栽培最佳氮肥用量不同,汕优明86在氮肥用量241.3 kg·hm-2时产量最高[11],佳辐占以138 kg·hm-2时产量最高[12]。前人研究主要集中于促芽氮肥对再生季氮素吸收与分配利用、干物质生产与转运、产量因子构成的影响,生产实践中人们已经注重再生季氮肥施用,而头季氮肥在满足头季需要的情况下往往出现富余[13],其对再生稻产量形成的影响研究较少,本试验主要研究再生季氮肥用量固定的情况下,头季不同氮肥施用量对头季干物质生产、两季产量形成的影响,以期阐明头季氮肥对再生稻产量形成的作用机理,为福建省中部山区再生稻高产高效栽培与氮肥合理施用提供理论依据和技术支持。
1. 材料与方法
1.1 试验材料与设计
试验地点设置在福建省尤溪县,尤溪县光热资源适于种植再生稻,全县常年种植面积达到0.53万hm2,平均头季产量9 027 kg·hm-2、再生季4 524 kg·hm-2[14]。供试材料为适合当地机械化栽培的三系杂交水稻天优华占,2014年3月13日播种,4月17日移栽,移栽前各处理统一施过磷酸钙375 kg·hm-2,拔节始期统一施用氯化钾150 kg·hm-2,氮肥设置5个水平,各处理施用时期和施肥量见表 1,小区面积4 m×5 m,3次重复。头季稻7月28日收割,收割前10 d和收割后10d各处理施用尿素150 kg·hm-2,收割后20 d各处理施用三元复合肥150 kg·hm-2(养分含量N:P2O5:K2O=15:15:15),9月30日收割再生季,其他措施与大田常规高产管理相同。
表 1 不同处理氮肥施用方法Table 1. Rates and times of N fertilization[单位/(kg·hm-2)] 处理 头季 再生季 总计 移栽后7 d 移栽后30 d 拔节期 剑叶露尖 收获前10 d 收获后7 d 收获后2 1d 头季 再生季 N0 0 0 0 0 69.00 69.00 22.50 0 160.50 N1 34.5 17.25 17.25 0 69.00 69.00 22.50 69.00 160.50 N2 69.00 34.50 34.50 0 69.00 69.00 22.50 138.00 160.50 N3 103.50 51.75 34.50 17.25 69.00 69.00 22.50 207.00 160.50 N4 138.00 69.00 34.50 34.50 69.00 69.00 22.50 276.00 160.50 1.2 测定项目与方法
1.2.1 生长发育记载
移栽至齐穗期,定点每隔7 d观察记载分蘖消长动态,并用红笔标记主茎叶尖,记录叶龄。
1.2.2 干物质积累和叶面积
分别于移栽期、拔节期、齐穗期和成熟期,各处理选取代表性植株3丛,分叶、茎鞘和穗置于烘箱中105℃下杀青30 min,80℃下烘干至恒重,称量各器官干物重。另取20片鲜叶,用长宽系数法测量叶面积和相应干物重,利用比重法计算绿叶面积。
干物质表观转化率/%=[(齐穗期营养器官干物质重-成熟期营养器官干物质重)/(成熟期穗干物质重-齐穗期穗干物质重)]×100%
氮素农学利用率/%=[(施氮处理区产量-不施氮肥处理区产量)/氮肥施用量]×100%。
1.2.3 产量及产量构成因素
成熟区每小区连续选择40丛调查穗数,按平均数选取5丛观察单穗总粒数、每穗实粒数、千粒重,计算理论产量,按小区收获计算实际产量。
1.3 数据处理
使用Microsoft Excel 2003进行数据处理,DPS软件进行统计分析。
2. 结果与分析
2.1 头季茎蘖动态
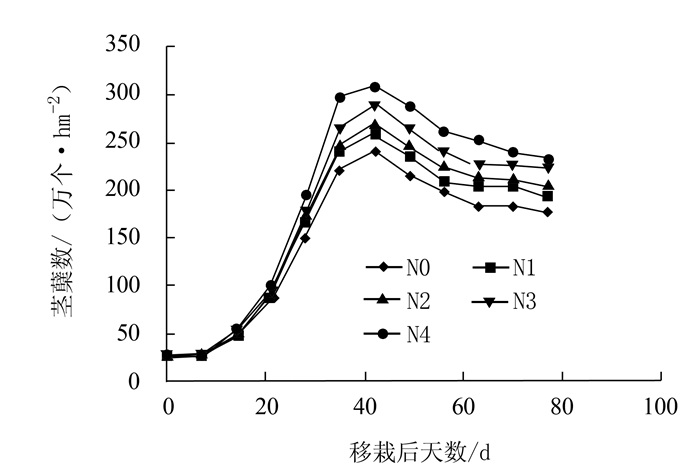
由图 1可知,随生育进程的推进,分蘖数逐渐增加,最大分蘖出现在移栽后第6周(拔节前1周),之后随着无效分蘖的消亡而减少,齐穗后茎蘖数趋于稳定。施氮处理各个时期分蘖数均超过不施氮肥处理,并且随着氮肥用量增加而增加。各处理最高分蘖为224.3~298.1万个·hm-2,N1、N2、N3和N4分别较对照N0增加7.01%、11.35%、19.73%和27.48%。不同处理最终成穗率为73.32%~77.66%,各施氮处理与N0差异显著,增加幅度为2.67%~4.33%。
2.2 头季干物质积累与转运
干物质积累是作物产量形成的基础。移栽至拔节期、拔节期至齐穗期叶片和茎鞘等营养器官干物质净积累量为正值,齐穗到成熟期随着干物质向籽粒中转运,营养器官干物质净积累量变为负值(表 2)。移栽到拔节期各个器官干物质净积累量随氮肥增加而增加,各处理与N0处理差异显著;拔节至齐穗期干物质净积累量与齐穗到成熟期贮藏物质输出量、干物质表观转化率均表现为N3>N4>N2>N1>N0,齐穗至成熟期则相反,且净积累量皆为负值,不同氮肥处理间差异显著。说明氮肥对水稻生育后期干物质积累和转运具有促进作用,但是当氮肥超过一定用量时这种效应开始下降。
表 2 不同施氮水平下头季干物质净积累量Table 2. Net dry matter accumulation on rice plants treated with different N fertilizations in first crop[单位/(g·m-2)] 处理 移栽~拔节 拔节~齐穗 齐穗~成熟 贮藏物质输出量 表观转化率/% 叶片 茎鞘 叶片 茎鞘 穗 叶片 茎鞘 穗 N0 149.38c 146.19e 160.33bc 412.84c 168.50d -67.75c -103.79e 637.50c 171.54d 26.91b N1 163.38b 179.16d 161.75b 433.64b 194.78c -72.50b -118.81d 685.47b 191.31c 27.91b N2 169.46b 206.08c 166.33ab 452.15b 217.67b -76.25a -130.57c 737.66a 206.82b 28.04b N3 191.88a 225.75b 168.50a 516.16a 239.83a -78.09a -147.17a 765.75a 225.26a 29.42a N4 198.79a 264.24a 171.34a 457.84b 224.34b -73.75b -137.92b 750.74a 211.67b 28.19ab 注:同列数据后不同小写字母表明在5%水平上差异显著,下同。 2.3 再生稻产量及产量构成因子
2.3.1 头季产量结构
头季产量与氮肥用量呈抛物线型关系,不同氮肥处理之间以N3产量最高(表 3)。各施氮处理比不施N空白处理增产幅度为12.12%~23.35%,方差分析结果表明差异达显著水平,N2、N3和N4处理之间产量无显著差异。在头季产量构成各因素中,每667 m2穗数随氮肥施用量的增加而增加,施氮处理与不施氮肥处理差异显著;每穗总粒数随氮肥增加呈先增加后减少的趋势,N2处理较N0处理显著增加,其余处理差异不显著;结实率和千粒重则在不同氮肥水平下差异不显著。结果表明在一定范围内,施用氮肥可以同步提高穗数和穗粒数,再继续增加氮肥后,在千粒重相对稳定的情况下,穗数的增加对产量的正效应不能补偿穗粒数下降对产量造成的损失。
表 3 头季产量和产量构成因素、氮素农学利用率Table 3. Grain yield, yield components and NAUE of first crop季别 处理 穗数/
(万穗·hm-2)总粒数 实粒数 结实率
/%千粒重
/g产量/
(kg·hm-2)氮农学利用率
/%头季 N0 177.30c 188.90bc 166.97b 88.37a 25.69a 7508.55c - N1 196.65b 193.83ab 171.63b 88.50a 25.74a 8481.45b 14.10a N2 207.15b 201.40a 180.33a 89.53a 25.55a 9106.50a 11.58b N3 224.70a 189.03bc 170.37b 90.10a 25.47a 9261.45a 8.47c N4 232.95a 182.07c 162.87b 89.47a 25.22a 9066.45a 5.64d 2.3.2 再生季产量结构
头季氮肥用量不同,再生季各处理统一施用促芽促蘖肥160.50 kg·hm-2后,再生季产量与头季产量变化趋势不一致,表现为N1>N2>N3>N0>N4(表 4)。N1比N0处理增产了325.50 kg·hm-2,增幅达5.54%,而N4则比N0处理减产277.95 kg·hm-2,降幅达4.73%,差异均达到显著水平。在产量构成各因素中,穗数、结实率随头季氮肥施用量的增加而减少,而每穗总粒数随头季氮肥施用量的增加而增加,各施肥处理与N0比较差异显著;千粒重则在不同氮肥水平下差异不显著。表明头季氮肥施用过量,不利于再生季产量的形成。
表 4 再生季产量和产量构成因素、氮素农学利用率Table 4. Yield, yield components, and NAUE of ratoon crop季别 处理 穗数/
(万穗·hm-2)总粒数 实粒数 结实率
/%千粒重
/g产量/
(kg·hm-2)氮农学利用率
/%再生季 N0 396.60a 77.77c 65.97b 84.83a 24.53a 5877.00b - N1 369.00b 87.97b 73.33a 83.43a 24.30a 6202.50a 4.72a N2 351.60bc 89.73b 74.47a 82.97ab 24.23a 6054.45ab 1.28b N3 334.05cd 93.40ab 75.67a 81.03b 24.08a 5971.50ab 0.46c N4 313.20d 96.70a 78.17a 80.83b 24.01a 5599.05c -1.01d 2.4 氮素农学利用率
不同施氮水平氮素农学利用率不同,头季和再生季均呈现随氮素施用量增加氮素农学利用率依次递减的趋势,不同处理之间差异显著(表 3、4)。头季氮肥超过N3处理时,再生季氮素农学利用率逐步降为零甚至负数,表明头季氮肥施用过多,再生季依然施入充足的氮肥,会造成产量降低,肥料利用率下降。生产实践中,头季氮肥充足的情况下,再生季可酌情减少肥料用量。
2.5 头季最佳氮素施用量
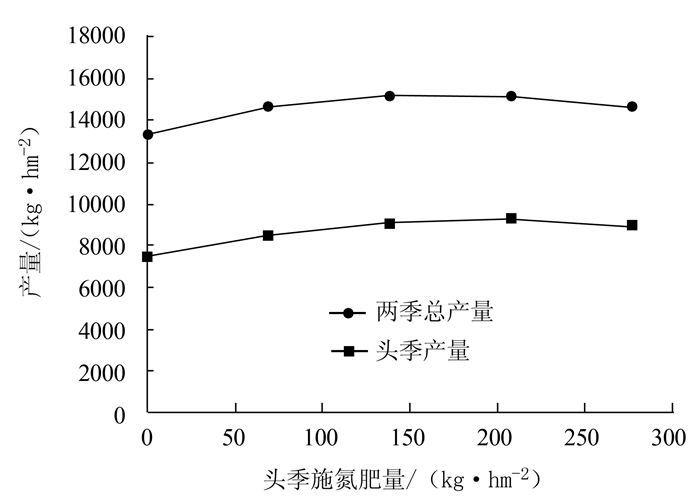
由图 2可知,再生稻头季产量、两季总产量与头季施氮量均呈抛物线型相关,其回归方程分别为:
y=−0.0421x2+17.265x+7504.8,R2=0.9996y=−0.0621x2+21.636x+13413,R2=0.9957 由方程① 计算可知,头季产量最高为9 274.87 kg·hm-2,相应施氮量为205.05 kg·hm-2,代入,两季总产量为15 238.44 kg·hm-2;由方程计算可知两季总产量最高可达到15 297.59 kg·hm-2,相应头季氮肥用量为174.20 kg·hm-2,代入方程,得到相应头季产量为9 234.92 kg·hm-2,再生季产量为6 062.73 kg·hm-2,表明天优华占再生季施氮量160.50 kg·hm-2时,头季合理施氮定于174.20 kg·hm-2两季总产量最高。
3. 讨论与结论
干物质积累和转运是作物产量形成的基础,头季和再生季对碳水化合物转运和分配的争夺存在矛盾,这因为头季稻产量主要来自于花后叶片光合物质直接转运和抽穗前营养器官积累的可溶性碳水化合物的再转运,光合同化物向籽粒分配多,营养器官贮藏少的品种产量高[15]。另一方面,对再生季来说,叶片进行光合作用前,腋芽萌发所需的能量全部来自于头季稻桩贮存的碳水化合物,稻桩中超过50%的同化产物最终转运到再生稻体内[16],这就需要头季同化物较多的贮存在茎秆中,尽量减少向籽粒的转运,因此协调二者之间的平衡很重要。本研究表明头季施用氮肥减少头季营养器官干物质净积累量,增加碳水化合物向籽粒中转运,并且头季产量和营养器官贮藏物质输出量、表观转变率变化趋势一致,再生季产量和头季干物质净积累量没有明显的相关性。
产量是由穗数、穗粒数和千粒重构成,一般来说千粒重是相对稳定的性状,杨惠杰指出头季穗粒数是产量的决定因素,再生季穗数是产量的决定因素[17]。本研究表明施用氮肥促进分蘖发生,随氮肥增加分蘖成穗数增加,超过一定量之后(138.00 kg·hm-2),总粒数和实粒数开始降低,头季产量并没有随穗数增加而相应增加,其原因是分蘖数多,无效分蘖随之增多,造成穗粒数降低[18]。再生季产量则随着头季氮量的增加而逐渐降低,分析其产量构成因子表明,产量降低是由于头季施氮量的增加减少了再生季穗数,虽然单穗粒数增加,但不能弥补穗数减少对产量造成的损失,这和杨惠杰穗数是再生季产量主要贡献因子的结论一致。
徐富贤[19]指出,再生季施肥决定于头季稻植株营养水平,在头季营养状况充足的情况下,可以少施或者不施促芽肥,同时提出了头季植株营养过剩的诊断指标。生产实践中人们头季和再生季都施用足够的氮肥,本研究表明从肥料利用率来看,无论是头季还是再生季,氮素农学利用率与氮肥水平呈现相反的变化趋势,在头季氮肥用量超过207.00 kg·hm-2时,其再生季产量的农学利用率接近于零的水平。本试验条件下,从两季总产量和氮肥利用率的角度考虑,天优华占再生季施氮量160.50 kg·hm-2的情况下,头季合理氮肥用量为174.20 kg·hm-2。
-
表 1 不同处理氮肥施用方法
Table 1 Rates and times of N fertilization
[单位/(kg·hm-2)] 处理 头季 再生季 总计 移栽后7 d 移栽后30 d 拔节期 剑叶露尖 收获前10 d 收获后7 d 收获后2 1d 头季 再生季 N0 0 0 0 0 69.00 69.00 22.50 0 160.50 N1 34.5 17.25 17.25 0 69.00 69.00 22.50 69.00 160.50 N2 69.00 34.50 34.50 0 69.00 69.00 22.50 138.00 160.50 N3 103.50 51.75 34.50 17.25 69.00 69.00 22.50 207.00 160.50 N4 138.00 69.00 34.50 34.50 69.00 69.00 22.50 276.00 160.50 表 2 不同施氮水平下头季干物质净积累量
Table 2 Net dry matter accumulation on rice plants treated with different N fertilizations in first crop
[单位/(g·m-2)] 处理 移栽~拔节 拔节~齐穗 齐穗~成熟 贮藏物质输出量 表观转化率/% 叶片 茎鞘 叶片 茎鞘 穗 叶片 茎鞘 穗 N0 149.38c 146.19e 160.33bc 412.84c 168.50d -67.75c -103.79e 637.50c 171.54d 26.91b N1 163.38b 179.16d 161.75b 433.64b 194.78c -72.50b -118.81d 685.47b 191.31c 27.91b N2 169.46b 206.08c 166.33ab 452.15b 217.67b -76.25a -130.57c 737.66a 206.82b 28.04b N3 191.88a 225.75b 168.50a 516.16a 239.83a -78.09a -147.17a 765.75a 225.26a 29.42a N4 198.79a 264.24a 171.34a 457.84b 224.34b -73.75b -137.92b 750.74a 211.67b 28.19ab 注:同列数据后不同小写字母表明在5%水平上差异显著,下同。 表 3 头季产量和产量构成因素、氮素农学利用率
Table 3 Grain yield, yield components and NAUE of first crop
季别 处理 穗数/
(万穗·hm-2)总粒数 实粒数 结实率
/%千粒重
/g产量/
(kg·hm-2)氮农学利用率
/%头季 N0 177.30c 188.90bc 166.97b 88.37a 25.69a 7508.55c - N1 196.65b 193.83ab 171.63b 88.50a 25.74a 8481.45b 14.10a N2 207.15b 201.40a 180.33a 89.53a 25.55a 9106.50a 11.58b N3 224.70a 189.03bc 170.37b 90.10a 25.47a 9261.45a 8.47c N4 232.95a 182.07c 162.87b 89.47a 25.22a 9066.45a 5.64d 表 4 再生季产量和产量构成因素、氮素农学利用率
Table 4 Yield, yield components, and NAUE of ratoon crop
季别 处理 穗数/
(万穗·hm-2)总粒数 实粒数 结实率
/%千粒重
/g产量/
(kg·hm-2)氮农学利用率
/%再生季 N0 396.60a 77.77c 65.97b 84.83a 24.53a 5877.00b - N1 369.00b 87.97b 73.33a 83.43a 24.30a 6202.50a 4.72a N2 351.60bc 89.73b 74.47a 82.97ab 24.23a 6054.45ab 1.28b N3 334.05cd 93.40ab 75.67a 81.03b 24.08a 5971.50ab 0.46c N4 313.20d 96.70a 78.17a 80.83b 24.01a 5599.05c -1.01d -
[1] 徐富贤, 熊洪, 张林, 等.再生稻产量形成特点与关键调控技术研究进展[J].中国农业科学, 2015, 48(9):1702-1717. DOI: 10.3864/j.issn.0578-1752.2015.09.04 [2] 陈家威, 卓传营.尤溪县发展再生稻生产的主要措施[J].福建稻麦科技, 2011, (3):58-59. http://www.cnki.com.cn/Article/CJFDTOTAL-FJDM201101040.htm [3] 熊洪, 冉茂林, 徐富贤, 等.南方稻区再生稻研究进展及发展[J].作物学报, 2000, 26(3):298-304. http://www.cnki.com.cn/Article/CJFDTOTAL-XBZW200003007.htm [4] 何花榕, 房贤涛, 翁国华, 等.留桩高度对再生稻生长发育和产量的影响研究现状及展望[J].中国农学通报, 2012, 28(9):6-10. http://www.cnki.com.cn/Article/CJFDTOTAL-ZNTB201209004.htm [5] 易镇邪, 周文新, 屠乃美.留桩高度对再生稻源库性状与物质转运的影响[J].中国水稻科学, 2009, 23(5):509-516. http://www.cnki.com.cn/Article/CJFDTOTAL-ZGSK200905012.htm [6] HIROSHI NAKANO, SATOSHI MORITA. Effects of time of first harvest, total amount of nitrogen, and nitrogen application method on total dry matter yield in twice harvesting of rice[J].Field Crops Research, 2008, (105):40-47. http://www.sciencedirect.com/science/article/pii/S0378429007001384
[7] DUSTIN L, HARRELL, JASON A, et al.Evaluation of main-crop stubble height on ratoon rice growth and development[J].Field Crops Research, 2009, (114):396-403. http://www.cabdirect.org/abstracts/20093352869.html
[8] BOND J A, BOLLICK P K. Ratoon rice response to nitrogen fertilizer[M]. Crop Management, 2006.
[9] 杨东, 陈鸿飞, 卓传营, 等.头季不同施氮方式对再生稻生理生化的影响[J].中国生态农业学报, 2009, 17(4):643-646. http://www.cnki.com.cn/Article/CJFDTOTAL-ZGTN200904006.htm [10] 陈鸿飞, 杨东, 梁义元, 等.头季稻氮肥运筹对再生稻干物质积累、产量及氮素利用率的影响[J].中国生态农业学报, 2010, 18(1):50-56. http://www.cnki.com.cn/Article/CJFDTOTAL-ZGTN201001011.htm [11] 姜照伟, 林文雄, 李义珍, 等.不同氮肥施用量对再生稻氮素吸收和分配的影响[J].福建农业学报, 2003, 18(1):50-55. http://www.fjnyxb.cn/CN/abstract/abstract1085.shtml [12] 廖海林, 熊顺贵, 郑景生, 等.再生稻佳辐占再生季施肥试验初报[J].福建农业学报, 2014, 29(7):646-650. http://www.fjnyxb.cn/CN/abstract/abstract2473.shtml [13] 何海兵, 杨茹, 廖江, 等, 水分和氮肥管理对灌溉水稻优质高产高效调控机制的研究进展[J].中国农业科学, 2016, 49(2):305-318. http://www.cnki.com.cn/Article/CJFDTOTAL-ZNYK201602011.htm [14] 张水金, 杨东, 董瑞霞, 等.尤溪县再生稻生产发展状况[J].福建稻麦科技, 2012, 30(1):81-83. http://www.cnki.com.cn/Article/CJFDTOTAL-FJDM201201031.htm [15] 杨建昌, 张文虎, 手志琴, 等.水稻新株型与粳/籼杂种源库特征与物质运转的研究[J].中国农业科学, 200l, 34(5):465-468.. http://www.cnki.com.cn/Article/CJFDTOTAL-ZNYK200105009.htm [16] 刘爱中, 张胜文, 屠乃美.稻桩贮藏同化产物的分配与再生稻腋芽再生率及产量构成的关系[J].华北农学报, 2008, 23(3):190-193. DOI: 10.7668/hbnxb.2008.03.045 [17] 杨惠杰, 郑景生, 姜照伟.再生稻超高产库的结构特征[J].福建农业学报, 2005, 20(2):65-68. http://www.fjnyxb.cn/CN/abstract/abstract933.shtml [18] 李木英, 石庆华, 王涛.谭雪明种植密度对双季超级稻群体发育和产量的影响[J].杂交水稻, 2009, 24(2):72-77. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=zjsd200902031&dbname=CJFD&dbcode=CJFQ [19] 徐富贤, 熊洪, 朱永川, 等.再生稻促芽肥高效施用量与头季稻齐穗期库源结构关系[J].西南农业学报, 2006, 19(5):833-837. http://www.cnki.com.cn/Article/CJFDTOTAL-XNYX200605012.htm -
期刊类型引用(4)
1. 王敏羽,戴志刚,余德芳,王向平,关绍华,邵远刚,张家学,李小坤. “水稻-再生稻”种植模式专用肥轻简施用对产量、肥料利用率及经济效益的影响. 中国水稻科学. 2022(05): 531-542 .  百度学术
百度学术
2. 余延丰,张富林,刘冬碧,吴茂前,张志毅,夏颖,范先鹏,王玲,肖依波,肖国平. 氮肥用量和运筹方式对再生稻产量品质和氮肥利用率的影响. 中国土壤与肥料. 2022(12): 133-140 .  百度学术
百度学术
3. 周瑜,李泽碧,张亚勤,吴毓,黄娟. 主季种植密度和施氮量对高粱再生产量的影响. 中国农业大学学报. 2021(08): 43-53 .  百度学术
百度学术
4. 刘锋. 头季不同氮肥施用量对再生稻两优616干物质生产及产量的影响. 福建稻麦科技. 2021(03): 17-21 .  百度学术
百度学术
其他类型引用(10)




 下载:
下载: