Heterogeneity of Tomato Metabolites induced by Ralstonia solanacearum with Varied Pathogenicity
-
摘要: 采用基于气相色谱-质谱联用技术的代谢组学方法,研究不同致病性青枯雷尔氏菌诱导番茄植株代谢物变化的异质性。将青枯雷尔氏菌强致病力菌株FJAT-91和无致病力菌株FJAT-1458分别单独接种和混合接种番茄植株,以清水为对照,接种后6、24、48、72、96 h取样,测定番茄植株代谢产物的变化。结果表明,检测到的代谢物种类主要为醇类、酯类、酸类、醛类、吡啶类和烷烃类。不同处理番茄代谢产物组成变化的时间动态结果表明,FJAT-91单独接种处理48 h、FJAT-1458单独接种处理48 h、同时接种FJAT-91和FJAT-1458处理96 h及对照处理72、96 h的番茄中检测到代谢物种类最多,分别为12、18、15和15种。邻苯二甲酸二丁酯在不同处理不同时间的番茄中均检测到,为完全分布类型,其他代谢物为不完全分布类型。FJAT-91单独接种处理能诱导番茄代谢产物棕榈酸消亡,而FJAT-1458单独接种或与菌株FJAT-91混合接种及对照处理的番茄植株该代谢物维持在相当含量,说明该代谢物可能与植株免疫抗病有关。主成分分析表明,不同接种处理诱导番茄植株的代谢谱存在一定的差异,主成分一和主成分二基本上能将其区分开来。Abstract: Gas chromatography-mass spectrometry was employed for the investigation on the heterogeneity of metabolites in tomato plants infected by strains of Ralstonia solanacearum with varied pathogenicity. The plants were inoculated with the virulent FJAT-91 and/or avirulent FJAT-1458, as well as water as control. After 6, 24, 48, 72 and 96 h, metabolites in the plants were analyzed. The results showed the metabolites were mostly alcohols, esters, acids, aldehydes, pyridines, and alkanes. The compositional differences on the plants infected by different pathogenic strains were compared. It was found that the number of metabolite varieties in the plants varied by the treatments and time. The tomato plants treated by FJAT-91 for 48 h had 12 different metabolites; those treated by FJAT-1458 for 48 h, 18;those treated by both strains simultaneously for 96 h, 15;and, control treated for 72 or 96 h, 15. Dibutyl phthalate was the only metabolite present in all samples. n-hexadecanoic acid was absent in the plants inoculated with FJAT-91, but was detected at considerable amounts in those infected with FJAT-1458 or combined strains, and control. The discrepancy might be due to a variation in the immunology of the tomato plants. A principal component analysis on the metabolites revealed discernible differences among the tomato plants that received different treatments. It suggested that the viral infections could be identified by comparing the two most abundant metabolites in a plant.
-
Keywords:
- tomato /
- bacterial wilt disease /
- Ralstonia solanacearum /
- GC-MS
-
由致病性青枯雷尔氏菌Ralstonia solanacearum Yabuuchi et al.引起的番茄青枯病是一种毁灭性的土传病害,广泛分布在热带和亚热带地区[1]。青枯病在番茄中危害严重,一旦发病难以控制,造成植株大面积枯萎死亡和果实产量的严重下降,轻病田块减产10%~30%,重病田块减产50%以上,甚至绝收,严重制约着番茄产业的发展和经济效益的提高[2]。目前该病害尚未得到有效防治[3]。青枯雷尔氏菌无病力菌株能在一定程度上控制青枯病的发展,具有一定生防潜力[4]。青枯雷尔氏菌与番茄互作会诱导其代谢物发生变化,比较分析强、弱青枯雷尔氏菌株诱导番茄代谢产物变化的异质性,对于阐明强致病力菌株的致病机制和无致病力菌株的诱导抗病机制具有重要的参考价值。
代谢组学是研究生物体受刺激或扰动而引起的体内代谢物的定性和定量变化,并将代谢信息与生物体的病理生理过程关联起来,从而了解生物体生命活动的代谢过程[5-6]。代谢组学技术可对植物获得系统抗性发生过程中的所有代谢物进行定性和定量分析,并能识别未知代谢产物,该技术的发展和应用有助于我们更好了解生物体各种复杂相互作用及生物系统对外界因素干扰的应答反应[7-8],已成为系统生物学研究的主要手段之一。作为众多化学分析方法中的一种,气相色谱-质谱(GC-MS)技术由于具有快速、高灵敏度和高分辨率,已成为代谢组学研究的首要技术[9-11]。
目前,不同致病力青枯雷尔氏菌与番茄互作的代谢机制研究未见报道。本研究运用GC-MS技术对青枯雷尔氏菌强、弱菌株侵染番茄植株诱导其代谢产物的变化进行了初步研究,在代谢物水平上为进一步揭示青枯雷尔氏菌与番茄寄主互作机制提供依据。
1. 材料与方法
1.1 材料
青枯雷尔氏菌致病性菌株FJAT-91和无致病力菌株FJAT-1458分别分离自番茄青枯病病株和健康植株,由福建省农业科学院农业生物资源研究所菌种库收集并保存。青枯雷尔氏菌鉴别培养基为TTC(1%蛋白胨、0.1%水解酪蛋白、0.5%葡萄糖、1.8%琼脂和0.05% 2, 3, 5-氯化三苯基四氮唑),液体培养基为SP培养基(2%蔗糖、0.5%蛋白胨、0.05%KH2PO4和0.0025%MgSO4)。
1.2 菌株活化及培养液制备
将菌株FJAT-91和FJAT-1458活化于TTC培养基上,30℃培养48 h,挑取单菌落转接种于35 mL SP液体培养基中,30℃、170 r·min-1振荡培养48 h后,将培养液涂布于TTC平板上,30℃培养48 h后统计活菌数,确定FJAT-91和FJAT-1458培养液的原始浓度。2种培养液均用无菌水稀释至1.0×108 cfu·mL-1备用。
1.3 接种处理
采用伤根接种法,接种至5~6叶龄的番茄(金石王1号)盆栽苗。各处理如下,处理1:只接种菌株FJAT-91,接种1.0×108 cfu·mL-1,接种量80 mL·盆-1;处理2:只接种菌株FJAT-1458,接种1.0×108 cfu·mL-1,接种量80 mL·盆-1;处理3:同时接种菌株FJAT-91和FJAT-1458,二者接种均为1.0×108cfu·mL-1,2种菌等量混合后接种,接种量为80 mL·盆-1;处理4:清水对照,80 mL·盆-1,各处理设3个重复。处理后6、24、48、72、96 h取植株叶片约5 g,同种处理不同重复的叶片混合成小样,-80℃冰箱保存备用。
1.4 番茄植株代谢产物的提取
番茄植株代谢产物的提取参照Jan等[12]的方法进行,具体步骤如下:(1) 每个样本设3次重复,分别称重1 g,液氮研磨后置于2 mL离心管中;(2) 加入100%甲醇至1.5 mL,涡旋混匀;(3) 加入60 μL核糖醇(0.2 mg·mL-1)涡旋10 s;(4)70℃,水浴15 min;(5)10 000 r·min-1离心15 min;(6) 将分层的上层溶液转移至10 mL玻璃管中;(7) 加入750 μL氯仿(-20℃预冷),再加入1.5 mL ddH2O(4℃预冷),涡旋10 s;(8)6 000 r·min-1离心15 min;(9) 转移上层相至一个新的三角瓶中;(10) 氮吹仪吹干有机溶剂;(11) 加入40 μL methoxyamination试剂(需新制现用现配:1 mg methoxyamine hydrochloride+50 μL纯吡啶),37℃、250 r·min-1振荡120 min;(12) 加入70 μL MSTFA(N-甲基-N-三甲基硅烷基三氯乙酰胺)试剂(4℃预冷);(13) 加入10 μL正十八烷时标试剂(0.22 mg·mL-1溶于纯吡啶中),37℃、250 r·min-1振荡30 min;(14) 转入GC-MS玻璃小瓶;(15) GC-MS分析。
1.5 番茄植株代谢产物的GC-MS分析
气相色谱-质谱联用仪为Agilent 7890A/5975C,色谱柱为HP5-MS。气相色谱条件:分流比10:1,进样口温度250℃,柱温50℃;起始温度50℃,保持2 min;6℃·min-1升温到250℃,保持5 min;20℃·min-1升到280℃,保持5 min。质谱条件:离子源EI;采集模式为全扫描;EMV模式为相对值;质量扫描范围:50.00~550.00 amu;MS离子源温度为230℃,MS四级杆温度150℃。
1.6 番茄植株代谢产物的鉴定
数据经NIST谱库检索,匹配度大于80%的鉴定化合物予以报道[13]。采用峰面积归一化法,以各组分的峰面积占总峰面积之比值表示组分相对含量。
1.7 主成分分析
采用DPS7.05软件,以不同处理不同时间番茄叶片为样本,以各样本中各代谢物相对含量为指标,进行主成分分析。主成分分析过程采用DPS7.05软件的相关模块进行处理,主要包括数据求协方差矩阵,计算特征方程中所有特征值,并根据特征值累积比例确定主成分的数量,计算主成分载荷值和主成分得分,进行一级主成分评分等。
2. 结果与分析
2.1 代谢产物的鉴定
利用NIST05质谱数据库对谱图中的代谢物逐一进行检索和鉴定,通常匹配度高于80%的化合物较为可信予以报道[13]。根据这一原则,各类化合物在不同处理番茄植株中的分布情况如表 1所示,只接种青枯雷尔氏菌致病性菌株FJAT-91的番茄植株中,酯类和烷烃类化合物在不同处理时间均有分布,而醛类化合物均未检测到,醇类化合物除了处理6 h均检测,酸类化合物只在接种初期(6、24、48 h)番茄植株分布,吡啶类化合物只在接种后期(72 h和96 h)有分布;接种青枯雷尔氏菌无致病力菌株FJAT-1458的番茄植株,酯类、酸类和烷烃类化合物在不同处理时间均有分布,醇类除接种48 h均检测到分布,醛类和吡啶类化合物除接种初期(6、24 h),在其他时期均检测到;同时接种FJAT-91和FJAT-1458的番茄植株中,酯类除了接种48 h、酸类除了接种6 h和吡啶类除了接种24、72 h,其他接种时期均检测到这类化合物;对照处理的番茄植株中,各类化合物分布情况与只接种FJAT-1458相似。
表 1 不同接种处理下番茄代谢产物的种类和数量Table 1. Types and numbers of detected compounds under different treatments处理 化合物类型 化合物种类数目/种 6 h 24 h 48 h 72 h 96 h 只接种FJAT-91 醇类 ND 2 1 3 2 酯类 1 1 3 1 1 酸类 2 2 3 ND ND 醛类 ND ND ND ND ND 哌啶类 ND ND ND 1 1 烷烃类 2 2 1 1 2 只接种FJAT-1458 醇类 1 2 ND 1 2 酯类 1 4 3 2 1 酸类 1 2 7 1 2 醛类 ND ND 1 1 1 哌啶类 ND ND 1 1 1 烷烃类 3 2 1 1 3 同时接种FJAT-91和FJAT-1458 醇类 2 1 ND 4 2 酯类 1 4 2 3 5 酸类 1 2 3 2 2 醛类 ND 1 1 1 1 哌啶类 1 ND 1 ND 2 烷烃类 2 2 3 1 3 清水对照 醇类 1 ND ND 2 1 酯类 1 1 2 4 1 酸类 1 1 2 2 1 醛类 ND ND 2 1 1 哌啶类 ND ND 1 1 1 烷烃类 2 2 2 1 3 注:ND表示未检测到该类化合物。 2.2 不同处理番茄代谢产物组成变化的时间动态
比较不同处理番茄代谢产物组成变化的时间动态,结果表明,FJAT-91处理不同时间的番茄代谢物组成不同,处理6、24、48、72、96 h的番茄中分别检测到5、10、12、7、7种代谢物,其中邻苯二甲酸二丁酯在各时间均检测到,为完全分布类型,其他代谢物随时间呈不完全分布;FJAT-1458处理6、24、48、72、96 h的番茄中分别检测到6、9、18、12、10种代谢物,其中邻苯二甲酸二丁酯和棕榈酸为完全分布类型,其他代谢物为不完全分布类型;同时接种FJAT-91和FJAT-1458处理96 h的番茄检测代物种类最多为15种,处理6 h最少8种,邻苯二甲酸二丁酯和棕榈酸为完全分布类型,其他代谢物为不完全分布类型;对照处理的番茄96、72 h均检测到15种代谢物,处理6、24 h均检测到5种代谢物。
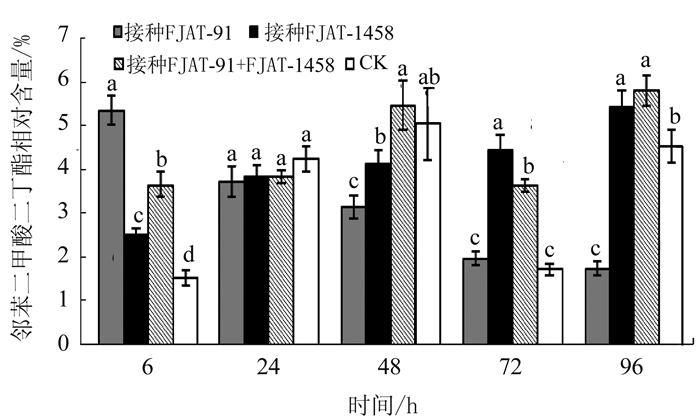
邻苯二甲酸二丁酯在不同处理不同时间的所有样本中均检测到,在只接种FJAT-91处理6、24、48、72、96 h的番茄植株中,相对含量分别为5.35%、3.72%、3.14%、1.98%、1.74%;邻苯二甲酸二丁酯在只接种FJAT-1458处理6、24、48、72、96 h的相对含量分别为2.53%、3.84%、4.13%、4.45%、5.45%;在同时接种FJAT-91和FJAT-1458处理6、24、48、72、96 h番茄中的相对含量分别为3.66%、3.84%、5.47%、3.64%、5.81%;在清水对照中6、24、48、72、96 h的相对含量分别为1.52%、4.25%、5.05%、1.73%、4.53%。该物质在不同处理不同时间样本(处理24 h除外)中的分布量均达显著水平(P<0.05)(图 1)。
![]() 图 1 邻苯二甲酸二丁酯在不同处理不同时间番茄中的相对含量注:图中数据为平均数±标准差,不同字母表示同一时间不同处理之间差异达显著水平(P<0.05),图 2同。Figure 1. Dibutyl phthalate in tomato plants induced by treatments with varied durations
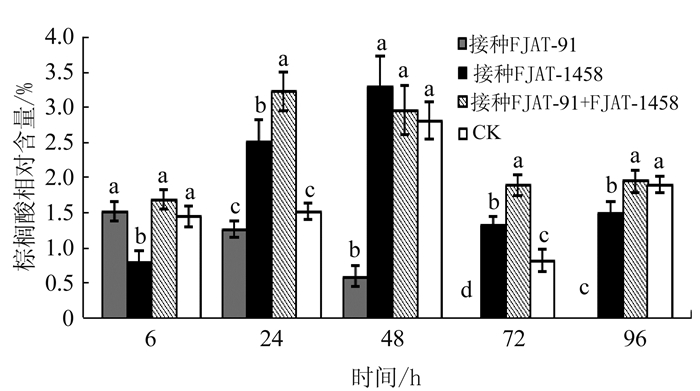
图 1 邻苯二甲酸二丁酯在不同处理不同时间番茄中的相对含量注:图中数据为平均数±标准差,不同字母表示同一时间不同处理之间差异达显著水平(P<0.05),图 2同。Figure 1. Dibutyl phthalate in tomato plants induced by treatments with varied durations棕榈酸在只接种FJAT-1458、同时接种FJAT-1458和FJAT-91及对照处理不同时间的番茄植株中均保持一定的分布数量,在只接种FJAT-91的番茄植株中,48 h后分布量低,显著低于其他3种处理(P<0.05),72 h后未检测到,说明FJAT-91可能诱导番茄植株棕榈酸的消亡(图 2)。
2.3 不同处理番茄代谢谱变化分析
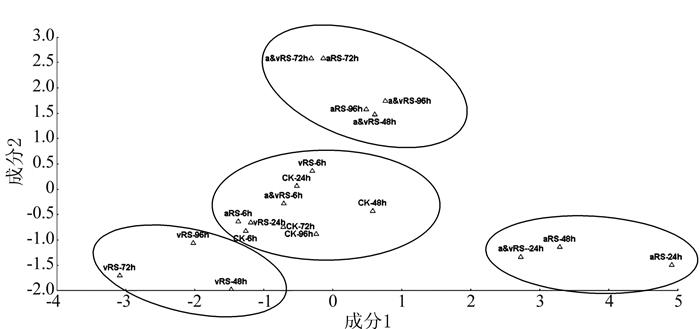
主成分分析(Principal component analysis,PCA)是将高维数据降维,投影变换到变异最大的主轴上,从而提取出数据集的特性,有效解决了样本变量较多情况下利用肉眼分析Loading图可靠性差的问题[14]。将不同处理的番茄代谢物相对含量数据组成数据矩阵,用DPS软件的因子分析程序对数据进行标准化处理后进行主成分分析(PCA)。选取2个主成分绘制成主成分二维谱图(图 3)。PCA分析结果表明,不同处理的样本被分成4组,不同处理接种番茄植株6 h的样本与对照组处理在同一组,且在主成分一和二的坐标零点附近,说明各处理接种初期(6 h)未诱导番茄植株代谢产物的变化。致病性菌株FJAT-91接种48、72、96 h的样本归在同一组,且与主成分一和主成分二均呈负相关。无致病力菌株FJAT-1458接种72、96 h及同时接种菌株FJAT-1458和FJAT-91的48、72、96 h的样本在同一组,与主成分一和主成分二均呈正相关。菌株FJAT-1458接种24、48 h及同时接种菌株FJAT-1458和FJAT-91的24 h的样本归在同组,与主成分一成正相关,与主成分二成负相关。
3. 讨论与结论
代谢物是生物体生理调控过程的终产物,其种类和数量变化反映了生物系统对基因或环境变化的最终响应[7]。本研究以GC-MS联用技术为平台,通过多元统计分析等手段探索了不同致病性青枯雷尔氏菌诱导番茄植株代谢谱的变化。结果表明,不同处理诱导番茄代谢产物变化主要表现在棕榈酸和邻苯二甲酸二丁酯含量的变化。青枯雷尔氏菌强致病力菌株FJAT-91诱导番茄植株棕榈酸的消亡,而无致病力菌株FJAT-1458处理及对照处理的番茄植株棕榈酸维持一定的含量,推测棕榈酸在无致病力青枯雷尔氏菌诱导番茄免疫抗病反应中起重要作用,此结果与尹玉玲等[15]的研究结果相吻合。尹玉玲等的研究结果表明棕榈酸和豆蔻酸与根系土壤黄萎病菌的分布数量呈显著负相关。张恩平等[16]研究表明,高浓度的邻苯二甲酸二丁酯会导致土壤生态系统退化,土壤有效养分利用率下降。本研究不同处理不同时间样本中均检测到邻苯二甲酸二丁酯,说明该物质可能是番茄一种自毒物质,今后利用无致病力青枯雷尔氏菌防治番茄青枯病时,也可以利用邻苯二甲酸二丁酯为检测指标,分析其对土壤肥力的影响。
主成分分析是一个无监督数据降维方法,可用来考察样品的分组情况[17],其对应的载荷图可以用来识别对分组有较大贡献的代谢物[18]。本研究对不同处理不同时间的番茄代谢物进行主成分分析,结果表明,只接种FJAT-1458处理或只接种FJAT-91或同时接种FJAT-1458和FJAT-91处理6 h样本与对照组处理不同时间样本聚在同一区,且在原点附近,说明各不同处理初期(6 h)未能诱导番茄代谢产物发生明显变化。强致病力菌株FJAT-91处理进程中各样本划分在同一区,说明其诱导的番茄代谢产物变化相似。无致病力菌株FJAT-1458处理和同时接种FJAT-1458和FJAT-91处理的样本,随着接种进程分别划在2个区,表明这2种处理诱导的番茄代谢产物变化相似。
不同植物的初生代谢物差异并不大,但因组织器官或生长发育状态的多样性,对代谢组学研究方法提出了很高的要求,样品的前处理和制备往往会因物种而异。因此,建立一套重复性好、分离效果好的代谢物测定方法是成功开展并深入研究代谢组学的必要步骤。本研究采用GC-MS技术对所收集的样本进行代谢物测定分析,样本处理方法相对简单,已有许多文献报道[19-20],且有很好分离效率,但需要对样本进行衍生化处理,这一步骤可能会引起样本的变化,因此,需要制定实验操作标准。
-
图 1 邻苯二甲酸二丁酯在不同处理不同时间番茄中的相对含量
注:图中数据为平均数±标准差,不同字母表示同一时间不同处理之间差异达显著水平(P<0.05),图 2同。
Figure 1. Dibutyl phthalate in tomato plants induced by treatments with varied durations
表 1 不同接种处理下番茄代谢产物的种类和数量
Table 1 Types and numbers of detected compounds under different treatments
处理 化合物类型 化合物种类数目/种 6 h 24 h 48 h 72 h 96 h 只接种FJAT-91 醇类 ND 2 1 3 2 酯类 1 1 3 1 1 酸类 2 2 3 ND ND 醛类 ND ND ND ND ND 哌啶类 ND ND ND 1 1 烷烃类 2 2 1 1 2 只接种FJAT-1458 醇类 1 2 ND 1 2 酯类 1 4 3 2 1 酸类 1 2 7 1 2 醛类 ND ND 1 1 1 哌啶类 ND ND 1 1 1 烷烃类 3 2 1 1 3 同时接种FJAT-91和FJAT-1458 醇类 2 1 ND 4 2 酯类 1 4 2 3 5 酸类 1 2 3 2 2 醛类 ND 1 1 1 1 哌啶类 1 ND 1 ND 2 烷烃类 2 2 3 1 3 清水对照 醇类 1 ND ND 2 1 酯类 1 1 2 4 1 酸类 1 1 2 2 1 醛类 ND ND 2 1 1 哌啶类 ND ND 1 1 1 烷烃类 2 2 2 1 3 注:ND表示未检测到该类化合物。 -
[1] ALLEN C, PRIOR P, HAYWARD A C. Bacterial wilt disease and the Ralstonia solanacearum species complex[M]. Saint Paul:American Phytopathological Society (APS Press), 2005.
[2] VAMITHA S C, NIRANJANA S R, UMESHA S. Role of phenylalanine ammonia lyase and polyphenol oxidase in host resistance to bacterial wilt of tomato[J]. Journal of Phytopathology, 2009, 157(9):552-557. DOI: 10.1111/jph.2009.157.issue-9
[3] JACOBS M J, BABUJEE L, MENG F, et al. The In Planta transcriptome of Ralstonia solanacearum:conserved physiological and virulence strategies during bacterial wilt of tomato[J]. American Society for Microbiology, 2012, 3(4):1-11. http://www.ncbi.nlm.nih.gov/pubmed/22807564
[4] 郑雪芳, 刘波, 林乃铨, 等.青枯雷尔氏菌无致病力突变菌株的构建及其防效评价模型分析[J].植物病理学报, 2013, 43(5):518-531. http://www.cnki.com.cn/Article/CJFDTOTAL-ZWBL201305010.htm [5] 许国旺, 杨军.代谢组学及其研究进展[J].色谱, 2003, 21(4):316-320. http://youxian.cnki.com.cn/yxdetail.aspx?filename=ZYHS201710009&dbname=CJFDPREP [6] 刘峥颢, 赵志磊, 夏立娅.市场中食品添加剂明胶及添加明胶的食品中铬含量本底调查[J].食品科技, 2010, 35(2):224-227. http://www.cnki.com.cn/Article/CJFDTOTAL-SSPJ201002063.htm [7] FIEHN O. Metabolic networks of Cucurbita maxima phloem[J]. Phytochemistry, 2002, 62(6):875-886. http://www.ncbi.nlm.nih.gov/pubmed/12590115
[8] 周宝利, 尹玉玲, 李云鹏.嫁接茄根系分泌物与抗黄萎病的关系及组分分析[J].生态学报, 2010, 30(11):3073-3079. http://www.cnki.com.cn/Article/CJFDTOTAL-STXB201011032.htm [9] DETTMER K, ARONOV P A, HAMMOCK B D. Mass spectrometry-based metabolomics[J]. Mass Spectrometry Reviews, 2007, 26(1):51-78. DOI: 10.1002/(ISSN)1098-2787
[10] DUNN W B, ELLIS D I. Metabolomics:current analytical platforms and methodologies[J]. TrACL:Trends Analytical Chemistry, 2005, 24(4):285-294. DOI: 10.1016/j.trac.2004.11.021
[11] GLINSKI M, WECKWERTH W. The role of mass spectrometry in plant systems biology[J]. Mass Spectrometry Reviews, 2006, 25(2):173-214. DOI: 10.1002/(ISSN)1098-2787
[12] JAN L, NICOLAS S, JOACHIM K, et al. Gas chro-matogramphy mass spectrometry-based metabolite profiling in plants[J]. Nature Protocols, 2006, 1(1):387-396. DOI: 10.1038/nprot.2006.59
[13] MAJOR H J, WILLIAMS R, WILSON A J, et al. A meta-bonomic analysis of plasma from Zucker rat strains using gas chromatography/mass spectrometry and pattern recognition[J]. Mass Spectrometry, 2006, 20(22):3295-3302. http://www.ncbi.nlm.nih.gov/pubmed/17044115
[14] ERIKSSONN L, ANTTI H, GOTTFRIES J, et al. Using chemometrics for navigating in the large data sets of genomics, proteomics, and metabonomics (gpm)[J]. Analytical and Bioanalytical chemistry, 2004, 380(3):419-429. DOI: 10.1007/s00216-004-2783-y
[15] 尹玉玲, 刘圆, 汤泳萍, 等.豆蔻酸和棕榈酸诱导茄子根系拮抗菌与黄萎菌数量消长的关系[J].生态学报, 2015, 35(20):6728-6733. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=stxb201520018&dbname=CJFD&dbcode=CJFQ [16] 张恩平, 衣宁宁, 李亮亮.番茄自毒物质对土壤养分的影响[J].西北农业学报, 2010, 23(3):820-823. http://www.cnki.com.cn/Article/CJFDTOTAL-XNYX201003046.htm [17] BAILEY N J, OVEN M, HOLMES E, et al. Metabolomic analysis of the consequences of cadmium exposure in Silene cucubalus cell cultures via 1H NMR spectroscopy and chemometrics[J]. Phytochemistry, 2003, 62(6):851-858. DOI: 10.1016/S0031-9422(02)00719-7
[18] PSIHOGIOS N G, KALAITZIDIS R G, DIMOU S, et al. Evaluation of tubulointerstitial lesions' severity in patients with glomerulonephritides:an NMR-based metabonomic study[J]. Journal of Proteome Research, 2007, 6(9):3760-3770. DOI: 10.1021/pr070172w
[19] WECKWERTH W, FIEHN O. Can we discover novel pathways using metabolomic analysis[J]. Current Opinion in Biotechnology, 2002, 13(2):156-160. DOI: 10.1016/S0958-1669(02)00299-9
[20] 段礼新, 漆小泉.基于GC-MS的植物代谢组学研究[J].生命科学, 2015, 27(8):971-977. http://www.cnki.com.cn/Article/CJFDTOTAL-SMKX201508002.htm -
期刊类型引用(1)
1. 阳妮,玛依拉·玉素音,杨延龙,李春平,张大伟,徐海江,赖成霞. 黄萎病枯斑型与黄化型病症棉花叶片的植物挥发物对比. 新疆农业科学. 2023(08): 1975-1986 .  百度学术
百度学术
其他类型引用(3)




 下载:
下载: