Effect of Drought Stress on Physiology of Camellia nitidissima Saplings
-
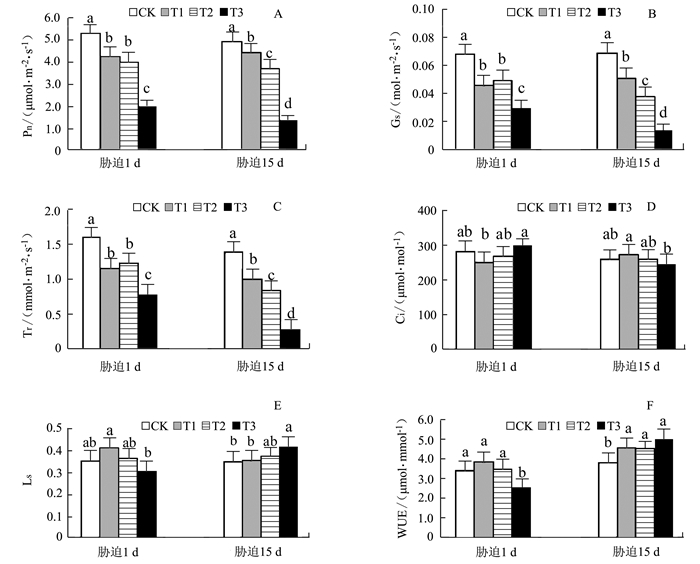
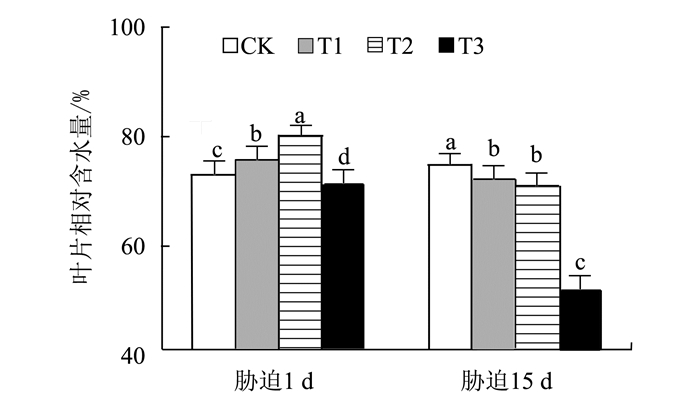
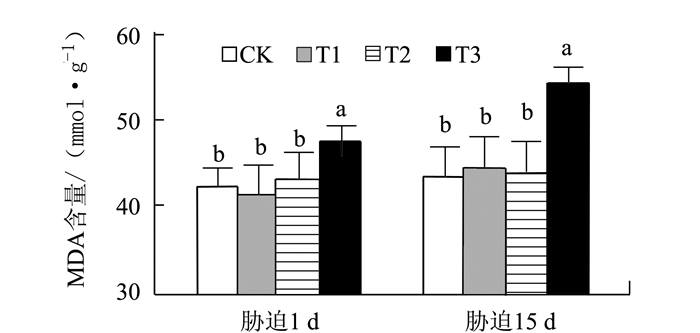
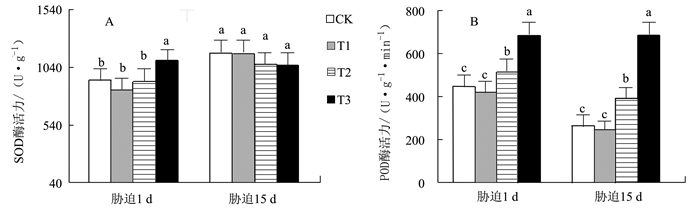
摘要: 以盆栽控水法对3年生金花茶幼树进行干旱胁迫,研究金花茶幼树各项生理指标的变化,结果表明:(1)轻度干旱胁迫即能引起金花茶叶片净光合速率(Pn)的下降,但土壤相对含水量降至20%并时未对3年生金花茶幼树成熟功能叶的光合系统造成不可逆的损伤;(2)轻、中度胁迫下,3年生金花茶幼树叶片相对含水量(LRWC)仅小幅降低,丙二醛(MDA)、叶绿素(Chl)、叶绿素a/b(Chl a/b)、可溶性糖(SS)含量和超氧化物歧化酶(SOD)活性与CK相比无显著差异,过氧化物酶(POD)活性在中度胁迫时较CK显著提高,类胡萝卜素(Car)含量在轻度胁迫15 d时较CK显著提高,脯氨酸(Pro)含量在胁迫初期较CK显著提高,可溶性蛋白(SP)在轻度胁迫15 d时较CK显著提高;(3)重度胁迫下,3年生金花茶幼树叶片除Car以外的各项生理指标均较CK有显著变化。说明轻、中度干旱(土壤相对含水量40%~65%)对金花茶幼树成熟叶的生理影响较小,重度干旱(土壤相对含水量20%~25%)对金花茶幼树成熟叶的各项生理指标影响较大。因此,在金花茶幼树栽培中应制定合理的水分管理措施,当土壤相对含水量低于25%时应及时补充水分,避免持续重度干旱造成严重影响。Abstract: Potted 3-year-old saplings of Camellia nitidissima Chi were grown under drought stress to monitor the physiological responses of the plants. The results showed that (1)mild drought could lower the net photosynthetic rate (Pn), but a relative water content in soil as low as 20% would not irreversibly damage the photosynthetic function of a 3-year-old C. nitidissima; (2) under a mild or moderate drought condition, the leaf relative water content (LRWC) of the saplings would decline slightly, while the contents of malondialdehyde (MDA), chlorophyll (chl)and soluble sugars (SS) as well as the activity of superoxide dismutase (SOD) would not differ significantly from those of CK; (3) under moderate stress, the peroxidase (POD) activity, carotenoid (Car) content after 15 d of exposure, proline (Pro) at beginning, andsoluble protein (SP) after 15 d were all significantly elevated as compared to CK; and under severe drought, all physiological indicators except Car content were altered significantly. It appeared that mild or moderate drought (when the soil relative water content was reduced to 65% or 40%) indeed affected the physiology of the saplings, but only severe drought (when the soil relative water content became as low as 20%-25%) would permanently change it. Therefore, whenever the water level in soilwas below 25%, appropriate water management and timelywatering could sufficiently avert any serious damages that might incur to the saplings by draught.
-
Keywords:
- Camellia nitidissima Chi /
- saplings /
- drought stress /
- physiology
-
Cd是对生物体具有高度毒性的重金属元素,其中菜园土壤受Cd污染的问题日益严重。因Cd可在土壤中长期滞留,极易被蔬菜等作物吸收,一方面造成重金属胁迫逆境,影响作物产量和品质,另一方面造成Cd超标,危害人体健康。丛枝菌根Arbuscular mycorrhiza,AM真菌广泛存在于土壤中,可与宿主植物根系形成良好的共生关系,对促进植物生长和提高植物抗逆性均有重要作用。相关报道显示,黄瓜、番茄等蔬菜接种AM真菌后,对于盐胁迫[1]、低温胁迫[2]、Co胁迫[3]及As胁迫[4]的抗性增强;同时AM真菌也是目前应对土壤重金属污染的微生物修复剂的主要成分,对于缓解重金属胁迫伤害以及改善重金属土壤环境具有重要意义。
本试验以黄瓜为试材,采用基质栽培方式,以富含AM真菌的育苗基质进行育苗,研究受AM真菌侵染的黄瓜幼苗在Cd胁迫条件下的生长、叶片光合参数、叶绿素荧光以及活性氧代谢相关酶活性的变化,可对缓解重金属对蔬菜的危害、提高蔬菜产量及品质以及菌根基质的开发提供实践依据。
1. 材料和方法
1.1 试验材料
试验于2015年5月至2016年2月在河北农业大学农林教学基地内进行。供试品种为黄瓜“津优一号”,由天津黄瓜所提供。菌根基质购自江苏柴米河公司;进行生理指标测定的药剂均为分析纯试剂。
1.2 试验设计
选用50孔穴盘,分别采用普通育苗基质和富含AM真菌混合菌剂的育苗基质进行黄瓜幼苗的培养,播种30d后将已被AM真菌侵染的黄瓜幼苗定植于基质栽培槽中,栽培基质采用蛭石。试验设计如下:(1) CK:正常栽培,不添加Cd2+;(2) Cd1:定植普通基质育苗的黄瓜幼苗,栽培槽内Cd2+添加浓度为0.2 mmol·L-1;(3) Cd1+AM:定植菌根基质育苗的黄瓜幼苗,Cd2+添加浓度为0.2 mmol·L-1;(4) Cd2:定植普通基质育苗的黄瓜幼苗,栽培槽内Cd2+添加浓度为0.4 mmol·L-1;(5) Cd2+AM:定植菌根基质育苗的黄瓜幼苗,Cd2+添加浓度为0.4 mmol·L-1。
每处理定植40株,于定植后第30 d测定下列指标,重复3次。
1.3 指标测定
1.3.1 生长指标的测定
用直尺测定主枝高度作为株高;用数显游标卡尺测定茎基部2 cm处直径作为茎粗;用AM-350便携式叶面积仪测定顶数第二片叶的叶面积;采用TTC法测定根系活力[5]。整株取出幼苗,用去离子水清洗后吸干水分,从根茎部位剪开幼苗,用分析天平称量幼苗地下部和地上部鲜重;80℃烘干24 h后用分析天平称量干重;根冠比采用公式计算:地下部干重/地上部干重。
1.3.2 光合参数及叶绿素荧光参数的测定
采用便携式光合速率测定仪(L-iCor6400型, 美国L-iCor公司)测定生长点下第2片展开叶的净光合速率(Pn)、气孔导度(Gs)、胞间二氧化碳浓度(Ci)、蒸腾速率(Tr)[6]。采用Mini-Imaging-PAM调制叶绿素荧光成像系统(德国,WALZ公司)测定PSⅡ最大光化学效率(Fv/Fm)、光合电子传递速率(ETR)、PSⅡ实际量子效率(фPSII)、光化学猝灭系数(qP)、非光化学猝灭系数(NPQ)。测定条件参照罗黄颖等[7]方法。采用叶绿素测定仪(SPAD-502,美国)进行叶色指数测定。
1.3.3 抗氧化酶活性测定
超氧化物歧化酶(SOD)活性测定参考Giannopolitis等[8]测定;过氧化物酶(POD)活性测定采用曾韶西等[8]方法;过氧化氢酶(CAT)活性测定采用Dhindsa等[9]方法。
1.3.4 超氧阴离子(O⋅_2)产生速率和H2O2含量测定
O⋅_2产生速率测定采用王爱国[10]等的方法。
1.3.5 丙二醛(MDA)含量的测定
丙二醛(MDA)含量测定采用Heath[11]的方法。
1.4 统计分析
使用Microsoft Excel软件对数据进行处理,采用SAS 8.1软件Duncan多重比较法(α=0.05)进行方差分析。
2. 结果与分析
2.1 丛枝菌根对Cd胁迫下黄瓜幼苗生长的影响
由表 1可知,与对照相比,黄瓜幼苗在2个浓度的Cd胁迫下均表现为生长指标的显著下降,各指标出现随Cd浓度上升而下降的现象。经菌根基质育苗后的黄瓜苗根系活力较Cd胁迫处理均显著提高,同时Cd1+AM处理的叶面积也显著提高。对比菌根基质育苗对2个浓度Cd胁迫处理的效果,可以看出虽然Cd1+AM处理和Cd2+AM处理的各生长指标均较胁迫处理有一定提高,但受菌根侵染的幼苗对于较低浓度(0.2 mmol·L-1)的Cd胁迫的缓解作用更好,对于各指标的提高优于对较高浓度(0.4 mmol·L-1)的Cd胁迫处理的效果。
表 1 丛枝菌根基质对Cd胁迫下黄瓜幼苗生长的影响Table 1. Effect of substrates inoculated with arbuscular mycorrhizal on the growth of cumcuber seedling under Cadmium stress处理 株高/cm 茎粗/cm 叶面积/cm2 根系活力/
(μg·g-1·h-1)CK 65.52±2.92a 1.08±0.02a 47.22±1.55a 186.25±4.50a Cd1 52.46±0.90b 0.92±0.01b 39.26±0.74c 119.63±8.93c Cd1+AM 56.81±0.60b 0.95±0.01b 43.46±0.40b 151.79±4.42b Cd2 49.63±0.99b 0.89±0.11b 35.59±0.82b 117.11±6.78c Cd2+ AM 52.84±0.29b 0.92±0.01b 37.92±0.96b 141.43±3.47b 注:同列数据后不同小写字母表示差异达显著(P < 0.05)水平。表 2~5同。 2.2 丛枝菌根对Cd胁迫下黄瓜幼苗生长量的影响
从表 2可以看出,2个浓度的Cd胁迫下的黄瓜幼苗地上和地下干鲜重均显著低于对照处理,且0.2 mmol·L-1的Cd胁迫处理各指标均高于0.4 mmol·L-1处理。菌根基质育苗显著提高了0.2 mmol·L-1的Cd胁迫处理的黄瓜幼苗地上和地下干鲜重;同时显著提高了0.4 mmol·L-1的Cd胁迫处理的黄瓜幼苗地上鲜重和地下干鲜重。同时,菌根基质育苗处理均提高了黄瓜幼苗的根冠比。说明,AM菌根通过促进植株生长,提高幼苗的生长量,来应对Cd胁迫,但其对于较低浓度(0.2 mmol·L-1)的Cd胁迫作用更好。
表 2 丛枝菌根基质对Cd胁迫下黄瓜幼苗生长量的影响Table 2. Effect of substrate inoculated with arbuscular mycorrhizal on growth of cucumber seedlings under Cd-stress处理 地上部鲜重
/g地上部干重
/g地下部鲜重
/g地下部干重
/g根冠比 CK 96.38±1.86a 8.07±0.15a 10.18±0.17a 0.93±0.03a 0.115±0.0004a Cd1 81.56±3.16b 7.10±0.08c 8.06±0.09c 0.75±0.02c 0.106±0.0006c Cd1+ AM 91.33±0.65a 7.59±0.15b 8.75±0.17b 0.83±0.01b 0.109±0.0007b Cd2 73.96±1.11c 6.87±0.10b 7.16±0.09c 0.63±0.02c 0.092±0.0086b Cd2+ AM 81.66±0.48b 7.33±0.05b 8.03±0.05b 0.73±0.02b 0.010±0.0008ab 2.3 丛枝菌根对Cd胁迫下黄瓜幼苗光合作用的影响
如表 3所示,黄瓜幼苗叶片经Cd胁迫处理的后Pn、Gs、Tr显著降低,而Ci则显著上升。菌根基质育苗的幼苗则表现为显著提高了0.2 mmol·L-1的Cd胁迫处理的黄瓜幼苗叶片Tr指标,并显著降低了Ci,Pn、Gs也有了一定提高。菌根处理对于0.4 mmol·L-1的Cd胁迫处理的黄瓜幼苗叶片光合参数的改善效果优于对于0.2 mmol·L-1的Cd胁迫处理的效果,表现为Pn、Gs、Tr显著提高,而Ci显著下降。说明菌根处理可有效缓解Cd胁迫对于黄瓜叶片光合作用的抑制。
表 3 丛枝菌根基质对Cd胁迫下黄瓜幼苗光合参数的影响Table 3. Effect of substrates inoculated with arbuscular mycorrhizal on photosynthetic parameters in leaves of cumcuber seedling under Cadmium stress处理 净光合速率Pn
/(μmol·m-2·s-1)气孔导度Gs
/(μmol·m-2·s-1)蒸腾速率Tr
/(mmol·m-2·s-1)胞间CO2浓度Ci
/(μL·L-1)CK 14.91±0.34a 0.194±0.004a 8.250±0.22a 237.75±7.70c Cd1 12.19±0.18b 0.176±0.003b 5.460±0.29c 307.57±7.11a Cd1+ AM 13.20±0.34b 0.186±0.003ab 6.903±0.08b 269.13±6.28b Cd2 10.89±0.08c 0.167±0.003c 5.037±0.47c 336.29±3.91a Cd2+ AM 12.49±0.27b 0.180±0.001b 6.373±0.26b 276.51±1.44b 2.4 丛枝菌根对Cd胁迫下黄瓜幼苗叶绿素荧光参数的影响
与对照相比,Cd胁迫使叶片叶色指数和叶绿素荧光参数均发生显著变化,其中叶色指数显著降低,同时PSⅡ系统的活性也受到显著抑制,表现为Fv/Fm、ETR、qP、фPSⅡ的显著降低和NPQ的显著上升。菌根处理可显著提高Cd胁迫黄瓜叶片的Fv/Fm、ETR、qP、фPSⅡ及0.4 mmol·L-1的Cd胁迫处理的叶色指数。说明AM真菌可有效提高两个浓度Cd胁迫叶片的光合系统效率,从而减轻Cd胁迫对光合系统和细胞膜的伤害(表 4)。
表 4 丛枝菌根基质对Cd胁迫下黄瓜幼苗叶绿素荧光参数的影响Table 4. Effect of substrates inoculated with arbuscular mycorrhizal on chlorophyll fluorescence parameters in leaves of cumcuber seedling under Cadmium stress处理 叶色指数 PSⅡ的最大光
化学效率光合电子
传递速率PSⅡ实际
量子效率光化学
淬灭系数非光化学
淬灭系数CK 43.39±1.46a 0.824±0.004a 46.20±0.58a 0.583±0.010a 0.833±0.009a 0.247±0.009c Cd1 36.52±0.91b 0.779±0.009b 33.51±1.37c 0.473±0.050c 0.750±0.006c 0.343±0.009a Cd1+ AM 39.80±0.43b 0.805±0.002a 39.51±0.67b 0.530±0.006b 0.793±0.007b 0.283±0.009b Cd2 34.81±0.56c 0.750±0.009c 29.64±0.49c 0.417±0.009c 0.687±0.019c 0.400±0.015a Cd2+ AM 38.22±0.70b 0.789±0.006b 35.67±0.87b 0.487±0.012b 0.750±0.006b 0.343±0.007b 2.5 丛枝菌根对Cd胁迫下黄瓜幼苗叶片活性氧代谢的影响
如表 5所示,Cd胁迫处理的黄瓜幼苗叶片的抗氧化酶活性变化呈现两种趋势,SOD活性较对照显著降低,而POD、CAT活性显著提高;而MDA含量和O⋅_2产生速率也显著上升。2个浓度胁迫处理相比,随Cd添加浓度上升MDA含量和O⋅_2产生速率也上升。经菌根基质育苗后2个胁迫处理的叶片SOD、POD、CAT活性显著提高,并细胞内O⋅_2产生速率和MDA含量显著降低。说明菌根处理通过提高黄瓜叶片细胞内的抗氧化酶活性,降低细胞的活性氧含量,从而减轻Cd胁迫对于细胞的伤害。
表 5 丛枝菌根基质对Cd胁迫下黄瓜幼苗叶片活性氧代谢的影响Table 5. Effect of substrates inoculated with arbuscular mycorrhizal on metabolism of reactive oxygen species in leaves of cumcuber seedling under Cadmium stress处理 SOD
/(U·g-1FW)POD
/(U·g-1FW)CAT
/(U·g-1FW)O⋅_2
/(nmol·min-1 ·g-1 FW)MDA
/(μmol·g-1FW)CK 83.36±1.68b 208.29±4.29c 107.79±2.93c 0.70±0.01c 4.72±0.08b Cd1 51.71±4.85c 311.80±6.52b 146.79±4.40b 0.94±0.02a 6.52±0.37a Cd1+ AM 124.58±3.91a 367.80±11.17a 163.57±3.41a 0.83±0.02b 5.30±0.23b Cd2 44.95±1.83c 265.08±4.48b 139.04±1.84b 1.14±0.05a 7.45±0.32a Cd2+ AM 103.16±3.05a 301.44±1.53a 161.04±1.98a 0.89±0.01b 6.01±0.08b 3. 讨论与结论
近年来,随着工矿企业的粗放式增长,重金属已成为威胁耕地安全的污染源之一[12]。据统计,我国受重金属污染的耕地约10×106hm2, 占耕地总面积的8%以上,仅京津冀地区比例已超过10%[13]。而这种重金属积累不可降解,污染土壤的修复十分困难。因此,如何经济有效的修复重金属污染的土壤成为当前研究的热点。植物-微生物修复是近年来新兴的一种生物修复重金属污染土壤的手段,因其高效环保而被国内外学者广泛认可。大量研究表明,AM真菌侵染植物根系后可有效改善植物根际环境,影响植物对于重金属离子的吸收[14],增加植物对于重金属胁迫的适应性,达到缓解重金属胁迫伤害和修复重金属污染土壤的效果。因此,AM真菌在植物中的应用成为目前重金属胁迫研究以及修复污染土壤的常用手段之一。
黄瓜属我国栽培面积较广的蔬菜,根系抗性差,常作为多种逆境胁迫,尤其是重金属胁迫的研究材料。石爽等[15]以水培法研究了铅、砷污染对黄瓜种子萌发的影响,发现低浓度铅和砷溶液可促进种子的萌发和幼苗生长,高浓度则有抑制作用。Pb和NaCl复合胁迫对于黄瓜幼苗伤害机理的研究表明,叶片的叶绿素含量显著下降,而SOD、POD活性和MDA含量显著提高[16]。黄瓜水培条件下对于镉胁迫的响应表现为随胁迫时间延长,叶片光合作用及光合系统参数均显著下降[17]。本试验中采用基质栽培法,模拟重金属胁迫条件,在基质中添加了0.2 mmol·L-1和0.4 mmol·L-1两种浓度的Cd2+,比较了菌根育苗基质培育的幼苗和普通育苗基质培育的幼苗在Cd胁迫下的生长和生理特性。结果表明黄瓜幼苗生长、光合参数、叶绿素荧光参数和活性氧代谢指标均发生显著变化。Cd胁迫显著降低了黄瓜幼苗株高、茎粗、叶面积、根系活力、地上和地下干鲜重等生长指标,且表现为浓度效应,即较高浓度(0.4 mmol·L-1) Cd对于植株生长的抑制作用更明显。Verma等[18]认为Cd胁迫影响Fe的吸收,会引起植株Fe缺乏,且在高浓度镉处理中更明显,这可能也是Cd胁迫导致植物生长不良的原因之一。
黄瓜幼苗外观表现为生长不良现象的主要原因在于幼苗内部生理特性的变化。试验中发现Cd胁迫直接导致幼苗光合作用的减低和光合系统反应中心活性的下降。直接反映光合作用的指标,如Pn、Gs、Tr显著下降,而反映光合受抑制程度的Ci显著上升;表明光合系统受胁迫程度的Fv/Fm、ETR、фPSII等指标均显著下降,而NPQ较对照显著上升,说明Cd胁迫通过降低PSII系统的光化学效率,抑制光合系统电子传递效率,增加了光合系统产量的非光散失,导致光合系统活性降低,光合效率下降,从而抑制了植株光合作用,最终导致植株生长的减缓。活性氧代谢是反映生物体受胁迫程度的另一重要指标,Cd胁迫处理的黄瓜幼苗叶片的SOD活性显著降低,而POD、CAT、MDA含量和O⋅_2产生速率则显著上升,且出现细胞活性氧含量随Cd浓度上升而增加的现象。这与石爽等[15]结果一致。主要原因为植物在逆境下启动自我保护反应,机体通过提高抗氧化酶活性而降低有害于细胞的活性氧含量,从而减轻自身在逆境中所受伤害。
蔬菜由于其栽培位置靠近市郊,是当前受重金属污染最严重的作物之一。现有丛枝菌根真菌对于植物重金属胁迫的缓解作用的报道,主要集中于大田作物或林木[19-23],而对于蔬菜的研究较少[3-4];且采用的多为实验室接种和外源添加的手段,尚未见应用商品化菌根育苗基质进行生产研究的报道。黄瓜等瓜类蔬菜,根系与AM真菌共生状态好,由于其需经育苗移栽且育苗期长达3~4周,因此,应用富含AM真菌的菌根基质育苗除简化试验程序外,还可在提高抗逆性的同时,促进幼苗生长。采用的菌根基质育苗可经育苗过程令AM菌株活化,直接侵染黄瓜幼苗根系,育苗过程与普通穴盘育苗无异,操作简单,成本低,接近生产实践,且便于推广应用。本试验中菌根基质培育的幼苗对于不同浓度Cd胁迫处理的耐受性好于普通基质培育的幼苗。表现为幼苗根系活力、叶面积和地下干鲜重的显著提高,叶片光合参数和叶绿素荧光参数的改善以及POD、CAT氧化酶等抗氧化酶活性提高。这与已有的对于其他作物的研究结果一致。但本试验结果还表明,菌根处理对于不同浓度Cd胁迫处理幼苗的生长和生理特性改善效果存在一定差异,虽然均表现为促进植株生长和优化各生理相关参数,但AM菌根对于较低浓度的Cd胁迫处理(0.2 mmol·L-1)黄瓜幼苗各项生长和生理指标的改善效果好于对于较高浓度的Cd胁迫处理(0.4 mmol·L-1)的效果,说明针对较高浓度的重金属胁迫,还需进一步调整AM菌根基质的菌种成分和比例,使之更适用于缓解较严重Cd胁迫伤害,更大限度发挥其生物修复重金属污染土壤的效果。
-
表 1 干旱胁迫下金花茶幼树光合色素含量
Table 1 Chlorophyll content of C. nitidissima saplings under drought stress
处理 胁迫1 d 胁迫15 d 叶绿素总量/(mg·L-1) 类胡萝卜素/(mg·L-1) 叶绿素a/叶绿素b 叶绿素总量/(mg·L-1) 类胡萝卜素/(mg·L-1) 叶绿素a/叶绿素b CK 3.59±0.35 b 0.35±0.01 a 1.95±0.09 a 3.40±0.26 b 0.37±0.02 b 2.12±0.04 a T1 3.47±0.07 b 0.36±0.01 a 2.05±0.02 a 3.67±0.18 b 0.41±0.01 a 1.97±0.07 a T2 3.40±0.15 b 0.35±0.01 a 2.09±0.05 a 3.74±0.03 b 0.39±0.01 ab 2.02±0.02 a T3 3.84±0.17 a 0.37±0.02 a 1.88±0.04 b 4.45±0.23 a 0.37±0.02 b 1.67±0.14 b 注:同列数据后不同小写字母表示差异显著(P<0.05)。 -
[1] 韦霄, 蒋运生, 韦记青, 等.珍稀濒危植物金花茶地理分布与生境调查研究[J].生态环境学报, 2007, 16(3):895-899. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=tryhj200703039 [2] 曹芬, 樊兰兰.金花茶研究进展[J].中国药业, 2013, 22(4):95-96. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zlzw201407019 [3] 陈永欣, 吕淑娟, 韦锦斌.金花茶化学成分和药理作用研究进展[J].广西中医药, 2013, 36(1):4-6. http://med.wanfangdata.com.cn/Paper/Detail/PeriodicalPaper_zcy201112045 [4] 郭建.金花茶等5种物品被批准为新资源食品[J].农产品加工, 2010, 1(6):39. http://www.cqvip.com/Main/Detail.aspx?id=34122035 [5] 黄付平.金花茶林下人工栽培试验初报[J].广西林业科学, 2001, 30(3):125-128. http://www.cqvip.com/QK/90684A/200103/5769907.html [6] 李建基, 廖国英, 黄霖.金花茶林下种植栽培技术要点[J].农村经济与科技, 2016, 27(20):41-42. DOI: 10.3969/j.issn.1007-7103.2016.20.029 [7] 林植.金花茶在阔叶林林下种植技术初探[J].花卉, 2015, 1(22):10-11. DOI: 10.3969/j.issn.1009-8496.2015.22.003 [8] 柴胜丰, 唐健民, 王满莲, 等.干旱胁迫对金花茶幼苗光合生理特性的影响[J].西北植物学报, 2015, 35(2):322-328. DOI: 10.7606/j.issn.1000-4025.2015.02.0322 [9] 杨期和, 李旭群, 杨和生, 等.金花茶幼苗光合生理生态特性研究[J].北京林业大学学报, 2010, 32(2):57-63. https://www.wenkuxiazai.com/doc/5c32c3d980eb6294dd886c2f.html [10] 邹琦.植物生理学实验指导[M].北京:中国农业出版社, 2003. [11] 王学奎.植物生理生化实验原理和技术[M].北京:高等教育出版社, 2006. [12] MOORE K. Measurement of lipid peroxidation[J]. Free Radical Research, 1998, 28(6):659. DOI: 10.3109/10715769809065821
[13] CHAVES M M, FLEXAS J, PINHEIRO C. Photosynthesis under drought and salt stress:regulation mechanisms from whole plant to cell[J]. Annals of Botany, 2009, 103(4):551. DOI: 10.1093/aob/mcn125
[14] PINHEIRO C, CHAVES M M. Photosynthesis and drought:can we make metabolic connections from available data?[J]. Journal of Experimental Botany, 2011, 62(3):869. DOI: 10.1093/jxb/erq340
[15] 周光良, 罗杰, 胡红玲, 等.干旱胁迫对巨桉幼树生长及光合特性的影响[J].生态与农村环境学报, 2015, 31(6):888-894. DOI: 10.11934/j.issn.1673-4831.2015.06.014 [16] 裴斌, 张光灿, 张淑勇, 等.土壤干旱胁迫对沙棘叶片光合作用和抗氧化酶活性的影响[J].生态学报, 2013, 33(5):1386-1396. http://www.cnki.com.cn/Article/CJFDTotal-STXB201305005.htm [17] 姬慧娟, 贾会霞, 章小铃, 等.干旱胁迫对红皮柳光合特性日变化及生长的影响[J].南京林业大学学报(自然科学版), 2016, 40(6):41-46. http://www.cnki.com.cn/Article/CJFDTotal-LYKJ201306003.htm [18] FARQUHAR G D, SHARKEY T D. Stomatal conductance and photosynthesis[J].Annu Rev Plant Physiol, 1982, 33(1):317-345. DOI: 10.1146/annurev.pp.33.060182.001533
[19] 汪本福, 黄金鹏, 杨晓龙, 等.干旱胁迫抑制作物光合作用机理研究进展[J].湖北农业科学, 2014, 53(23):5628-5632. http://www.cnki.com.cn/Article/CJFDTotal-LYKE201511015.htm [20] 邓旭, 董晨, 张广明.干旱对两种金花茶幼苗抗氧化能力及渗透物质含量的影响[J].热带作物学报, 2012, 33(6):1034-1039. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=rdzwxb201206013 [21] 张雁霞, 李萍, 刘玉皎.西北地区蚕豆苗期干旱胁迫下表型差异性与抗旱性研究[J].东北农业大学学报, 2015, 46(9):30-37. http://cdmd.cnki.com.cn/Article/CDMD-10298-2008113038.htm [22] 朱教君, 康宏樟, 李智辉, 等.水分胁迫对不同年龄沙地樟子松幼苗存活与光合特性影响[J].生态学报, 2005, 25(10):2527-2533. DOI: 10.3321/j.issn:1000-0933.2005.10.010 [23] JUBANY-MARÍ T, MUNNÉ-BOSCH S, ALEGRE L. Redox regulation of water stress responses in field-grown plants. Role of hydrogen peroxide and ascorbate[J]. Plant Physiology & Biochemistry Ppb. 2010, 48(5):351. http://linkinghub.elsevier.com/retrieve/pii/S0981942810000276
[24] 邓仁菊, 卢扬, 曾宪浩, 等.持续干旱胁迫对青薯9号幼苗生长及生理特性的影响[J].西南农业学报, 2017, 30(2):291-295. http://www.cnki.com.cn/Article/CJFDTotal-ZJLK201503004.htm [25] WU S, HU C, TAN Q, et al. Effects of molybdenum on water utilization, antioxidative defense system and osmotic-adjustment ability in winter wheat (Triticum aestivum) under drought stress[J]. Plant Physiology and Biochemistry, 2014, 83:365-374. DOI: 10.1016/j.plaphy.2014.08.022
[26] 杨柳, 何正军, 赵文吉, 等.狭叶红景天幼苗对水分及遮阴的生长及生理生化响应[J].生态学报, 2017, 37(14):4706-4714. http://www.cnki.com.cn/Article/CJFDTOTAL-ZWSL200304011.htm [27] 季杨, 张新全, 彭燕, 等.干旱胁迫对鸭茅根、叶保护酶活性、渗透物质含量及膜质过氧化作用的影响[J].草业学报, 2014, 23(3):144-151. DOI: 10.11686/cyxb20140316 -
期刊类型引用(4)
1. 汪浩,张强,张文地,李思宇,黄健,朱安,刘立军. 腋芽萌发能力对再生稻产量影响的研究进展. 中国水稻科学. 2020(03): 205-216 .  百度学术
百度学术
2. 文明辉,武晓兰,肖夏萍,文新华,张卫,谷亚娟. 不同施氮量对再生稻产量的影响及相关性分析. 基层农技推广. 2019(07): 37-40 .  百度学术
百度学术
3. 杨飞翔,黄璜,陈灿,常培恩,欧林志. 稻鳖共作模式中的土壤养分动态变化及产量形成. 作物研究. 2019(05): 402-407 .  百度学术
百度学术
4. 陈元伟,陈其敏,徐小健,郑华斌,唐启源. 促芽肥对黄华占再生季农艺性状及产量的影响. 中国稻米. 2017(06): 90-92+96 .  百度学术
百度学术
其他类型引用(7)




 下载:
下载: