Cloning and Sequence Analysis of Myostatin(MSTN) Gene from Fujian White Rabbit
-
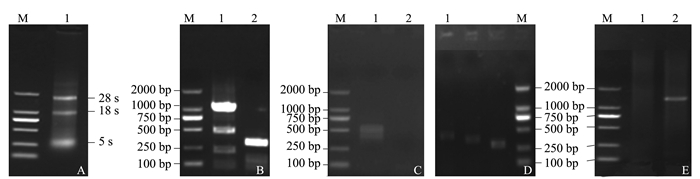
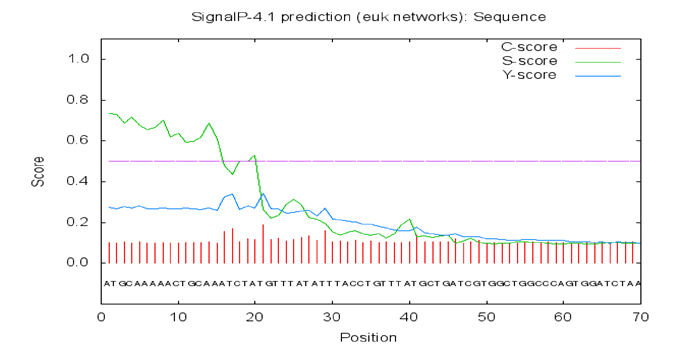
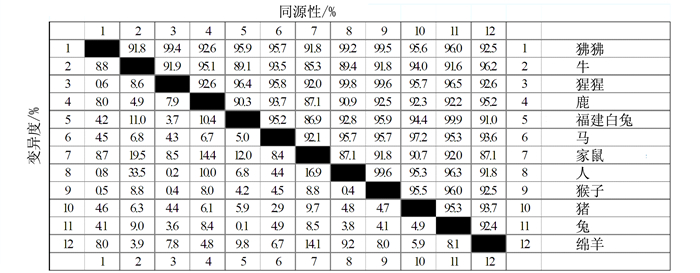
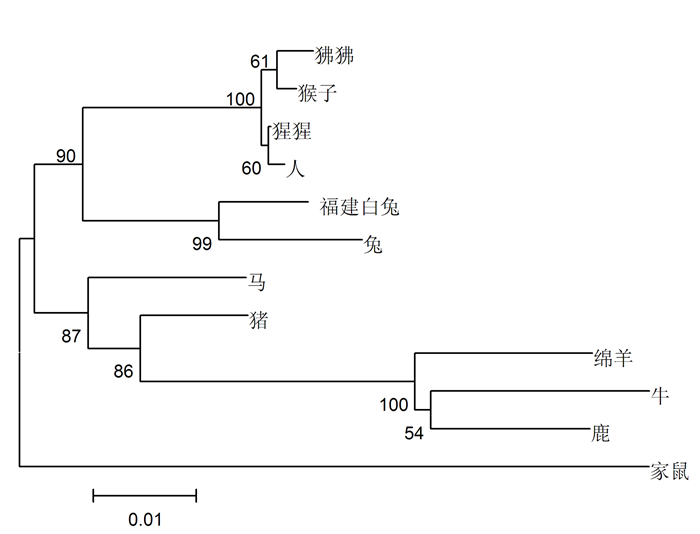
摘要: 为掌握福建白兔负向调控骨骼肌生长发育的肌肉生长抑制素(Myostatin,MSTN)基因分子基础,应用RT-PCR和RACE技术从肌肉组织总RNA中克隆出福建白兔MSTN基因的cDNA序列并进行分析。结果表明,该基因序列全长1 551 bp(GenBank登录号:KX084386),其中5'非翻译区136 bp,3'非翻译区287 bp,1 128 bp的开放阅读框,编码375个氨基酸,MSTN蛋白在第97~768核苷酸处编码的氨基酸存在1个TGF-β前肽超家族结构域,在第841~1 125核苷酸处编码的氨基酸存在1个TGF-β家族结构域。序列分析表明:福建白兔与穴兔、人、猪、家鼠、马、牛、绵羊、鹿、狒狒、猩猩、猴的MSTN核苷酸序列同源性分别为99.9%、92.8%、94.4%、86.9%、95.2%、89.1%、91.0%、90.3%、95.9%、96.4%、95.9%。研究结果为进一步开展福建白兔MSTN基因的结构、表达以及分子育种等相关研究提供了基础数据。Abstract: In order to master the molecular basis of Myostatin(MSTN) gene that negatively regulates skeletal muscle growth and development in Fujian white rabbit, Fujian white rabbit MSTN gene cDNA was amplified and cloned from total RNA of muscle by RT-PCR and RACE(rapid amplification of cDNA ends). Sequence analysis indicated that the full cDNA (1 551 bp, Gen Bank accession number:KX084386) consisted of a 5'-terminal untranslated region (UTR) (136 bp), a 3'-terminal UTR (287 bp) and an ORF(1 128 bp). The open reading frame encoded a deduced protein with 375 amino acids residues. There were one TGF-beta propeptide superfamily domains at amino acids encoded by the 97 to 768 nucleotides and one TGF-beta family domains at amino acids encoded by the 841 to 1 125 nucleotides. Comparison of Fujian white rabbit MSTN with those of other rabbit, human, pig, mouse, horse, cattle, sheep, deer, baboons, orangutan and monkey showed that the amino acids horno1ogy were 99.9%, 92.8%, 94.4%, 86.9%, 95.2%, 89.1%, 91.0%, 90.3%, 95.9%, 96.4%, 95.9%, respectively. It provides the basic data for further research on structure function, expression regulation and molecular breeding of MSTN gene in Fujian white rabbit.
-
Keywords:
- Fujian white rabbit /
- MSTN /
- clone /
- sequence analysis
-
0. 引言
【研究意义】烟草黑胫病(Tobacco Black Shank)是由烟草疫霉菌(Phytophthora nicotianae )引起的真菌性土传病害[1]。其病原菌为卵菌门(Oomycota),游动孢子从茎基部侵入烟株,然后扩散至维管束,导致烟株茎基部坏死甚至烟株死亡[2-3]。黑胫病在烟株各个生育期均能发生[4],一旦爆发流行,往往造成烟株大面积死亡,对烟草生产造成巨大经济损失,是严重制约烟草产业健康持续发展的严重病害[5]。土壤微生物是土壤生态系统的重要组成部分[6],参与植株与土壤环境之间养分循环,能量交换。黑胫病作为土传性真菌病害,烟株感染后势必会影响烟株根际土壤微生物群落的变化。【前人研究进展】近年来,随着土壤微生物研究的不断深入,根际土壤微生物与植物病害之间关系的研究亦引起了高度重视。烟株感病后,根际微生态细菌群落的功能会受到破坏,不利于维持种群平衡,易导致土传病害的发生[7],同时病原菌在易感病烟田中的相对丰度较高,不同发病程度烟株根际主要环境因子差异中,土壤酶活性受到不同程度抑制,细菌群落组成发生改变,土壤微生物多样性降低[8]。前人的研究着重于土壤理化性质、微生物数量的变化以及各种防治措施对烟草土传病害的影响[9],而通过调节烟田根际土壤微生态环境来抑制烟田土传病害的发生已成为研究的热点。【本研究切入点】健康与感染黑胫病烟株根际土壤细菌群落结构与多样性有待深入探讨。【拟解决的关键问题】通过Illumina MiSeq高通量测序技术分析健康烟株和感染黑胫病烟株根际土壤的细菌群落结构差异,探究黑胫病对烟株根际土壤细菌群落结构的影响,探讨根际土壤细菌对黑胫病的生态作用机理,以期为烟草黑胫病的生物防治提供理论基础。
1. 材料与方法
1.1 样品采集
2019年7月于云南省曲靖市宣威热水关营试验地进行样品采集,品种为云烟100。在烟株旺长期随机选取3株烟草黑胫病发病严重的烟株和3株健康烟株,去除烟株周围地表土壤,将烟株连根拔起,去除烟株根系主土壤,收集根须2 mm范围土壤根际土。健康烟株根际土(ZCTY)编号为H1、H2、H3;感染黑胫病烟株根际土(HJTY)编号为P1、P2、P3。去除根系及其他杂物,分装于50 mL离心管中带回实验室,置于−80 ℃中冷冻保存,待用。
1.2 样品DNA提取
参照PowerSoil® DNA土壤基因组DNA提取试剂盒,对健康烟株和感黑胫病烟株根际土壤进行DNA的提取,用1%琼脂糖凝胶电泳检测DNA的质量。用无菌水将DNA稀释至1 ng·μL−1作为模板,选用特异性引物338F(5′-ACTCCTACGGGAGGCAGCAG-3′)和806R(5′-GGACTACHVGGGTWTCTAAT-3′)扩增16S rRNA基因的V3~V4可变区,扩增程序为:预变性,95 ℃ 3 min;变性,95 ℃ 30 s,36个循环(退火,55 ℃ 30 s;延伸,72 ℃ 45 s)再延伸72 ℃ 10 min。扩增体系为 20 μL:4 μL 5×FastPfu 缓冲液;2 μL 2.5 mmol·L−1 dNTPs;0.8 μL Forward Primer (5 μmol·L−1);0.8 μL Reverse Primer (5 μmol·L−1);0.4 μL FastPfu 聚合酶;0.2 μL BSA;10 ng DNA 模板;加 ddH2O 至 20 μL。使用 2%琼脂糖凝胶回收 PCR 产物,利用 AxyPrep DNA Gel Extraction Kit (Axygen, USA) 试剂盒进一步纯化回收后,送上海美吉生物医药科技有限公司进行 MiSeq 测序。
1.3 下机数据的质控与分析
剔除下机数据中的标签及引物序列,进行序列拼接得到原始数据;使用Usearch 软件(Version 7.0)进行过滤、去嵌合体序列得到有效序列;利用Mothur软件(version v.1.30.1)绘制稀释度曲线,计算文库覆盖率、Chao1、ACE、Shannon、Simpson指数,对根际土壤微生物群落中的物种多样性和丰富度进行评价;利用Uparse软件在97%相似性水平上进行OTUs聚类分析;利用RDP classifier软件和SILVA数据库进行物种注释,使用Qiime软件进行主成分分析,并利用R语言进行绘图。
1.4 数据处理
采用Excel软件进行数据处理;采用SPSS 22.0数据处理系统进行统计分析,Duncan’s新复极差法进行数据的多重比较和分析。
2. 结果与分析
2.1 测序深度分析
稀释曲线(Rarefaction curve)既反映了不同测序数据量下各样品中的物种丰度,又可以表示测序深度是否覆盖了一个环境样品中的所有测序对象。由图1稀释曲线可知本次测序样品的曲线斜率逐渐变小,但最终未进入到平台期,表明随着序列数的不断增加,不会产生过多新的OTU数。说明此次测序结果能够较全面地反映根际土壤样品细菌群落与结构的真实情况。
2.2 细菌的OTU丰度与Alpha多样性
由图2可见,健康烟株根际土壤样本(ZCTY)与感染黑胫病烟株根际土壤样本(HJTY)共有和特有OTU所占比例。健康烟株根际土样和感染黑胫病烟株根际土样两组土壤样本中,共有OTUs数3182个。其中,健康烟株根际土样中特有OTU有1518个,占总OTU数的24.59%;感染黑胫病烟株根际土样中特有OTU有1471个,占总OTU数的23.84%;健康烟株根际土样中特有OTU丰度高于感染黑胫病烟株根际土样3%。
由表1可知ZCTY和HJTY的coverage值均在96%以上,说明样本序列的检测概率较高,能够较全面地反映样本土壤细菌群落的真实分布情况。在Alpha丰富度指标中ACE、Chao1数值越大说明生物丰度越高,HJTY的ACE、Chao1数值低于ZCTY数值21.29%、15.23%,表明感染黑胫病烟株的根际土壤细菌丰度低于健康烟株根际土壤。在Alpha多样性指标中Shannon数值越高,Simpson数值越低,表明样本生物多样性指数越高。ZCTY的Shannon数值高于HJTY数值3.05%,ZCTY的Simpson数值低于HJTY数值9.09%。表明健康烟株的根际土壤细菌多样性高于感染黑胫病的烟株。Alpha多样性指标表明感染黑胫病烟株根际土壤细菌丰度及多样性均低于健康烟株根际土壤。
表 1 健康与感染黑胫病烟株根际土壤微细菌多样性指数Table 1. Microbial diversity indices of rhizosphere soils at tobacco lots infected with black shank disease处理
Treatment丰富度指数
Richness index多样性指数
Diversity index覆盖率
Coverage/%ACE Chao1 Shannon Simpson HJTY 3741.63 3792.47 6.36 0.0048 97.14 ZCTY 4753.59 4473.79 6.56 0.0044 96.53 2.3 健康与感染黑胫病烟株根际土壤细菌组成分析
门水平样品菌落相对丰度堆积图(图3)表明:ZCTY中相对丰度大于1.00%的优势细菌门分类数量为9个:放线菌门(Actinobacteria,35.57%) >变形菌门(Proteobacteria,20.14%)>绿弯菌门(Chloroflflexi,15.40%)>酸杆菌门(Acidobacteria,11.72%)>芽单胞菌门(Gemmatimonadetes,5.77%)>粘球菌门(Myxococcota,2.65%)>厚壁菌门(Firmicutes,2.40%)>拟杆菌门(Bacteroidota,2.08%)>硝化螺旋菌门(Nitrospirae,1.14%);与HJTY优势细菌门分类组成比例存在一定差异,其中,绿弯菌门(Chloroflflexi)、芽单胞菌门(Gemmatimonadetes)、厚壁菌门(Firmicutes)、Methylomirabilota相对丰度有所增加,分别增加了6.04%、7.79%、34.17%、117.19%。HJTY中放线菌门(Actinobacteria)、变形菌门(Proteobacteria)、酸杆菌门(Acidobacteria)、粘球菌门(Myxococcota)、拟杆菌门(Bacteroidota)、硝化螺旋菌门(Nitrospirae)相对丰度分别减少0.73%、5.76%、3.50%、20.38%、59.13%、16.67%。
由图4可知,健康烟株土壤样本中,相对丰度大于4%优势菌属有Nocardioides (4.99%)、norank_f__norank_o__Vicinamibacterales(4.50%);感染黑胫病烟株根际土壤样本中相对丰度大于4%优势菌属有norank_f__norank_o__Gaiellales(5.39%)、norank_f__norank_o__Vicinamibacterales(4.71%)、norank_f__Gemmatimonadaceae(4.31) ;而在健康烟株根际土壤中为优势菌属的类诺卡氏菌属(Nocardioides, 4.99%),在感染黑胫病烟株中并未检测到。在感染黑胫病烟株根际土壤中Gaiella、节杆菌属(Arthrobacter)相对丰度分别下降5.52%、23.05%,且此二种菌属皆为放线菌纲。
图5热图上部样本层级聚类树表明,健康烟株根际土与感染黑胫病烟株根际土壤细菌群落结构与多样性存在差异。根据热图所示:P1、H1、H2聚为一类,H3、P2、P3聚为一类。其中发病烟株根际土样P1与其余样本间差异最大,与P2、P3的差异主要集中在类诺卡氏菌属(Nocardioides)、芽单胞菌属(Gemmatimonas)、norank_f__Xanthobacteraceae、慢生根瘤菌属(Bradyrhizobium)、天蓝色链霉菌属(Streptomyces)5个属。
在OTU水平上对健康烟株土壤样本和感染黑胫病烟株土壤样本进行PCoA 分析。结果如图6所示,PC1、PC2对样品差异的解释度分别为63.43%和17.73%,两者总计可解释全部土壤样品的71.16%,其中PC1是两处理产生差异的主要因素,从图中可以看出PC2能够将ZCTY和HJTY区分开,其中ZCTY样品主要分布在PC2的正值区域,而HJTY主要分布在负值区域,阐明ZCTY与HJTY微生物群落组成存在较大差异。
3. 讨论
高通量测序技术能够揭示土壤微生物群落结构的相关信息[10],而土壤微生物群落组成在一定程度上反映了土壤健康状况,当土壤中病原微生物大量生长,有益微生物数量减少时,常引起作物病害的发生[11]。土壤微生物群落变化是影响植物土传病害中最重要的因子[12,13],在控制植物土传病害中的重要性已经得到了研究人员的广泛认可。部分土壤微生物具有拮抗土壤病原菌的功能[14],对抑制病原体入侵或在根部组织间的二次传播具有重要作用。土壤细菌不仅能够快速、高效地分解与转化营养物质[15]、影响植物对养分的获取和土壤肥力,而且细菌群落结构的差异和变化规律能反映土壤现状及变化趋势,可用来指示土壤生态功能[16]。
测序结果表明,感染黑胫病烟株烟株根际土壤的Shannon、ACE和Chao1指数分别较健康植株降低了3.05%、21.29%、15.23%。烟株感染黑胫病后根际土壤中细菌群落的多样性及丰富度均有显著下降。在门水平上,感染黑胫病烟株与健康烟株根际土壤共同优势菌门为放线菌门、变形菌门、绿弯菌门、酸杆菌门、芽单胞菌门,此结果与向立刚等[17]健康与感染黑胫病烟株根际土壤与茎秆细菌群落结构与多样性,以及王秋君等[18]通过调节土壤细菌群落结构控制辣椒疫病与土壤细菌群落结构的研究结果相一致。其中放线菌门在健康与感染黑胫病烟株根际土壤中的相对丰度无明显差异。与健康烟株根际土壤相比,感染黑胫病烟株根际土壤中变形菌门和酸杆菌门相对丰度分别下降5.76%、3.50%;变形菌门和酸杆菌门对土壤生态系统的构建具有重要作用,二者均属于化能异养细菌[19],以土壤中的有机物质作为碳源和能源,其相对丰度的变化通常与土壤肥力水平的变化呈正相关[20,21]。绿弯菌门和芽单胞菌门相对丰度分别增长6.04%、7.79%,而绿弯菌门和芽单胞菌门都有很强的能力支持基本的生物过程,对于恶劣的环境的抗性较强,且绿弯菌门在酸化土壤中的相对丰度较高[22]。拟杆菌门、硝化螺旋菌门相对丰度从大于1%下降至1%以下。结果表明,烟株感染黑胫病后根际土壤细菌群落结构发生改变,暗示在生境恶劣的情况下寡营养细菌将代替部分富营养细菌维持土壤细菌的基本生态功能[23]。
属水平上,节杆菌属、Gaiella属在感染黑胫病土样中相对丰度均有所降低,而且此二种属均属于放线菌纲。本次研究与前人研究结果一致,但也存在差异,健康与感染黑胫病烟株根际土壤中属水平的差异还体现在类诺卡氏菌属、慢生根瘤菌属、天蓝色链霉菌属。类诺卡氏属在感染黑胫病烟株根际土壤中未检出,其在降解有机污染物在污染区域的生物修复中发挥重要作用,进一步说明烟株感染黑胫病会导致其根际土壤生态失衡,但类诺卡氏属对烟草疫霉是否存在相互作用及其作用机理有待进一步研究。
4. 结论
本研究通过高通量测序分析阐明了健康及感染黑胫病烟株根际土壤细菌群落结构及多样性的变化,为烟草黑胫病生物防治提供理论基础。此外,本研究为烟株感染黑胫病旺长期的调查分析,尚缺乏对烟株其他生育期细菌多样性的分析,有待进一步探讨。
-
表 1 设计的引物
Table 1 Primer sequence
名称 序列(5′-3′) 长度/(mers) F1(已知序列) GTTTATGCTGATCGTGGCTG 20 R1(已知序列) CACCCACAGCGGTCTACTAC 20 F2(已知序列) CTGTGTAATGCATGCACTTG 20 F3(3′RACE) AGCAGGTCCTTGCTGTACTC 20 F4(3′RACE) CCAATTACTGCTCTGGAGAC 20 F5(3′RACE) GAGCACTCAACAGAATCACG 20 R4(5′RACE) CTTCCAAAGAGCCATCACTG 20 R6(5′RACE) CTGAACGTCGTACTGATC 18 YZF1(序列验证) CTCAAGCTGTTCATGCAT 18 YZR1(序列验证) CCAACCATTGCATGTATTC 19 -
[1] MCPHERRON A C, LAWLER A M, LEE S J. Regulation of skeletal muscle mass by a new TGF-β superfamily member[J]. Nature, 1997, 387(6628):83-90. DOI: 10.1038/387083a0
[2] KAMBADUR R, SHARMA M, SMITH TP, et al. Mutations in myostatin (GDF8) in double-muscled Belgian Blue and Piedmontese cattle[J]. Genome Res, 1997, 7(9):910-916. DOI: 10.1101/gr.7.9.910
[3] SCHUELKE M, WAGNER K R, STOLX L E, et al. Myostatin mutation associated with gross muscle hypertrophy in a child[J]. N Engl J Med, 2004, 350(26):2682-2688. DOI: 10.1056/NEJMoa040933
[4] MCPHERRON A C, LEE S J.Suppression of body fat accumulation in myostatin deficient mice[J]. J Clin Invest, 2002, 109:595-601. DOI: 10.1172/JCI0213562
[5] ALEXANDRA C, McPHERRON, SE-JIN LEE. Double muscling in cattle due to mutations in the myostatin gene[J]. USA: Proc Natl Acad Sci, 1997, 94: 12457-12461.
[6] MARK THOMAS, BRETT LANGLEY. Myostatin, a negative regulator of muscle growth, function of inhibiting myoblast proliferation[J]. J Biol Chem, 2000, 275(51):40235-40243. DOI: 10.1074/jbc.M004356200
[7] RIOS R, CAMEIRO I. Myostatin is an inhibitor of myogenic differentiation[J]. Am J Physiol Cell Physiol, 2002, 282(5):993-999. DOI: 10.1152/ajpcell.00372.2001
[8] ALEXANDRA C, MCPHERRON A C. Suppression of body fat accumulation in myostatin-deficient mice[J]. J Clin Invest, 2002, 109(5):595-601 DOI: 10.1172/JCI0213562
[9] LIN J, ARNOLD H B, DELLA-FERA M A. Myostatin knockout in mice increases myogenesis and decreases adipogenesis[J]. Biochem Biophys Res Commun, 2002, 291(3):701-706. DOI: 10.1006/bbrc.2002.6500
[10] KOLLIAS H D, McDERMOTT C.Transforming growth factor-βand myostatin signaling in skeletal muscle[J]. J Appl Physiol, 2008, 104:579-587. DOI: 10.1152/japplphysiol.01091.2007
[11] KRIK S, OLKHAM J. Myostatin regulation during skeletal muscle regeneration[J]. J Cell Physiol, 2000, 184(3):356-363. DOI: 10.1002/(ISSN)1097-4652
[12] 李帅, 杨舒黎, 苟潇.肌肉生成抑制素(MSTN)基因研究进展[J].中国畜牧兽医, 2011, 38(2):60-63. http://d.old.wanfangdata.com.cn/Periodical/zgxmsy201102013 [13] HWANG W Y, FU Y, REYON D, et al. Efficialent genome editing in zebrafish using a CRISPR-CAS system[J]. Nat Biotechnol, 2013, 31(3):227-229. http://mbe.oxfordjournals.org/external-ref?access_num=23360964&link_type=MED
[14] 王伟, 连林生, 李继中.猪MSTN基因生物信息学分析[J].安徽农业科学2012, 40(10):5943-5945. DOI: 10.3969/j.issn.0517-6611.2012.10.083 [15] 吴清洪, 岳敏, 田雨光, 等.西藏小型猪MSTN基因分子克隆及序列分析[J].中国比较医学杂志, 2015, 25(3):18-22. DOI: 10.3969/j.issn.1671-7856.2015.03.005 [16] 王娇娇, 张世伟, 张丽君, 等.辽育白牛MSTN基因分子克隆及序列分析[J].现代畜牧兽医, 2016(10):21-27. DOI: 10.3969/j.issn.1672-9692.2016.10.004 [17] 张丽, 刘丽霞, 李强子, 等.天祝白牦牛MSTN基因编码区克隆及生物信息学分析[J].浙江农业学报, 2017, 29(4):618-624. DOI: 10.3969/j.issn.1004-1524.2017.04.15 [18] 梁春年, 丁学智, 包鹏甲, 等.牦牛MSTN基因分子克隆及序列分析[J].华北农学报, 2013, 28(1):76-81. DOI: 10.3969/j.issn.1000-7091.2013.01.015 [19] 金鑫燕.山羊肌生成抑制素(MSTN)基因的克隆及生物信息学分析[J].中国畜牧兽医, 2011, 38(9):11-114. http://d.old.wanfangdata.com.cn/Periodical/zgxmsy201109026 [20] JEANPLONG F, FALCONER S J, OLDHAM J M. et al.Discovery of a mammalian splice variant of myostatin that stimulates myogenesis[J]. PloS ONE, 2013, 8:e81713. DOI: 10.1371/journal.pone.0081713
[21] JAIN H, SINGH S, KADAM M, et al. Knockdown of the myostatin gene by RNA interference in caprine fibroblast cells[J]. J Biotechnol, 2010, 145(2):99-102. DOI: 10.1016/j.jbiotec.2009.10.017
[22] TRIPAT A K, RAMANI U V, PATEL A K, et al.short hairpin RNA-induced myostatin gene silencing in caprine myoblast cells in vitro[J]. Appl Biochem Biotechnol, 2013, 169:688-694. DOI: 10.1007/s12010-012-0021-1
[23] TANG D, ZHU H, WU J, et al.Silencing myostatin gene by RNAi in sheep embryos[J]. J Biotechnol, 2012, 158:69-74. DOI: 10.1016/j.jbiotec.2012.01.008
[24] TRIPATHI A K, APARNATHI M K, VYAVAHARE S S, et al.Myostatin gene silencing by RNA interference in chicken embryo fibroblast cells[J]. J Biotechnol, 2012, 160:140-145. DOI: 10.1016/j.jbiotec.2012.03.001
[25] HU S, NI W, SAI W, et al.Knockdown of myostatin expression by RNAi enhances muscle growth in transgenic sheep[J]. PloS ONE, 2013, 8(3):e58521. DOI: 10.1371/journal.pone.0058521
[26] ZHON Z R, ZHONG B S, JIA R X, et al.Production of myostatin-targeted goat by nuclear transfer from cultured adult somatic cells[J]. Theriogenology, 2013, 79(2):225-233. DOI: 10.1016/j.theriogenology.2012.08.006
[27] LUO J, SONG Z, YU S, et al. Efficient generation of myostatin (MSTN) biallelic mutations in cattle using zinc finger nucleases[J]. PloS ONE, 2014, 9:e95225. DOI: 10.1371/journal.pone.0095225
[28] 高丽, 谌颜, 廷茂, 等.肌肉生长抑制素基因在哺乳动物中的最新研究进展[J].生物技术进展, 2014, 4(6):381-388. DOI: 10.3969/j.issn.2095-2341.2014.06.01 -
期刊类型引用(6)
1. 高正锋,宝童曦,徐丝,李先伟,杨绍磊,虞健,姚俊杰,毛璞麟,叶鹏,杨智斌,吕芬. 烟草黑胫病对不同类型植烟土壤化学性状及细菌群落的影响. 江苏农业科学. 2024(15): 255-261 .  百度学术
百度学术
2. 方宇,蔡永占,韩小女,白涛,刘冬梅,刘舜,王瑞宝,郭永升,陈小龙,黄飞燕,余磊,刘佳妮. 黑胫病对不同品种烟草根际土壤细菌群落的影响. 江苏农业科学. 2023(03): 118-125 .  百度学术
百度学术
3. 杨娅琳 ,陈健鑫 ,武自强 ,刘丽 ,张东华 ,马焕成 ,伍建榕 . 油茶根腐病根际土壤和根系内细菌群落结构及多样性. 经济林研究. 2023(02): 69-82 .  百度学术
百度学术
4. 代先强,杨盛刚,肖鹏,冉茂. 渝东北烟区土壤退化现状剖析. 西南大学学报(自然科学版). 2023(12): 65-75 .  百度学术
百度学术
5. 韩凤,章文伟,李巧玲,杨晓玉,林茂祥. 多花黄精根腐病对根际土壤细菌微生态的影响. 现代中药研究与实践. 2022(05): 6-11 .  百度学术
百度学术
6. 王伶瑞,红雨,李慧玲,李景环. 老芒麦、加拿大披碱草及其杂交一代根际土壤细菌群落结构和多样性. 北方农业学报. 2022(05): 24-33 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载: