Duplex PCR Assay for Simultaneous Detections of Staphylococcus aureus and Bordetella bronchiseptica in Rabbits
-
摘要: 为建立同时检测兔金黄色葡萄球菌和支气管败血波氏杆菌的双重PCR检测方法,本研究根据金黄色葡萄球菌的nuc基因和支气管败血波氏杆菌的fimN基因的保守序列设计2对特异性引物,通过优化反应条件,成功建立兔金黄色葡萄球菌和支气管败血波氏杆菌双重PCR检测方法。该方法对兔多杀性巴氏杆菌、大肠杆菌和魏氏梭菌的检测结果为阴性;能够检出5 pg的金黄色葡萄球菌和支气管败血波氏杆菌的基因组DNA;与单重PCR检测方法的符合率为100%。说明本试验建立的双重PCR检测方法具有良好的特异性、敏感性和准确性,为兔金黄色葡萄球菌和支气管败血波氏杆菌的鉴别诊断提供了有效的技术手段。Abstract: To develop a duplex PCR assay for simultaneous detections of Staphylococcus aureus and Bordetella bronchiseptica in rabbits, two pairs of specific primers were designed based on the conserved regions of nuc and fimN genes of the pathogens. The methodology with optimized reaction conditions was specific and free of cross-reactions with Pasteurella multocida, Escherichia coli and Clostridieum welchii. The detection limit of the method was 5 pg genome DNA on both pathogens. Moreover, the results obtained by using the duplex PCR assay were in perfect agreement with those determined separately by single PCR determinations. Thus, the newly developed highly specific, sensitive and accurate methodology could be a rapid assay applied for simultaneous identification of S. aureus and B. bronchiseptica present in a diseased rabbit.
-
Keywords:
- rabbit /
- Staphylococcus aureus /
- Bordetella bronchiseptica /
- duplex PCR assay
-
随着养兔业的规模化发展,呼吸道疾病已成为制约其发展的重要因素之一。其中,由金黄色葡萄球菌和支气管败血波氏杆菌感染导致的呼吸道疾病尤为突出。部分兔场由金黄色葡萄球菌感染导致的发病率约30%,病兔死亡率达90%以上[1];而支气管败血波氏杆菌的感染率可高达70%,导致感染兔生产性能低下[2]。由金黄色葡萄球菌和支气管败血波氏杆菌感染导致的呼吸道疾病具有相似的临床症状,如喷嚏、咳嗽、流鼻涕、严重者流脓性鼻涕;剖解均可见气管出血、肺脏出血坏死,严重者则表现为化脓性肺炎[3-6]。此外,在多数病例中还可见这两种病原菌的混合感染,给临床鉴别诊断带来困难[6]。
目前,针对兔金黄色葡萄球菌和支气管败血波氏杆菌的检测方法主要有细菌分离鉴定、血清学检测和单重PCR等[6-8],还未见能同时检测这两种兔源病原菌的双重PCR检测方法。本试验根据金黄色葡萄球菌的nuc基因和支气管败血波氏杆菌的fimN基因保守序列,设计2对特异性引物,建立兔金黄色葡萄球菌和支气管败血波氏杆菌双重PCR检测方法,以期为两种兔病原菌的鉴别诊断提供技术支持。
1. 材料与方法
1.1 试验材料
1.1.1 菌株
兔金黄色葡萄球菌、支气管败血波氏杆菌、多杀性巴氏杆菌、大肠杆菌和魏氏梭菌均由本实验室分离保存。
1.1.2 主要试剂
DL2000 Marker和胶回收试剂盒购自宝生物工程(大连)有限公司;2 × Easy Taq PCR SuperMix和细菌基因组DNA提取试剂盒购自北京全式金生物技术有限公司。
1.2 试验方法
1.2.1 引物设计与合成
根据GenBank中已发表的金黄色葡萄球菌nuc基因序列和支气管败血波氏杆菌fimN基因序列,利用Primer Premier 5.0软件设计2对特异性引物。引物由上海博尚生物技术有限公司合成,引物序列和扩增片段长度见表 1。
表 1 双重PCR引物Table 1. Primers used for duplex PCR assay病原 靶基因 引物序列(5′-3′) 参考序列登录号 产物大小/bp 金黄色葡萄球菌 nuc F:ttggttgatacacctgaaacaa;R:cgttgtcttcgctccaaata DQ399678 322 支气管败血波氏杆菌 fimN F:gtgatcaccggcaacatc;R:tgcctgtggctttcttca AF231910 478 1.2.2 单重PCR扩增与测序鉴定
以金黄色葡萄球菌和支气管败血波氏杆菌基因组DNA为模板,利用单引物进行PCR扩增。PCR扩增体系:2 × PCR Mix 25 μL,细菌基因组DNA 2 μL,上下游引物各2 μL,ddH2O补齐至50 μL。PCR反应程序:94℃预变性4 min;94℃ 30 s、56℃ 30 s、72℃ 30 s,30个循环;72℃延伸10 min。目的片段经1.5%琼脂糖电泳回收并送上海博尚生物技术有限公司测序。
1.2.3 双重PCR反应体系的建立及优化
将金黄色葡萄球菌和支气管败血波氏杆菌基因组DNA的质量浓度均调整至50 ng·μL-1,等体积混合,作为双重PCR的模板。将nuc基因上下游引物和fimN基因上下游引物均稀释至20 μmol·L-1,等体积混合作为双重PCR的引物。PCR扩增体系:2 × PCR Mix 25 μL,混合基因组DNA 2 μL,混合引物4 μL,ddH2O补齐至50 μL。PCR反应程序:94℃预变性4 min;94℃ 30 s、56℃ 30 s、72℃ 30 s,30个循环;72℃延伸10 min。在此基础上,将退火温度设置为53~60℃,混合引物终浓度设置为0.2、0.3、0.4、0.5、0.6 μmol·L-1对双重PCR反应条件进行优化,确定最佳的退火温度和引物浓度。
1.2.4 双重PCR的特异性试验
应用建立的双重PCR方法,对兔金黄色葡萄球菌、支气管败血波氏杆菌、多杀性巴氏杆菌、大肠杆菌和魏氏梭菌的基因组DNA进行PCR扩增,同时设置阴性对照,验证双重PCR检测方法的特异性。
1.2.5 双重PCR的敏感性试验
将金黄色葡萄球菌和支气管败血波氏杆菌基因组DNA的浓度均调整至50 ng·μL-1,等体积混合后进行10倍倍比稀释,以稀释的混合基因组DNA为模板,应用建立的双重PCR方法进行PCR扩增,检验该方法的敏感性。
1.2.6 临床样品的检测
63份已知结果的分离株或分离株混合样品,其中20份为金黄色葡萄球菌阳性,24份为支气管败血波氏杆菌阳性,14份为金黄色葡萄球菌和支气管败血波氏杆菌混合感染,5份为金黄色葡萄球菌和支气管败血波氏杆菌阴性样品。应用建立的双重PCR方法检测上述63份临床样品,比较该方法与已知结果的一致性。
2. 结果与分析
2.1 单重PCR扩增与测序鉴定
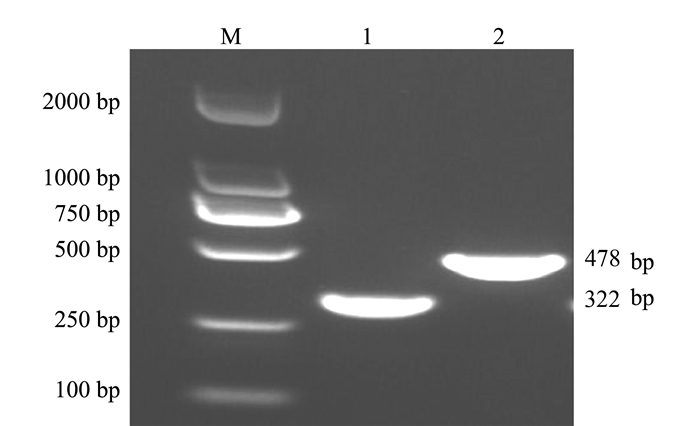
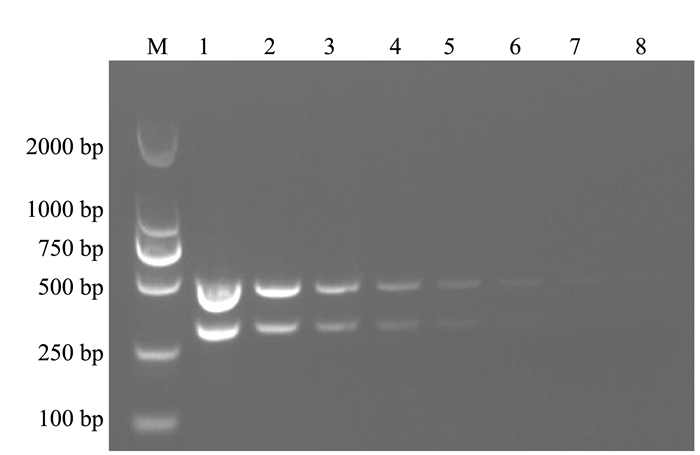
利用本试验设计的金黄色葡萄球菌nuc基因引物和支气管败血波氏杆菌fimN基因引物分别进行PCR扩增。结果显示,扩增得到的目的片段与预期相符,分别为322、478 bp(图 1)。将目的片段纯化回收并测序,测序结果表明扩增得到的2种病原的目的片段与参考序列的同源性均超过99%。
2.2 双重PCR反应体系的建立及优化
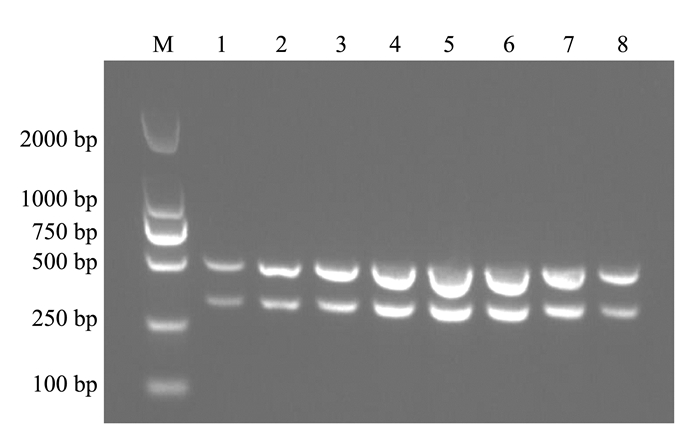
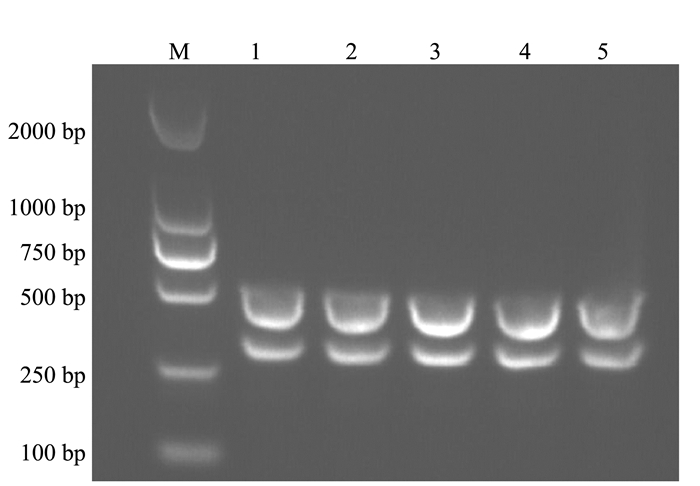
通过固定双重PCR反应体系中模板的量,依次对退火温度和引物浓度进行优化。试验结果表明当退火温度为55.8、57.5和58.8℃(图 2),引物浓度为0.4 μmol·L-1时(图 3),该双重PCR检测方法具有较好的扩增效果。根据退火温度高,特异性强的原则,确定最佳的退火温度为58.8℃。
2.3 双重PCR的特异性试验
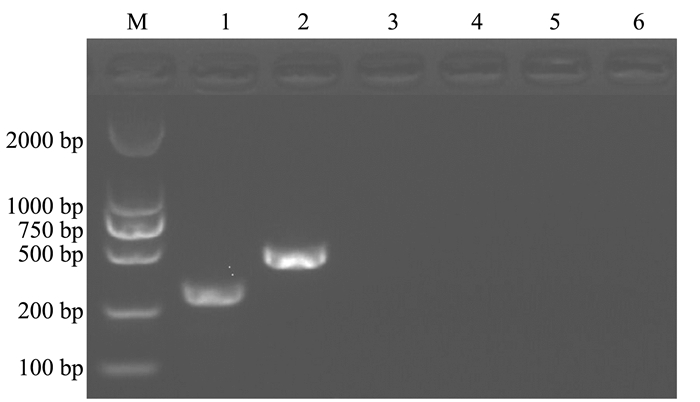
对多杀性巴氏杆菌、大肠杆菌和魏氏梭菌进行检测,结果显示该双重PCR方法与3种常见兔病原菌无交叉反应(图 4),表明该方法具有较好的特异性。
2.4 双重PCR的敏感性试验
对反应体系中DNA基因组含量为5 fg~50 ng的金黄色葡萄球菌和支气管败血波氏杆菌进行敏感性试验。当金黄色葡萄球菌和支气管败血波氏杆菌DNA基因组含量均低于5 pg时,扩增的目的条带较不明显(图 5)。结果说明,在50 μL PCR反应体系中,该双重PCR方法能检测到5 pg的金黄色葡萄球菌和支气管败血波氏杆菌DNA基因组。
2.5 临床样品的检测
应用建立的双重PCR方法对63份临床样品进行检测,结果(表 2)表明双重PCR的检测结果与已知结果的符合率为100%。说明该双重PCR方法准确性好。
表 2 临床样品检测结果Table 2. Pathogen detection of duplex PCR assay on clinic samples样品 已知结果/份 双重PCR方法鉴定结果/份 符合率/% 金黄色葡萄球菌 20 20 100 支气管败血波氏杆菌 24 24 100 混合感染 14 14 100 阴性 5 5 100 总计 63 63 100 3. 讨论
在众多引起兔呼吸道疾病的病原中,金黄色葡萄球菌和支气管败血波氏杆菌感染导致的临床症状和病变特征最相似,给这两种病原的鉴别诊断带来困难。金黄色葡萄球菌和支气管败血波氏杆菌的感染率和发病率均较高,且临床上主要依赖抗生素进行防治,药物的频繁使用导致耐药菌株的出现,使疾病愈来愈复杂[5-6, 9]。
nuc基因是金黄色葡萄球菌的特异基因。Brakstad OG等利用该基因上的保守序列建立了检测金黄色葡萄球菌的单重PCR检测方法[10]。向正刚等对四川部分区域分离的41株兔源金黄色葡萄球菌的研究结果表明,所有菌株均携带nuc基因[11]。fimN基因是支气管败血波氏杆菌的菌毛基因,保守、特异,编码的蛋白与细菌毒力相关。刘燕等[12]根据该基因设计了1对特异性引物,建立了检测兔支气管败血波氏杆菌的PCR快速检测方法。此外,还通过原核表达的fimN蛋白建立了间接ELISA方法[7, 13]。综上所述,以金黄色葡萄球菌nuc基因和支气管败血波氏杆菌fimN基因为目的基因能够建立检测这两种病原菌的特异性检测方法。
双重PCR反应体系不是单重PCR反应体系的单纯叠加,反应条件的优化是双重PCR建立的关键。本试验对退火温度和引物浓度进行优化后,确定最佳的退火温度为58.8℃,引物按1:1混合,最佳浓度为0.4 μmol·L-1。该双重PCR方法敏感性高,最低检出极限与刘燕等[12]建立的以fimN基因为目的基因的兔支气管败血波氏杆菌PCR检测方法和凤晓博等[14]建立的以nuc基因为目的基因的金黄色葡萄球菌PCR检测方法相同,能达到pg级;同时,该双重PCR方法特异性好,对其他3种常见兔病原菌无交叉反应。同时,通过对临床样品进行检测,该双重PCR方法与已知结果的符合率为100%。综上所述,本试验建立的双重PCR方法具有良好的特异性、敏感性和准确性,为兔金黄色葡萄球菌和支气管败血波氏杆菌的鉴别诊断提供了有效的技术手段。
-
表 1 双重PCR引物
Table 1 Primers used for duplex PCR assay
病原 靶基因 引物序列(5′-3′) 参考序列登录号 产物大小/bp 金黄色葡萄球菌 nuc F:ttggttgatacacctgaaacaa;R:cgttgtcttcgctccaaata DQ399678 322 支气管败血波氏杆菌 fimN F:gtgatcaccggcaacatc;R:tgcctgtggctttcttca AF231910 478 表 2 临床样品检测结果
Table 2 Pathogen detection of duplex PCR assay on clinic samples
样品 已知结果/份 双重PCR方法鉴定结果/份 符合率/% 金黄色葡萄球菌 20 20 100 支气管败血波氏杆菌 24 24 100 混合感染 14 14 100 阴性 5 5 100 总计 63 63 100 -
[1] 王孝友, 王永康, 杨睿, 等.兔葡萄球菌的分离与鉴定[J].中国养兔, 2011(4):12-14. DOI: 10.3969/j.issn.1005-6327.2011.04.004 [2] PATHAK A K, BOAG B, POSS M, et al. Seasonal breeding drives the incidence of a chronic bacterial infection in a free-living herbivore population[J]. Epidemiol infect, 2011, 139(8):2110-1219. http://europepmc.org/abstract/MED/20943004
[3] 张亚黎, 孙志强.家兔葡萄球菌病的初步诊断及防治[J].畜牧兽医杂志, 2015, 34(1):132-134. DOI: 10.3969/j.issn.1004-6704.2015.01.058 [4] 姜常青, 赵永峰, 刁非非, 等.兔源金黄色葡萄球菌的分离鉴定[J].山东畜牧兽医, 2015, 36(9):10-11. DOI: 10.3969/j.issn.1007-1733.2015.09.005 [5] 刘燕, 韦强, 肖琛闻, 等.兔波氏杆菌研究进展及防控对策思考[J].中国养兔, 2014(4):36-38. DOI: 10.3969/j.issn.1005-6327.2014.04.010 [6] 王晓芳, 刘燕, 肖琛闻, 等.兔支气管败血波氏杆菌的分离鉴定与耐药基因检测[J].中国畜牧兽医, 2015, 42(3):544-548. http://www.cnki.com.cn/Article/CJFDTOTAL-GWXK201503006.htm [7] 刘燕, 章春桃, 韦强, 等.兔波氏杆菌fimN蛋白间接ELISA抗体检测方法的建立[J].中国预防兽医学报, 2013, 35(11):899-902. DOI: 10.3969/j.issn.1008-0589.2013.11.09 [8] 马超锋, 陈铭, 徐永杰. PCR检测兔支气管败血波氏杆菌方法的建立及应用[J].河南农业科学, 2017, 46(4):124-127. http://d.old.wanfangdata.com.cn/Periodical/hnnykx201704025 [9] 邓钊宾, 余滔, 耿毅, 等.兔源金黄色葡萄球菌的耐药性及耐药基因分析[J].中国预防兽医学报, 2016, 38(1):45-48. DOI: 10.3969/j.issn.1008-0589.2016.01.11 [10] BRAKSTAD O G, AASBAKK K, MAELAND J A. Detection of Staphylococcus aureus by polymerase chain reaction amplification of the nuc gene[J]. J Clin Microbiol, 1992, 30(7):1654-1660. http://d.old.wanfangdata.com.cn/OAPaper/oai_pubmedcentral.nih.gov_265359
[11] 向正刚, 耿毅, 张雨薇, 等.四川兔源金黄色葡萄球菌毒力检测及分子分型[J].华南农业大学学报, 2017, 38(4):62-68. http://d.old.wanfangdata.com.cn/Periodical/hnnydxxb201704011 [12] 刘燕, 章春桃, 韦强, 等.兔支气管败血波氏杆菌PCR快速检测方法的建立及应用[J].中国养兔, 2012(4):13-15. DOI: 10.3969/j.issn.1005-6327.2012.04.003 [13] 章春桃, 刘燕, 韦强, 等.兔支气管败血波氏杆菌fimN基因的原核表达[J].浙江农业学报, 2011, 23(5):890-893. DOI: 10.3969/j.issn.1004-1524.2011.05.006 [14] 凤晓博, 赵青, 林童.食品中金黄色葡萄球菌PCR检测方法的建立[J].青海畜牧兽医杂志, 2014, 44(5):15-16. DOI: 10.3969/j.issn.1003-7950.2014.05.009 -
期刊类型引用(7)
1. 兰世捷,张蕾,李莉,江波涛,李丹,沈思思,刘博超,于辰龙,苗艳. 一例兔支气管败血波氏杆菌的诊治. 中国养兔杂志. 2024(02): 29-30 .  百度学术
百度学术
2. 刘秋瑾,白长胜,尹珺伊,张军,王岩,田秋丰,王欢,苗艳,薛沾枚,兰世捷,金振华,王丽坤. 兔常见呼吸系统疾病诊断与防治. 中国养兔杂志. 2024(05): 45-47 .  百度学术
百度学术
3. 张贺,陶坤盛,陈见兴,王豪杰,陈洪岩,王玉娥,夏长友. 兔源多杀性巴氏杆菌、金黄色葡萄球菌和肺炎克雷伯菌多重PCR检测方法的建立. 实验动物科学. 2023(04): 10-16 .  百度学术
百度学术
4. 叶健强,于吉锋,郭志强,林毅,肖璐,谢晶,曹冶,叶勇刚,吴学婧,毛丛剑,李兴玉,潘梦,魏甬,张先惠,康润敏. 四川地区兔波氏杆菌分离鉴定及耐药性分析. 中国养兔杂志. 2022(05): 4-7 .  百度学术
百度学术
5. 张倩文,刘玉梅,王玉琴,张飞可,刘凤军,张自强. 兔源性支气管败血波氏杆菌和金黄色葡萄球菌的分离鉴定及抗菌药物敏感性分析. 中国养兔杂志. 2022(06): 17-21 .  百度学术
百度学术
6. 任永军,杨泽晓,邝良德. 齐卡巨型兔结膜炎病症细菌学研究. 中国养兔. 2020(02): 7-11 .  百度学术
百度学术
7. 王锦祥,桑雷,孙世坤,陈冬金,陈岩峰,谢喜平. 福建省部分地区兔波氏杆菌病和巴氏杆菌病的流行病学调查. 中国养兔. 2019(02): 17-18+7 .  百度学术
百度学术
其他类型引用(3)




 下载:
下载: