Fungal Community in Soil of Wulongjiang Wetlands Analyzed Using PCR-DGGE
-
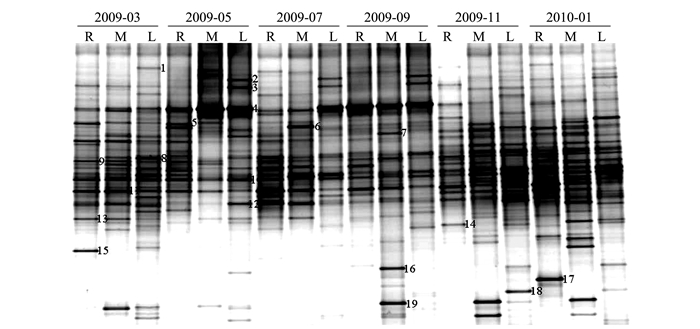
摘要: 为了解乌龙江湿地土壤真菌群落结构组成及动态变化,本研究通过稀释平板法对湿地土壤可培养真菌数进行测定,并采用变性梯度凝胶电泳(DGGE)技术分析乌龙江湿地土壤真菌群落结构。平板计数结果表明,不同时间不同采样点可培养真菌数的变化幅度较小,每克干土中可培养真菌数介于0.13×104~8.26×104 CFU。真菌18S rDNA的PCR-DGGE图谱显示,每个泳道条带的位置、数目和亮度各有不同,说明不同采样时间不同采样点土壤真菌群落结构存在着差异。DGGE图谱条带多样性分析结果表明,2009年3月、2009年11月和2010年1月所采集土壤样品的真菌群落多样性较其他时间更为丰富;从采样点来看,真菌群落丰富度则表现为样品L >样品M >样品R。对DGGE主要条带和差异性条带进行克隆测序后发现,乌龙江湿地土壤主要真菌类群为子囊菌Ascomycota和毛霉菌Mucoromycota。Abstract: Composition and dynamics of the fungal community in soil of Wulongjiang wetlands were studied. The classical plate count and the denatured gradient gel electrophoresis (DGGE) were applied to determine the cultivable population and diversity of the community. The plate counts of the samples averaged between 0.13×104 and 8.26×104 CFU per g of dry soil with no significant difference due to the locations or time of collection. On the other hand, the PCR-DGGE patterns of 18S rDNA (V1+V2) fragments exhibited variations on the positions, number and lightness of the bands from different lanes, indicating compositional differences among the fungal populations. The DGGE bands digitally analyzed by Quantity One software and the derived Shannon-Wiener index, evenness and abundance showed greater diversities in the samples obtained in March 2009, September 2009 and January 2010 than other times of a year. They also unveiled the differences in abundance of Sample L > Sample M > Sample R. The dominant fungi in the soil were identified to be Ascomycota and Mucoromycota according to a sequence analysis on the DGGE bands.
-
Keywords:
- Wulongjiang wetland /
- soil fungi /
- community composition /
- PCR-DGGE /
- diversity analysis
-
猪流行性腹泻(Porcine epidemc diarrhea,PED)由猪流行性腹泻病毒(Porcine epidemic diarrhea virus,PEDV)引起猪群发生呕吐、腹泻、脱水以及哺乳仔猪高死亡率为特征[1]的高度传染性疾病。所有不同阶段的猪均可感染。该病在许多养猪业发达的国家都已有爆发的报道, 并导致造成了重大的经济损失[2]。
PED首次是在1971年于英国报道[3],1978年在比利时和英国首次得到鉴定[4],我国于1984年证实该疾病的存在[5]。近年来,由于PEDV发生了变异,导致广泛流行,尤其以韩国、日本、中国、泰国和越南等国家发病严重[6-9]。自2010年秋以来, 首先我国部分省份出现了严重的仔猪流行性腹泻, 后蔓延至全国,发病情况比先前更为凶猛,造成仔大量的哺乳仔猪死亡,尤其是7日龄以内的仔猪死亡率高达100%,给养殖户造成了巨大的经济损失,并已成为影响我国养猪业健康发展的重要疫病之一。由于PED与猪传染性胃肠炎(TGE)等其他腹泻疾病在流行病学、临床症状等变化上非常相似,加上病毒变异,这给该病的快速诊断与防治都带来了一定困难。本研究通过采用单克隆抗体制备技术,制备获得特异性强和滴度高的PEDV单克隆抗体,对建立该病的快速诊断与防控技术具有重要意义, 更为今后开展PEDV抗原表位识别及病毒蛋白研究奠定良好基础。
1. 材料与方法
1.1 试验动物、细胞和病毒
6~8周龄SPF级Babl/C小鼠,购自吴氏实验动物有限责任公司,Vero细胞、小鼠骨髓瘤细胞(SP2/0) 由本实验室保存,猪繁殖与呼吸综合征病毒(PRRSV)、猪瘟病毒(CSFV)、猪传染性胃肠炎病毒(TGEV)均由本实验室分离保存,猪流行性腹泻病毒(PEDV)由本实验室通过空斑纯化技术获得保存。
1.2 试剂与培养液
DMEM、弗氏完全佐剂、弗氏不完全佐剂、羊抗鼠IgG辣根过氧化物酶、HAT、HT选择培养基均购自Sigma公司;羊抗鼠FITC购自武汉博士德生物工程有限公司;新生牛血清购自浙江天杭生物科技有限公司。NAbTMSpin Kits试剂盒和单克隆抗体亚级份检测试剂盒购自Thermo公司。
1.3 PEDV培养与纯化
将PEDV接种于Vero细胞单层,于37℃感作45 min,加维持液,培养2~3 d,当细胞病变达85%以上时,收集冻融3次,收获细胞毒。细胞毒经超声裂解后,10 000 r·min-1离心60 min,取上清液,45 000 r·min-1离心180 min,用0.01 mol·L-1PBS(pH 7.2) 悬浮沉淀,即为粗提病毒;取粗提病毒铺依次垫于30%~60%蔗糖-PBS,33 000 r·min-1离心180 min,收集条带病毒,PBS重悬,40 000 r·min-1离心180 min洗脱蔗糖,PBS重悬沉淀即为纯化的病毒抗原。同时以未接种病毒的Vero细胞同样处理,作为阴性抗原。
1.4 蛋白浓度的测定
蛋白浓度测定采用NaNodrop2000仪器, 其方法按说明书进行。
1.5 间接ELISA方法
病毒抗原用pH 9.6的碳酸盐缓冲液稀释,包被于ELISA板条,100 μL·孔-1,置37℃孵育2 h或4℃过夜,0.01 mmol·L-1 PBST洗涤液洗涤3次,用1.5%BSA-PBST封闭,300 μL·孔-1,37℃ 2 h,洗涤同上,加入杂交瘤细胞培养上清液,100 μL·孔-1,37℃反应60 min,同上洗涤,加1:40000稀释的羊抗鼠IgG辣根过氧化物酶,100 μL·孔-1,37℃反应45 min,同上洗涤后,加入OPD 100 μL·孔-1,37℃避光显色15 min,2 mol·L-1 H2SO4终止反应,在自动酶联检测仪上测定各孔的OD490值,以P:N≥2.1时,判断为杂交瘤细胞分泌抗体阳性。
1.6 杂交瘤细胞株的建立
1.6.1 Balb/c小鼠的免疫
将纯化PEDV抗原(4 mg·mL-1)与等体积弗氏完全佐剂乳化后,皮下多点注射6周龄Babl/C鼠4只,0.2 mL·只-1。于初次免疫后第14、28、42 d,取病毒抗原与弗氏不完全佐剂等量混匀乳化,进行二免、三免和四免,于融合前3 d用等量病毒经尾静脉加强免疫。
1.6.2 细胞融合
无菌取免疫小鼠脾脏,分散脾淋巴细胞,1 000 r·mim-1离心10 min, 将细胞疏松后加10 mL 0.17 mmol·L-1 NH4CL,冰浴10 min,同上离心,疏松、重悬于10 mL DMEM, 同时收集SP2/0细胞,按脾细胞和SP2/O细胞按8:1的比例混合,1 000 r·min-1离心5 min,疏松后1 min内缓缓加入1 mL 37℃预热的PEG进行细胞融合,缓慢加入DMEM 20 mL,同上离心,疏松细胞后,重悬杂交瘤细胞于含20%牛血清的HAT-DMEM培养基中,调节脾细胞数量,加到96孔细胞培养板,0.1 mL·孔-1,置37℃,5%CO2培养箱中培养,第5 d补加0.1 mL含15%牛血清的HT-DMEM,观察生长情况,待细胞长至孔底的1/3,或培养液变黄时,上清进行抗体检测。
1.6.3 阳性杂交瘤细胞的筛选
用间接ELISA筛选杂交瘤细胞生长孔特异性抗体,从检出的阳性孔中,挑选OD值高、细胞形态好生长旺盛且不与正常细胞培养物交叉的阳性孔,进行有限稀释法克隆。
1.6.4 饲养层细胞的制备
取8周龄左右的Babl/C小鼠,腹腔注射10 mL DMEM,轻揉小鼠腹腔数次,用灭菌针头在超净台内引出注入的DMEM。计数后调整细胞浓度加入96孔细胞培养板,100 μL·孔-1,置37℃,5%CO2培养箱中。
1.6.5 阳性细胞的克隆
采用有限稀释法,取经ELISA初筛为阳性细胞,用含20%牛血清的HT-DMEM逐步稀释至每毫升20个细胞,加到含饲养层细胞的96孔培养板中,每孔滴加1滴,置37℃,5%CO2培养箱中培养。5 d后观察克隆细胞生长情况,挑选只含一个细胞克隆的孔待细胞克隆生长至1/3孔底或上清液变黄时,取上清用间接ELISA检测。连续克隆直至克隆孔阳性率达100.0%。
1.7 腹水制备
1.7.1 Babl/C小鼠诱导
8周龄Balb/c小鼠腹腔注射灭菌的液体石蜡进行诱导,分笼饲养7 d。取对数生长期的杂交瘤细胞,经1 500 r·min-1离心5 min沉淀细胞,用不含血清的DMEM约1 mL重悬,腹腔注射石蜡诱导的Babl/C鼠,每只小鼠注射0.8×106杂交瘤细胞。
1.7.2 收集腹水
约7~10 d后观察小鼠腹部,有产生腹水的小鼠腹部会明显膨大。此时采用引流收集腹水,1 000 r·min-1,离心15 min,收集上层淡黄色腹水,用Thermo公司生产的NAbTMSpin Kits试剂盒进行纯化,测定效价,做好标记,冻于-70℃备用。
1.8 PEDV感染细胞的制备及免疫荧光试验(IFA)
将PEDV接种于已长成单层的Vero 96孔细胞板,培养至30%细胞出现病变时,弃上清,PBS洗涤1次,每孔加入预冷甲醇100 μL,4℃固定30 min,弃甲醇,PBS洗涤1次,晾干后,-30℃冻存备用。同样处理不接毒的Vero细胞用于阴性对照。IFA检测时,于上述细胞板中每孔加入30 μL杂交瘤细胞培养上清液于37℃作用30 min,用生理盐水洗涤3次,每次5 min,加FITC每孔50 μL,37℃作用30 min,洗涤同上,甩干,加50%PBS-甘油,每孔30 μL。于倒置荧光显微镜下观察。
1.9 单克隆抗体特性分析
1.9.1 单克隆抗体亚级份的测定
按照单克隆抗体分型试剂盒说明书进行。
1.9.2 单克隆抗体中和能力测定
参考文献[10]进行。采用固定病毒稀释抗体的方法测定各株单抗对PEDV的中和能力。将克隆抗体腹水10-1开始进行10倍比稀释至10-6,取各稀释度的单克隆抗体与等体积病毒液混合,37℃感作45 min,然后接种单层Vero细胞。试验设正常细胞对照、阴性腹水对照和病毒对照。接种24 h后观察细胞病变(CPE),连续观察96 h,按Karber法计算中和效价。
1.9.3 细胞株稳定性试验
将具有分泌特性的杂交瘤细胞体外连续培养2个月,每2周检测其上清液的抗体效价;将液氮冻存的阳性杂交瘤细胞每个月复苏1次,连续2个月,测定上清抗体效价。
1.9.4 单克隆抗体特异性的测定
应用间接ELISA和IFA方法检测腹水与Vero细胞、PRRSV、TGEV和CSFV的交叉反应性。
1.9.5 单克隆抗体ELISA效价测定
应用间接ELISA检测杂交瘤培养上清液和腹水抗体的效价,腹水用抗体稀释液按10倍稀释成10-8~10-1,杂交瘤细胞上清液用抗体稀释液稀释成2-10~2-1 ,测定OD490值,以P:N≥2.1时的最高稀释度为抗体的ELISA效价。
1.9.6 单克隆抗体荧光效价测定
应用间接免疫荧光法测定杂交瘤培养上清液和腹水的荧光特性,杂交瘤细胞上清液用抗体稀释液稀释成2-10~2-1 ,腹水用抗体稀释液按10倍稀释成10-8~10-2,以出现特异荧光的最高稀释度为单抗的IFA效价。
1.9.7 Western bloting试验
参照文献[10]方法, 分别以PEDV抗原和Vero细胞抗原进行SDS-PAGE电泳。转印至NC膜用TBS-T封闭, 4℃过夜, TBS-T洗膜3次, 加1:100倍稀释的腹水单克隆抗体, 37℃作用2 h,洗涤, 加入羊抗鼠IgG碱性磷酸酶标记抗体(1:10 000), 室温反应2 h, 同上洗涤, 显色。
2. 结果与分析
2.1 PEDV的培养、纯化及浓度测定
将PEDV接种于Vero细胞单层3 d后细胞病变达85%(图 1、2),经冻融、裂解及蔗糖-PBS梯度离心后,收集30%~40%病毒条带,经鉴定为PEDV后,测定蛋白质量浓度为4 mg·mL-1。
2.2 PEDV单克隆抗体的制备
2.2.1 ELISA筛选方法的建立
经方阵滴定法测定,当每孔抗原包被质量浓度为25 μg·mL-1、血清稀释度为1:2 000或每孔抗原包被质量浓度为35 μg·mL-1、血清稀释度为1:4 000时,阳性血清OD490值均达1.0,阴性血清的OD490 值较小,在0.08以下,最终确定最佳每孔抗原包被质量浓度为25~35 μg·mL-1。
2.2.2 杂交瘤细胞株的建立
融合8块96孔细胞板,获得256个融合阳性孔, 阳性率为33.3%,其中抗体分泌较强阳性的细胞孔36株。经多次有限稀释后,获得2株能稳定分泌抗PEDV抗体的杂交瘤细胞株,分别命名为E1和H6。这2株细胞在体外连续培2个月,能稳定分泌抗体,经液氮冻存、复苏后,细胞生长良好,且上清液抗体效价不变。
2.3 单克隆抗体特性分析
2.3.1 单克隆抗体Ig类别和亚类
经过抗体亚型试剂盒鉴定,2株单克隆抗体在亚类鉴定中E1属于IgG2a,H6株属于IgM。
2.3.2 单克隆抗体的中和活性
E1株和H6株单克隆抗体都不能抑制病毒的增殖,说明2株单克隆抗体无中和病毒的活性。
2.3.3 单克隆抗体ELISA和IFA效价
E1和H6单克隆抗体的培养上清液的ELISA效价分别为26和24,腹水抗体效价分别为105和104(图 3)。
2.3.4 单克隆抗体特异性鉴定
ELISA结果表明:2株单抗均能识别PEDV毒株;间接免疫荧光试验(IFA)结果表明:单抗都不与Vero细胞、TGEV、PRRSV和CSFV发生反应,说明单克隆抗体的特异性好。
2.3.5 Western bloting试验
本试验获得的2株单克隆抗体,其中E1株能识别PEDV中约31 ku蛋白(M蛋白),H6株能识别PEDV中约56 ku蛋白(N蛋白), 而不识别其他蛋白, 说明1株是针对M蛋白,另外1株是针对N蛋白。
3. 讨论
猪流行性腹泻病毒属于套式病毒目冠状病毒科冠状病毒属[11],主要的结构蛋白包括:纤突蛋白(S)、膜蛋白(M)和核衣壳蛋白(N),其中M蛋白在PEDV毒株间具有高度的保守性[12],在补体存在的条件下, 它可诱导机体产生中和抗体。N蛋白位于病毒粒子的内部,与病毒基因组RNA相互缠绕构成病毒的核衣壳,在同种病毒间也具有高度的保守性,参与病毒的复制, 其介导的特异性细胞免疫对于病毒的感染十分重要[13]。另外,PEDV的细胞培养与其他冠状病毒比, 在体外培养难, 细胞病变不明显, 抗体滴度也不高,这给抗原分离培养带来较大困难。基于PEDV的较难培养特性,丁壮[14]等通过PEDV猪体内的传代毒和人工感染猪的粪便中纯化出病毒,制备了抗PEDV的杂交瘤细胞株,另外,还有许多学者[15-16]利用体外表达病毒结构蛋白作为抗原,制备抗猪流行性腹泻病毒克隆抗体。
本研究利用从猪传染性胃肠炎-猪流行性腹泻-轮状病毒的三联弱毒疫苗中,通过空斑纯化技术,纯化获得PEDV弱毒,该病毒能在Vero细胞中稳定高效增殖,其TCID50/100 μL达到10-6.0;通过蔗糖梯度差速离心纯化,利用纯化抗原免疫小鼠,脾细胞与SP2/0细胞进行杂交融合,获得2株抗体效价高、特异性强、稳定性好的抗PEDV单克隆抗体,其中1株为IgG2a亚型,能识别PEDV的M蛋白, 另外1株为IgM,能识别PEDV的N蛋白。研究表明,PEDV的M蛋白和N蛋白在病毒的进化过程中都是比较保守稳定的蛋白,研制出相应的单克隆抗体,能为PEDV的早期诊断、防控、病毒免疫靶标识别及蛋白质组学的研究奠定良好基础。
本试验在单克隆抗体的制备过程中,曾疑使用PEDV弱毒株能否制备出效价高的单克隆抗体,但经过实践表明,SPF级Balb/c小鼠经过多次免疫,在杂交瘤细胞制备过程中注重无菌操作,把握融合时间,能获得高效价的单克隆抗体。本研究虽然筛选到能分泌阳性抗体的杂交瘤细胞数量较少,阳性率不是很高,但经过多次有限稀释克隆和特异性筛选,最终获得2株抗体效价高的单克隆抗体E1和H6株,这说明PEDV弱毒株经高度浓缩纯化后,仍具有很好的免疫原性,能刺激小鼠产生高效免疫应答,这为今后制备单克隆抗体的过程中,选择抗原方面提供了一个新思路。
-
表 1 乌龙江湿地土壤可培养真菌数量的动态变化
Table 1 Dynamics of culturable fungal population in Wulongjiang wetland soil
[单位/×104CFU·g-1(dry soil)] 样品名称 采样时间/(年-月) 2009-03 2009-05 2009-07 2009-09 2009-11 2010-01 R-1 6.18±0.81 4.32±0.55 4.43±0.12 5.94±0.43 4.04±0.43 8.26±0.28 R-2 2.68±0.44 2.50±0.80 4.09±0.77 1.99±0.14 1.93±0.36 4.96±0.51 R-3 1.02±0.03 8.62±0.18 1.73±0.22 2.75±0.62 1.60±0.81 2.80±0.84 M-1 6.03±0.54 3.73±0.86 2.45±0.35 2.75±0.63 1.63±0.23 0.59±0.12 M-2 2.41±0.46 1.34±0.18 3.51±0.76 3.57±0.23 4.50±0.99 4.44±0.23 M-3 1.95±0.31 1.84±0.07 2.24±0.41 1.87±0.19 4.73±0.61 2.19±0.51 L-1 2.27±0.45 0.29±0.06 0.84±0.58 0.50±0.01 1.14±0.18 0.88±0.16 L-2 2.11±0.19 0.56±0.11 2.00±0.71 0.19±0.09 0.90±0.05 0.33±0.08 L-3 1.24±0.15 1.66±0.44 1.91±0.76 0.23±0.04 2.49±0.17 0.13±0.01 表 2 DGGE图谱的Shannon-Wiener指数、均匀度和丰富度分析结果
Table 2 Shannon-Wiener index, evenness and abundance derived from DGGE patterns
采样时间/(年-月) 采样点 Shannon-Wiener指数 均匀度 丰富度 2009-03 R 3.18 0.97 27 M 3.13 0.97 25 L 3.18 0.98 26 2009-05 R 2.75 0.97 17 M 2.68 0.95 17 L 2.87 0.94 21 2009-07 R 3.04 0.97 23 M 2.75 0.97 17 L 2.88 0.96 20 2009-09 R 2.92 0.95 22 M 2.95 0.97 21 L 2.79 0.97 18 2009-11 R 3.08 0.98 23 M 3.18 0.97 26 L 3.23 0.98 27 2010-01 R 3.13 0.97 25 M 3.34 0.98 30 L 3.44 0.98 34 表 3 DGGE代表性条带的比对结果
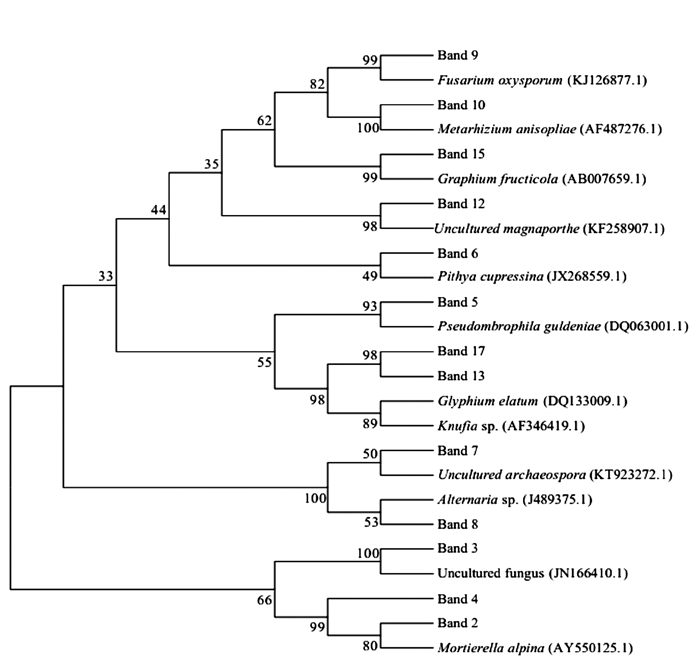
Table 3 Genomic sequences of dominant DGGE bands obtained by sequencing and BLAST analysis
编号 最相似菌株 登录名 相似率/% 最相似菌群 Band 1 Hyphochytrium catenoides X80344.1 99 Stramenopiles Band 2 Mortierella alpina AY550125.1 99 Mucoromycota Band 3 Uncultured fungus JN166410.1 99 Fungi Band 4 Mortierella alpina AY546098.1 99 Mucoromycota Band 5 Pseudombrophila guldeniae DQ063001.1 98 Ascomycota Band 6 Pithya cupressina JX268559.1 96 Ascomycota Band 7 Alternaria sp. GE KJ489375.1 100 Ascomycota Band 8 Uncultured archaeospora KT923272.1 100 Mucoromycota Band 9 Fusarium oxysporum KJ126877.1 99 Ascomycota Band 10 Metarhizium anisopliae AF487276.1 99 Ascomycota Band 11 Vischeria stellata KY271662.1 99 Stramenopiles Band 12 Uncultured magnaporthe KF258907.1 96 Ascomycota Band 13 Knufia sp. CBS 268.34 AF346419.1 99 Ascomycota Band 14 Liochthonius sp. AD1300 JQ000035.1 93 Arthropoda Band 15 Graphium fructicola AB007659.1 93 Ascomycota Band 16 Dicyrtomina environmental sample KF258916.1 95 Arthropoda Band 17 Glyphium elatum DQ133009.1 99 Ascomycota Band 18 Poduridae environmental sample EF024377.1 95 Arthropoda Band 19 Sminthuridae environmental sample EF024291.1 96 Arthropoda -
[1] 李甜甜, 胡泓, 王金爽, 等.湿地土壤微生物群落结构与多样性分析方法研究进展[J].土壤通报, 2016, 47(3):758-762. http://d.old.wanfangdata.com.cn/Periodical/trtb201603038 [2] 陈爱辉, 李朝霞, 梁慧星, 等. DGGE技术在湿地微生物多样性研究中的应用[J].湖北农业科学, 2010, 49(4):981-984. DOI: 10.3969/j.issn.0439-8114.2010.04.069 [3] 张晶, 陈书明, 王小国.天鹅湖湿地微生物群落PCR-DGGE分析[J].基因组学与应用生物学, 2016, 35(9):2423-2428. http://www.cnki.com.cn/Article/CJFDTOTAL-GXNB201609060.htm [4] ZELLES L, BAI Q Y, BECK T, et al. Signature fatty acids in phospholipids and lip-opolysaccharides as indicators of microbial biomass and community structure in agricultural soils[J]. Soil Biology and Biochemistry, 1992, 24(4):317-323. DOI: 10.1016/0038-0717(92)90191-Y
[5] 陈子熙, 陈磊, 张卫文.单细胞尺度下的微生物学研究:意义与方法[J].微生物学报, 2017, 57(6):920-931. http://d.old.wanfangdata.com.cn/Periodical/wswxb201706012 [6] 刘银银, 李峰, 孙庆业, 等.湿地生态系统土壤微生物研究进展[J].应用与环境生物学报, 2013, 19(3):547-552. http://d.old.wanfangdata.com.cn/Periodical/shidkx200902014 [7] ZHANG C P, WANG B, DAI X Y, et al. Structure and function of the bacterial communities during rhizoremediation of hexachlorobenzene in constructed wetlands[J]. Environmental Science and Pollution Research, 2017, 24:11483-11492. DOI: 10.1007/s11356-017-8463-1
[8] MARK B, HANNELE A, FREDERIK V K, et al. Susceptibility of constructed wetland microbial communities to silver nanoparticles:A microcosm study[J]. Ecological Engineering, 2016, 97:476-485. DOI: 10.1016/j.ecoleng.2016.10.033
[9] ZHONG F, WU J, DAI Y R, et al. Bacterial community analysis by PCR-DGGE and 454-pyrosequencing of horizontal subsurface flow constructed wetlands with front aeration[J]. Applied Microbiology and Biotechnology, 2015, 99:1499-1512. DOI: 10.1007/s00253-014-6063-2
[10] 佘晨兴, 仝川.闽江口芦苇沼泽湿地土壤产甲烷菌群落结构的垂直分布[J].生态学报, 2012, 32(17):5299-5308. http://d.old.wanfangdata.com.cn/Periodical/stxb201217002 [11] 曾志华, 杨民和, 佘晨兴, 等.闽江河口区淡水和半咸水潮汐沼泽湿地土壤产甲烷菌多样性[J].生态学报, 2014, 34(10):2674-2681. http://d.old.wanfangdata.com.cn/Periodical/stxb201410024 [12] 李振高, 骆永明, 滕应.土壤与环境微生物研究法[M].北京:科学出版社, 2008:90-92. [13] MAY L A, SMILEY B, SCHMIDT M G. Comparative denaturing gradient gel electrophoresis analysis of fungal communities associated with whole plant corn silage[J]. Canadian Journal of Microbiology, 2001, 47(9):829-841. DOI: 10.1139/w01-086
[14] BOWATTE S, ISHIHARA R, ASAKAWA S, et al. Characterization of ammonia oxidizing bacteria associated with weeds in a Japanese paddy field using amoA gene fragments[J]. Soil Science and Plant Nutrition, 2006, 52:593-600. DOI: 10.1111/j.1747-0765.2006.00077.x
[15] 赵兴青, 杨柳燕, 陈灿, 等. PCR-DGGE技术用于湖泊沉积物中微生物群落结构多样性研究[J].生态学报, 2006, 26(11):3610-3616. DOI: 10.3321/j.issn:1000-0933.2006.11.012 [16] RAVENSCHLAG K, SAHM K, PERUTHALER J, et al. High bacterial diversity in permanently cold marine sediments[J]. Applied and Environmental Microbiology, 1999, 65(9):3982-3989. http://d.old.wanfangdata.com.cn/OAPaper/oai_pubmedcentral.nih.gov_99730
[17] 蒲洋, 李文军, 王凯, 等.烟台市区河流入海口微生物群落的分析[J].海洋科学, 2017, 41(7):9-15. http://d.old.wanfangdata.com.cn/Periodical/hykx201707002 [18] 赵先丽, 周广胜, 周莉, 等.盘锦芦苇湿地土壤微生物数量研究[J].土壤通报, 2008, 39(6):1376-1379. DOI: 10.3321/j.issn:0564-3945.2008.06.031 [19] 亢宗静, 袁楠, 王蓥燕, 等.若尔盖高原湿地的真菌群落结构及低温纤维素降解真菌特征[J].土壤通报, 2017, 48(4):830-836. http://d.old.wanfangdata.com.cn/Periodical/trtb201704009 [20] FENG S G, ZHANG H X, WANG Y F, et al.Analysis of fungal community structure in the soil of Zoige Alpine W etland[J]. Acta Ecologica Sinica, 2009, 29:260-266. DOI: 10.1016/j.chnaes.2009.09.001
[21] 赵先丽, 周广胜, 周莉, 等.盘锦芦苇湿地土壤微生物特征分析[J].气象与环境学报, 2006, 22(14):64-67. http://d.old.wanfangdata.com.cn/Periodical/lnqx200604012 [22] 邱权, 陈雯莉.三峡库区小江流域消落区土壤微生物多样性[J].华中农业大学学报, 2013, 32(3):15-20. DOI: 10.3969/j.issn.1000-2421.2013.03.003 [23] CHAN O C, YANG X D, FU Y, et al. 16S rRNA gene analyses of bacterial community structures in the soils of evergreen broad-leaved forests in south-west China[J]. FEMS Microbiology Ecology, 2006, 58:247-259. DOI: 10.1111/fem.2006.58.issue-2
[24] 吕新, 陈丽华, 刘兰英, 等.抗真菌转基因水稻根际土壤真菌群落结构的动态变化[J].中国生态农业学报, 2012, 20(10):1340-1346. http://d.old.wanfangdata.com.cn/Periodical/stnyyj201210013 [25] 徐严.若尔盖高原湿地土壤真菌的初步研究[D].成都: 四川农业大学, 2008. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1403154 [26] 陈会海, 许修宏, 李洪涛.应用PCR-DGGE分析三江湿地土壤真菌群落结构的多样性[J].环境科学研究, 2012, 25(11):1272-1278. http://d.old.wanfangdata.com.cn/Periodical/hjkxyj201211012 -
期刊类型引用(6)
1. 李虎林,颜仁和,陈泽典,仇珍珍,李堪贺,马曼欣,毛莹莹,李建军,吕宗吉,李红卫. 基于哺乳动物细胞表达S1蛋白的猪流行性腹泻病毒单克隆抗体. 分子诊断与治疗杂志. 2023(04): 694-698 .  百度学术
百度学术
2. 张志榜,彭维祺. 猪流行性腹泻病毒单克隆抗体及其抗原表位的研究进展. 病毒学报. 2022(01): 235-245 .  百度学术
百度学术
3. 李洁森,孙荣航,邝燕齐,陈路漫,刘青,郭霄峰. 猪流行性腹泻病毒S1D蛋白的优化表达及其单克隆抗体的制备. 中国畜牧兽医. 2021(12): 4641-4651 .  百度学术
百度学术
4. 赵洪哲,范峻豪,李新培,王昊,关平原,温永俊. 牛病毒性腹泻病毒单克隆抗体的制备及其应用. 中国兽医科学. 2019(03): 287-293 .  百度学术
百度学术
5. 张庆桥,王一鹏,魏艳秋,米建华,赵雪,孙立旦,宋勤叶. 猪流行性腹泻病毒N蛋白单克隆抗体的制备与鉴定. 中国兽医杂志. 2019(01): 31-35+3 .  百度学术
百度学术
6. 马宇聪,刘增素,王书博,周晗,姜艳萍,崔文,王丽,乔薪瑗,唐丽杰,徐义刚,李一经. PEDV双抗体夹心ELISA检测方法的建立. 中国兽医科学. 2019(09): 1152-1159 .  百度学术
百度学术
其他类型引用(2)





 下载:
下载: