Aromatics Determination of Xinbai 8 Loquat by HS-SPME Internal Standard Method
-
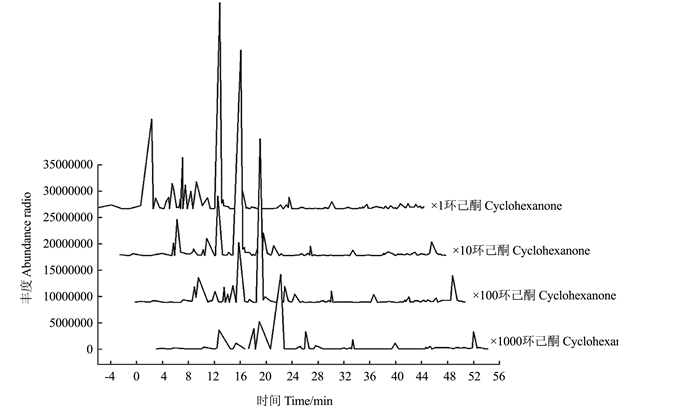
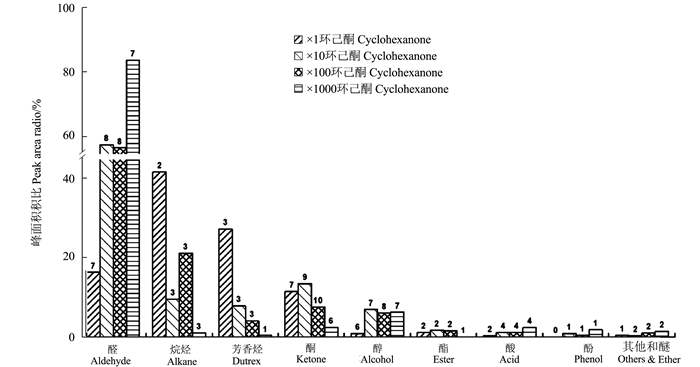
摘要:目的 探究新白8号枇杷香气成分及内标物的最适浓度,以期为白肉枇杷香气成分的研究及内标选择提供依据。方法 以白肉枇杷新白8号果实为试材,加入4种不同浓度等体积的环己酮溶液(947、94.7、9.47、0.947μg·μL-1)为内标,采用HS-SPME-GC/MS技术,对试材的香气成分进行定性和定量分析。结果 新白8号枇杷果肉中共检测出10类43种香气成分,以醛类、烷烃、芳香烃、酮类和醇类为主,其中相对含量较高的物质有己醛、(E)-2-己烯醛、正丁基环己烷、2-庚酮、正戊基环己烷、(E)-2-己烯-1-醇,苯乙烯等。4种环己酮浓度的样品分别检测出有效香气化合物为30、39、41和32种,有效峰面积占总峰面积比分别为38.20%、28.49%、42.70%和39.51%;环己酮峰面积比分别为47.38%、58.55%、36.37%和25.86%。加入9.47 μg·μL-1环己酮的样品检测出的香气物质种类最多、有效峰面积比最高、环己酮及各香气成分峰面积占比适宜。结论 新白8号香气成分丰富多样,9.47 μg·μL-1环己酮为枇杷果实香气成分固相微萃取的适宜内标浓度。Abstract:Objective To determine the aromatic composition of loquat fruit and cyclohexanone concentration for the HS-SPME-GC/MS internal standard method.Methods The pulp of Xinbai 8 fruits was added with a cyclohexanone solution in the concentration of 947, 94.7, 9.47, 0.947 μg·μL-1 at a same volume as the internal standard for HS-SPME-GC/MS analysis.Results The analysis detected 10 classifications of chemicals including aldehydes, alkanes, dutrex, ketones and alcohols. Hexanal, (E)-2-hexenal, n-butyl cyclohexane, 2-heptanone, n-pentyl cyclohexane, (E)-2-hexene-1-alcohol, and styrene were the dominating volatiles among the 43 compounds identified.In the cyclohexanone-added samples, the decreasing concentration produced 31, 40, 42 and 33 aromatic substances with the effective peak area ratios of 38.20%, 28.49%, 42.70% and 39.52%, and the peak area ratios of 38.20%, 58.55%, 36.37% and 25.86%, respectively. A maximum number of aromatics was found in the sample that was added with 9.47 μg·μL-1 cyclohexanone which also had the highest effective peak area ratio and optimum peak area radio.Conclusion The aromatics in the fruits of Xinbai 8 were diverse, and the cyclohexanone concentration at 9.47 μg·μL-1 was the choice internal standard for the analytical.
-
Keywords:
- loquat /
- aromatics /
- cyclohexanone /
- internal standard /
- SPME /
- GC-MS
-
0. 引言
【研究意义】镉(Cadmium,Cd)是环境中毒性最强的重金属元素之一,被联合国环境规划署列为具有全球意义的危险物质之首[1]。随着城市化、工业化的迅速发展,福州市城区土壤和农田土壤均受到重金属Cd污染,研究发现城区土壤和农田土壤中的Cd含量均超过福建省土壤背景值,相对于其他重金属元素,Cd元素存在严重积累现象[2-3]。不结球白菜作为Cd超富集蔬菜,在Cd胁迫下不结球白菜呈现叶片黄化、植株矮小的毒害症状[4-5],不结球白菜幼苗叶绿素的含量显著降低,光合作用受到抑制,同时产生过量的活性氧,造成膜质过氧化损伤[6],Cd在蔬菜中富集积累,可通过食物链传递危害人体健康[7]。【前人研究进展】水杨酸(Salicylic acid,SA)是植物体内广泛存在的一种酚类化合物,它不仅参与调节植物生长发育的生理过程,还能诱导植物对低温、盐碱、重金属等胁迫产生抗性[8]。近年来,关于SA缓解植物Cd胁迫的研究较为广泛,研究表明,SA能缓解Cd对花椰菜种子萌发和幼苗生长的抑制[9];外施SA可降低小麦根部Cd含量,提高光合速率,增强小麦的耐Cd能力[10];外源SA处理莴苣幼苗后,可以有效缓解Cd对莴苣幼苗生长的抑制作用[11];SA预处理可以缓解Cd胁迫对番茄生长的毒害作用,降低番茄根、叶中的Cd积累量[12]。【本研究切入点】不结球白菜(Brassica chinensis L.)为十字花科芸薹属芸薹种白菜亚种,原产于我国,种质资源丰富[13],生长快速、口感清爽、营养丰富[14],是福建省栽培最广的绿叶蔬菜之一。不结球白菜作为Cd敏感植物,更容易从土壤中吸收Cd并转移至可食部位[15]。目前,关于将SA用于缓解Cd对不结球白菜毒性效应的研究鲜见报道。【拟解决的关键问题】本试验以不结球白菜为材料,采用穴盘育苗,研究Cd胁迫下不同质量浓度SA处理对不结球白菜幼苗形态、生理及Cd富集量的影响,探讨SA诱导不结球白菜抗Cd胁迫的响应及对Cd吸收积累和转运差异,为利用SA减轻Cd胁迫对不结球白菜的伤害提供理论依据,在生产上为提高作物抗重金属栽培提供新方法。
1. 材料与方法
1.1 试验材料
以华冠不结球白菜为供试材料,产地为日本株式会社武藏野种苗园,该品种生育期短、属矮脚种、叶柄深绿肥厚,具有耐暑、耐病及耐雨等特性。以珍珠岩、草炭作为育苗基质。
1.2 试验方法
试验于2018年12月19日至2019年1月28日在福建省农业科学院中以示范农场玻璃温室和生理生化实验室进行。不结球白菜播种时间为12月19日,出苗时间为12月21日,试验共设6个处理,每个处理重复3次。将草炭与珍珠岩以2∶1体积比例(V/V)配成复合基质,将基质装入72孔穴盘中。不结球白菜播种后置于玻璃温室植物工厂育苗,采用的营养液配方为每200 L添加A:Ca(NO3)2 16 kg,KNO3 6 kg;B:KHPO4 3 kg,MgSO4 10 kg,EDTA-Fe 460 g,MnSO4 120 g,ZnSO4 60 g,CuSO4 4 g,NH4Mo 1.5 g,HBO3 60 g[16]。不结球白菜幼苗长至两叶一心时,于每天上午9:00,对幼苗进行以下处理:(1)空白对照(CK1)和Cd胁迫对照组(CK2),叶面均喷施去离子水;(2)叶面喷施去离子水配制的0.01 mmol·L−1SA溶液;(3)叶面喷施去离子水配制的0.05 mmol·L−1SA溶液;(4)叶面喷施去离子水配制的0.1 mmol·L−1SA溶液;(5)叶面喷施去离子水配制的0.5 mmol·L−1SA溶液。连续喷施3 d,叶片以正反两面全部湿润且无液体滴下为准。3 d后开始Cd胁迫处理,除CK1用正常营养液培养,其余处理用含50 mg·L−1 CdCl·2.5H2O营养液培养。分别在Cd胁迫处理的第5 d、第10 d取样测定不结球白菜幼苗的形态指标和生理指标。
1.3 测定项目与方法
1.3.1 形态指标
株高:用直尺测量植株基部到顶端生长点的长度;茎粗:用游标卡尺测定植株子叶下2 cm的直径;根长采用WinRHIZO加拿大根系分析系统测定;叶面积用YMJ-B型叶面积测定仪(浙江托普云农科技股份有限公司)测量;地上/地下部鲜干重:用JJ223BC型电子天平(感量为0.1 mg)进行测量;壮苗指数=(茎粗/株高+地下部干质量/地上部干质量)×植株干质量[17];根冠比=地下部鲜质量/地上部鲜质量。取样时,每个处理分别选取10株长势一样且具有代表性的植株。
1.3.2 叶片生理指标
叶绿素(Chl)含量采用张宪政[18]的丙酮乙醇混合液法,可溶性蛋白含量的测定采用杨晴[19]的考马斯亮蓝G-250染色法;脯氨酸(Pro)含量采用磺基水杨酸法,丙二醛(MDA)含量采用硫代巴比妥酸法,根系活力采用TTC法,超氧化物歧化酶(SOD)活性采用氮蓝四唑(NBT)法,过氧化物酶(POD)活性采用愈创木酚法,过氧化氢酶(CAT)活性采用紫外吸收比色法[20]。取样时,每个处理随机选取长势一致的植株,撕取相同部位的叶片,去除叶脉后,剪碎混匀,重复测试3次。叶片生理指标测定的部位均以鲜重(FW)计算。
1.3.3 镉含量测定
将不结球白菜幼苗从基质中取出,依次用自来水、超纯水洗涤,将地上与地下部分分开,于105 ℃杀青30 min,70 ℃烘干至恒重,用不锈钢粉碎机粉碎备用。取1 g烘干样品,经混合酸高温消煮成透明或淡黄色液体,用火焰原子吸收光谱法测定茎叶和根Cd含量[21],并计算转运系数。
转运系数=地上部分镉含量/地下部分镉含量[22]
1.4 数据处理
试验数据采用Excel、DPS v7.05 数据处理软件进行统计和分析。
2. 结果与分析
2.1 外源SA对Cd胁迫下不结球白菜幼苗生长的影响
从表1可以看出,Cd胁迫5 d,与CK1相比,CK2的不结球白菜幼苗生长受到抑制,其株高、茎粗、根长、叶面积、根冠比和壮苗指数分别下降6.88%、16.88%、5.58%、4.91%、42.31%和30.50%;0.01 mmol·L−1、0.05 mmol·L−1SA处理的不结球白菜各生长指标均高于CK2,但与CK1相比,株高、茎粗差异不显著,根长、叶面积显著高于CK1,根冠比、壮苗指数显著降低;SA质量浓度高于0.05 mmol·L−1,幼苗生长量反而下降。Cd胁迫10 d,CK2处理的不结球白菜幼苗的生长量依旧低于CK1,其中根冠比下降幅度达到62.27%;0.01 mmol·L−1、0.05 mmol·L−1SA处理的不结球白菜幼苗各生长量均高于CK2;与CK1相比,幼苗的株高、茎粗均升高,而根长、叶面积、根冠比、壮苗指数均下降;当SA质量浓度高于0.05 mmol·L−1,幼苗生长呈下降趋势。
表 1 外源SA对Cd胁迫下不结球白菜幼苗生长的影响Table 1. Effect of exogenous SA on growth of non-heading Chinese cabbage seedlings under Cd-stress处理时间
Processing time/dSA/(mmol·L−1) 株高
Plant height/cm茎粗
Stem thickness/cm根长
Root length/cm叶面积
Leaf area/cm2根冠比
Root shoot ratio壮苗指数
seedling index5 0(CK1) 10.67±0.35 ab 0.28±0.02 a 8.37±0.32 de 12.99±1.00 b 0.12±0.02 a 0.69±0.03 a 0(CK2) 9.93±0.40 b 0.23±0.02 b 7.90±0.46 e 12.35±0.73 b 0.07±0.02 c 0.48±0.04 b 0.01 11.57±0.80 a 0.28±0.03 a 9.70±0.10 b 15.19±1.60 a 0.09±0.00 bc 0.52±0.03 b 0.05 10.63±0.85 ab 0.27±0.03 a 11.83±0.21 a 16.33±0.62 a 0.09±0.01 b 0.50±0.09 b 0.1 10.37±0.65 b 0.21±0.02 bc 9.17±0.29 c 11.25±1.32 bc 0.08±0.01 bc 0.48±0.01 b 0.5 8.43±0.32 c 0.17±0.01 c 8.60±0.17 d 9.89±0.18 c 0.08±0.00 bc 0.53±0.04 b 10 0(CK1) 10.87±0.10 b 0.29±0.03 ab 12.00±1.13 a 17.31±0.55 a 0.20±0.02 a 0.61±0.01 a 0(CK2) 10.23±0.25 c 0.26±0.02 bc 8.90±0.36 b 13.29±1.45 b 0.08±0.04 c 0.42±0.06 b 0.01 11.77±0.21 a 0.33±0.02 a 9.17±0.58 b 16.65±0.34 a 0.12±0.00 bc 0.50±0.07 ab 0.05 10.80±0.26 b 0.32±0.02 a 9.60±0.36 b 16.55±1.41 a 0.18±0.08 ab 0.44±0.04 b 0.1 10.47±0.15 bc 0.22±0.01 cd 9.33±1.26 b 12.26±0.32 b 0.09±0.03 c 0.43±0.09 b 0.5 10.27±0.25 c 0.20±0.01 d 9.50±0.50 b 12.18±1.06 b 0.10±0.01 c 0.41±0.05 b 注:同列同处理数值不同字母表示处理间差异达到0.05显著水平;表2、3同。
Note: Data with different letters on same column under same treatment indicate significant difference at level of 0.05. Same for below.2.2 外源SA对Cd胁迫下不结球白菜幼苗叶片光合色素的影响
从表2可以看出,Cd胁迫5 d和10 d,与CK1相比,CK2的不结球白菜幼苗叶片的叶绿素含量和类胡萝卜素含量均降低。Cd胁迫5 d,不同浓度SA处理均能提高幼苗叶片的叶绿素含量,以0.05 mmol·L−1SA处理的叶绿素含量和类胡萝卜素含量最高,其叶绿素a、叶绿素b和叶绿素(a+b)含量较CK2分别增加40.47%、117.28%和55.10%,类胡萝卜素含量增加36.30%。Cd胁迫10 d,0.01 mmol·L−1SA、0.05 mmol·L−1SA处理的幼苗叶片叶绿素含量和类胡萝卜素含量与CK1相比差异不显著。当SA浓度高于0.05 mmol·L−1,叶绿素含量、类胡萝卜素含量均下降。
表 2 外源SA对Cd胁迫下不结球白菜幼苗叶片光合色素的影响Table 2. Effect of exogenous SA on photosynthetic pigment in non-heading Chinese cabbage seedling leaves under Cd-stress处理时间
Processing time/dSA/(mmol·L−1) 叶绿素a
Chlorophyll a/(mg·g−1)叶绿素b
Chlorophyll b/(mg·g−1)叶绿素(a+b)
Total chlorophyll content/(mg·g−1)类胡萝卜素
Carotenoid/(mg·g−1)5 0(CK1) 0.43±0.01 de 0.16±0.00 c 0.59±0.01 c 0.12±0.01 ab 0(CK2) 0.42±0.01 e 0.10±0.01 e 0.52±0.01 d 0.10±0.00 c 0.01 0.59±0.00 a 0.21±0.01 a 0.80±0.01 a 0.13±0.01 a 0.05 0.56±0.01 b 0.18±0.01 b 0.74±0.03 b 0.12±0.02 ab 0.1 0.44±0.00 cd 0.15±0.01 c 0.59±0.00 c 0.11±0.01 bc 0.5 0.46±0.02 c 0.12±0.01 d 0.58±0.02 c 0.09±0.01 c 10 0(CK1) 1.06±0.01 a 0.35±0.03 a 1.41±0.04 a 0.28±0.00 ab 0(CK2) 0.97±0.01 b 0.28±0.01 b 1.25±0.01 b 0.24±0.01 c 0.01 1.09±0.01 a 0.35±0.01 a 1.44±0.02 a 0.27±0.02 b 0.05 1.06±0.02 a 0.35±0.02 a 1.40±0.02 a 0.30±0.01 a 0.1 0.84±0.02 c 0.26±0.00 bc 1.10±0.02 c 0.25±0.00 c 0.5 0.77±0.04 d 0.23±0.01 c 1.00±0.05 d 0.21±0.00 d 2.3 外源SA对Cd胁迫下不结球白菜幼苗根系活力、可溶性蛋白、脯氨酸和MDA含量的影响
2.3.1 外源SA对Cd胁迫下不结球白菜幼苗根系活力的影响
由图1可以看出,CK2的不结球白菜幼苗根系活力显著低于CK1;Cd胁迫5 d 和10 d,外源SA处理的幼苗根系活力均高于CK2;Cd胁迫5 d,0.05 mmol·L−1SA处理的根系活力较CK2显著增加29.44%;Cd胁迫10 d,0.01 mmol·L−1SA处理的根系活力最高,较CK2显著提高103.28%,但不同浓度SA处理之间差异不显著。
2.3.2 外源SA对Cd胁迫下不结球白菜幼苗叶片可溶性蛋白含量的影响
由图2可知,CK2的幼苗叶片可溶性蛋白含量低于CK1;Cd胁迫5 d,0.01 mmol·L−1SA、0.05 mmol·L−1SA处理的幼苗叶片可溶性蛋白含量显著高于各个处理,0.1 mmol·L−1SA、0.5 mmol·L−1SA处理的可溶性蛋白含量出现下降;Cd胁迫10 d,SA处理显著提高可溶性蛋白含量,以0.01 mmol·L−1SA处理的可溶性蛋白含量升高最多,较CK1和CK2分别增加44.45%和70.74%。
2.3.3 外源SA对Cd胁迫下不结球白菜幼苗叶片脯氨酸含量的影响
从图3可知,CK2的幼苗叶片脯氨酸含量均低于CK1;处理5 d后,0.01 mmol·L−1SA处理的脯氨酸含量与CK2差异不显著,0.05 mmol·L−1SA、0.1 mmol·L−1SA处理的脯氨酸含量显著高于各个处理,0.5 mmol·L−1SA处理显著低于其余处理;处理10 d后,0.01 mmol·L−1SA、0.05 mmol·L−1SA处理的脯氨酸含量显著高于其余处理,其中0.05 mmol·L−1SA处理较CK1和CK2分别提高29.96%和44.98%;而0.1 mmol·L−1SA、0.5 mmol·L−1SA处理的脯氨酸含量显著降低,与其余处理之间差异显著。
2.3.4 外源SA对Cd胁迫下不结球白菜幼苗叶片丙二醛含量的影响
由图4可知,Cd胁迫5 d,CK1的不结球白菜幼苗叶片MDA含量最低,但与CK2、0.01 mmol·L−1SA、0.05 mmol·L−1SA处理之间差异不显著;胁迫10 d后,CK2的幼苗叶片MDA含量上升幅度最大,较CK1显著增加68.83%;不同浓度SA处理均能降低幼苗叶片MDA含量,但含量仍显著高于CK1,其中0.01 mmol·L−1SA处理下降幅度最大,较CK2显著降低27.50%。
2.4 外源SA对Cd胁迫下不结球白菜幼苗叶片抗氧化酶活性的影响
从图5可以看出,CK2的不结球白菜幼苗叶片SOD、POD、CAT活性均低于CK1。Cd胁迫5 d,CK2的不结球白菜幼苗叶片SOD活性与0.5 mmol·L−1 SA处理相比差异显著,与其余处理之间差异不显著;Cd胁迫10 d,CK2的幼苗叶片SOD活性显著低于CK1,0.01 mmol·L−1SA、0.05 mmol·L−1SA处理的幼苗叶片SOD活性略有增加。
Cd胁迫5 d,0.01 mmol·L−1SA、0.05 mmol·L−1SA处理显著提高幼苗叶片POD活性,以0.01 mmol·L−1SA处理表现最好,而0.1 mmol·L−1SA、0.5 mmol·L−1SA处理POD活性下降;Cd胁迫10 d,0.05 mmol·L−1SA处理的幼苗叶片POD活性较CK2显著提高1.18倍,当SA浓度超过0.05 mmol·L−1POD活性出现下降。
Cd胁迫5 d,不同浓度SA处理均能提高幼苗叶片CAT活性,以0.01 mmol·L−1SA处理的CAT活性最高,与其余处理之间差异显著;Cd胁迫10 d,0.05 mmol·L−1SA、0.1 mmol·L−1SA处理叶片的CAT活性得到提高,其中0.05 mmol·L−1SA处理的CAT活性较CK2显著提高70.43%,与各处理之间差异显著;当SA超过0.05 mmol·L−1CAT活性出现下降。
2.5 外源SA对Cd胁迫下不结球白菜幼苗地上、地下部分Cd含量及转运系数的影响
由表3可知,不结球白菜幼苗地上部分Cd含量高于地下部分,CK2的不结球白菜幼苗地上、地下部分Cd含量显著高于其余处理,外源SA处理能显著降低幼苗体内Cd含量;Cd胁迫5 d,CK2的转运系数显著高于其余处理,转运系数随SA浓度的增加呈先降低后升高的趋势,其中0.05 mmol·L−1SA处理的转运系数最小。
表 3 外源SA对Cd胁迫下不结球白菜幼苗地上、地下部分Cd含量及转运系数的影响Table 3. Effect of exogenous SA on Cd Content and transport coefficient of aboveground and underground parts of non-heading Chinese cabbage seedlings under Cd-stress处理时间
Processing time/dSA/mmol·L−1 地上部分Cd含量
Cd content in above ground/(mg·kg−1)地下部分Cd含量
Cd content in underground part/(mg·kg−1)转运系数
Transport coefficient5 0(CK2) 483.33±7.02 a 215.97±4.80 a 2.24±0.02 a 0.01 319.03±5.67 c 185.97±4.28 b 1.72±0.07 c 0.05 251.87±3.48 e 167.53±4.28 d 1.50±0.03 d 0.1 269.23±3.00 d 175.37±4.11 c 1.54±0.02 d 0.5 334.87±4.45 b 174.40±4.75 cd 1.92±0.03 b 10 0(CK2) 677.70±2.33 a 397.73±3.00 a 1.70±0.01 b 0.01 534.33±3.52 c 348.10±2.98 c 1.54±0.02 c 0.05 503.47±2.34 d 375.77±4.98 b 1.34±0.02 d 0.1 594.07±4.44 b 338.67±4.77 d 1.75±0.04 a 0.5 598.13±3.44 b 350.77±3.31 c 1.71±0.02 b 3. 讨论与结论
3.1 外源SA对Cd胁迫下不结球白菜幼苗生长的影响
生物量是植物生长状况的直接反映,是确定其对环境耐性的重要指标之一[23]。本研究结果表明,Cd胁迫下不结球白菜幼苗生物量积累受到抑制,较CK1表现出下降趋势,其中根冠比下降幅度最大,说明根系生长受抑制程度最大;0.01~0.05 mmol·L−1 SA处理不结球白菜幼苗后,可以有效缓解Cd胁迫对不结球白菜幼苗生长的抑制作用,当SA浓度高于0.05 mmol·L−1,缓解效果减弱甚至表现出抑制作用,这可能是高浓度SA与Cd共同作用对不结球白菜幼苗根系产生了双重的毒害有关,这与任艳芳等[11]的研究结果一致。
3.2 外源SA对Cd胁迫下不结球白菜幼苗叶片光合色素的影响
叶绿素是植物进行光合作用时吸收和传递光能的主要色素,其含量高低不仅反映植物的光合能力强弱,亦能反映出植物在逆境下受伤害的程度[24]。本试验中,不结球白菜幼苗叶片叶绿素含量在Cd胁迫后显著下降,可能出现的原因:一是Cd2+在幼苗叶片细胞内积累后,取代叶绿素中的Zn2+、Mg2+、Fe2+,或与叶绿体中蛋白质上的-SH结合,导致叶绿体的结构和功能被破坏;二是叶绿素合成所必需的酶活性受抑,导致叶绿素合成受阻;三是活性氧和MDA的产生,致使叶绿素受到破坏[25]。0.01~0.05 mmol·L−1SA处理的幼苗叶片叶绿素含量和类胡萝卜素含量显著增加,说明外源SA通过提高幼苗叶片叶绿素含量来维持Cd胁迫下光合作用的正常进行,从而提高其对Cd胁迫的抗性,这与张永平等[26]的研究结果相一致。
3.3 外源SA对Cd胁迫下不结球白菜幼苗根系活力、可溶性蛋白、脯氨酸和丙二醛含量的影响
根系是植物吸收和合成的重要器官,根的生长状况和活力水平直接影响植株地上部的生长和营养吸收及产量高低,因此根系活力是衡量根系功能的重要指标[20]。本次试验中,CK2的不结球白菜幼苗根系活力显著低于CK1,可能是土壤中的Cd2+使根系受到损伤,导致根系活力下降,幼苗生长受抑;而SA处理的幼苗根系活力显著升高,说明喷施SA能够缓解Cd对不结球白菜幼苗的伤害,维持根系吸收和运输功能,促进植株生长,这与邵小杰等[27]的研究结果相似。
植物体内可溶性蛋白、脯氨酸在逆境胁迫下可作为渗透调节剂,通过调节渗透压,维持细胞内环境的稳定;当植物遇到逆境胁迫时,植物体内可溶性蛋白、脯氨酸的含量会迅速积累[28]。本研究结果表明,Cd胁迫下不结球白菜幼苗叶片的可溶性蛋白、脯氨酸含量表现出下降,可能是较高浓度的Cd2+抑制蛋白质的合成和脯氨酸的积累;外源SA处理后不结球白菜幼苗叶片的可溶性蛋白、脯氨酸含量显著升高,说明SA能促进Cd胁迫下不结球白菜幼苗叶片可溶性蛋白的合成和脯氨酸的积累,通过调节渗透压、维持细胞膜的稳定性,缓解Cd2+对膜的伤害,这与张芬琴等[29]的研究结果一致。
MDA是膜脂过氧化作用的主要产物,可与蛋白质、核酸等发生反应,干扰细胞内正常的生命活动,抑制植物生长发育,故MDA含量可以反映细胞膜脂过氧化水平和细胞膜受伤害程度[30]。本研究中,Cd胁迫10 d时,CK2的不结球白菜幼苗叶片MDA含量迅速上升,这可能是因为植物根系不断吸收Cd2+,导致Cd2+在植物体内富集量增加,从而对植物的伤害更为严重;外源SA均可降低不结球白菜幼苗叶片MDA含量,这与任艳芳等[11]的研究结果一致。证明外施SA能减轻Cd胁迫对膜的过氧化损伤,降低膜的透性,稳定膜的结构,促进Cd胁迫下幼苗的生长。
3.4 外源SA对Cd胁迫下不结球白菜幼苗叶片抗氧化酶活性的影响
SOD、POD、CAT是植物体内具有协同作用的抗氧化酶,在逆境胁迫下清除细胞内过量的活性氧,维持活性氧代谢的平衡,减轻逆境胁迫对植物细胞造成的伤害[31]。本试验发现,Cd胁迫下,不结球白菜幼苗叶片SOD、POD和CAT活性较CK1均有不同程度降低,可能是Cd2+诱导氧化毒害的主要原因[32]。适宜浓度的SA处理可提高不结球白菜幼苗叶片的抗氧化酶活性,Cd胁迫5 d时以0.01 mmol·L−1SA处理效果较佳,Cd胁迫10 d时0.05 mmol·L−1SA处理抗氧化酶活性最高,这与赵新月等[33]研究玉米在镉胁迫下喷施SA的最适宜浓度为 50~100 μmol·L−1的结果一致。本试验中,当SA浓度大于0.05 mmol·L−1,明显抑制不结球白菜幼苗叶片的酶活性,可能是因为高浓度的SA 降低相应的酶活性,说明SA只能在一定范围内对植物的抗氧化酶活性产生促进作用,超过这个范围将产生抑制作用。
3.5 外源SA对Cd胁迫下不结球白菜幼苗地上、地下部分Cd含量及转运系数的影响
通常情况下,植物通过将重金属截留于根系,减少重金属由根部向地上部分转运,从而减轻镉对地上部分的毒害[34]。本试验中,不结球白菜幼苗对Cd的吸收表现为地上部分>地下部分,说明不结球白菜幼苗从土壤中吸收的Cd主要积累于茎叶,向地上部茎叶中转移较多,这与任艳军等[35]的研究一致。外源SA处理可以显著降低不结球白菜幼苗地上、地下部分Cd含量,其中0.01 mmol·L−1SA、0.05 mmol·L−1SA处理能有效降低幼苗的转运系数,说明0.01~0.05 mmol·L−1SA处理的不结球白菜幼苗对重金属Cd的根际阻控效应较强,减少Cd向幼苗地上部分的转运。
综上所述,Cd胁迫会对不结球白菜幼苗生长造成伤害,添加外源SA可有效缓解Cd胁迫的伤害,本研究结果认为SA为0.05 mmol·L−1时,不结球白菜幼苗的根长、根冠比最高,同时能显著提高幼苗脯氨酸含量和POD、CAT活性,降低不结球白菜幼苗地上部分的Cd累积量,提高不结球白菜幼苗的抗Cd能力。
-
表 1 新白8号果实香气主要成分的相对含量
Table 1 Relative content of aromatics in fruits of Xinbai 8
编号
No.化学成分
Components相对含量Relative content/(ng·g-1 FW) ×1环己酮
Cyclohexanone×10环己酮
Cyclohexanone×100环己酮
Cyclohexanone×1000环己酮
Cyclohexanone酯类Esters 1 2-甲基丁酸甲酯methyl 2-methylbutyrate - - - 0.10 2 甲酸环己酯Formic acid, cyclohexyl ester 901.57 84.85 18.76 - 3 乙酸环己酯Acetic acid, cyclohexyl ester - 3.37 0.56 - 4 顺式-3-己烯醇乳酸酯cis-3-Hexenyllactate 36.35 - - - 醇类Alcohol 5 1-甲基环己醇1-MethyLcyclohexanol 339.30 49.95 6.77 0.35 6 正己醇1-Hexano 178.37 85.49 17.66 2.94 7 (Z)-3-己烯醇3-Hexen-1-ol, (E)- 52.04 22.05 4.55 0.52 8 (E)-2-己烯-1-醇2-Hexen-1-ol, (E)- - 141.39 34.64 5.32 9 2-乙基己醇1-Hexanol, 2-ethyl- 57.17 8.45 2.08 0.36 10 正辛醇1-Octanol 48.93 11.68 2.10 0.34 11 新薄荷醇(1R)-(+)-neomenthol - - 5.28 - 12 戊乙二醇Pentaethylene glycol 98.08 38.10 0.78 0.20 酮类Ketones 13 3-庚酮3-Heptanone 331.77 38.12 5.44 - 14 2-庚酮2-Heptanone 8144.71 503.82 65.1 1.93 15 环戊基乙酮Ethanone, 1-cyclopentyl- 96.90 10.76 1.49 - 16 2-甲基环戊酮Cyclohexanone, 2-methyL- 634.71 72.03 8.41 - 17 甲基庚烯酮5-Hepten-2-one, 6-methyL- 78.23 16.85 2.98 0.34 18 2-环己烯酮2-CycLohexen-1-one 415.65 22.48 3.48 0.51 19 苯乙酮Acetophenone - 3.50 0.52 0.14 20 1.4-环己二酮2-Cyclohexene-1, 4-dione - - 1.10 0.23 21 香叶基丙酮Geranylacetone - 12.46 2.60 - 22 β-紫罗酮Beta-Ionone 168.23 12.12 2.47 0.69 烷烃Alkane 23 正丁基环己烷Cyclohexane, butyl- 19873.41 278.97 156.65 0.48 24 正戊基环己烷Cyclohexane, pentyl- 15890.51 207.81 104.70 0.93 25 环十二烷Cyclododecane - 4.38 0.70 0.18 醛类Aldehyde 26 己醛Hexanal 4908.29 1295.02 301.00 74.94 27 (E)-2-己烯醛2-HexenaL, (E)- 7896.42 1569.74 382.22 55.98 28 环己基甲醛Cyclohexane carboxaldehyde 111.95 8.48 1.86 - 29 壬醛Nonanal 228.65 34.57 6.01 1.12 30 (E.E)-2.4-庚二烯醛2, 4-Hexadienal, (E, E)- 580.28 23.18 6.58 1.12 31 癸醛Decanal 126.22 16.45 2.37 0.70 32 苯甲醛Benzaldehyde 148.86 10.08 2.54 0.51 33 β-环柠檬醛Beta-cyclocitral - 5.92 0.97 0.22 酸类Acid 34 乙酸Acetic acid 70.98 4.96 1.11 0.28 35 2-甲基丁酸Butanoic acid, 2-methyl- - 4.72 1.37 0.35 36 己酸Hexanoic acid 201.78 20.25 5.81 1.50 37 (E)-2-己烯酸2-Hexenoic acid, (E)- - 30.07 5.74 1.71 酚类Phenol 38 2, 6-二叔丁基对甲酚Butylated hydroxytoluene - 43.68 5.89 2.89 醚类Ether 39 三乙二醇单乙醚Ethanol, 2-(2-ethoxyethoxy)- 398.08 4.19 9.78 2.20 芳香烃Aromatic hydrocarbon 40 苯乙烯Styrene 3442.55 111.46 20.67 0.62 41 乙苯Ethylbenzene 2264.31 43.77 14.90 - 42 对二甲苯p-Xylene 17089.28 249.82 15.61 - 其他Others 43 2-乙基呋喃Furan, 2-ethyl- - 15.09 1.97 0.11 相对总含量The relative total content 84813.58 5120.08 1235.22 160.81 累计有效峰面积All of effective peak area 7.37×109 4.18×109 3.99×109 1.58×109 有效峰面积/总峰面积 38.20% 28.49% 42.70% 39.51% The proportion of effective and total peak area 环己酮峰面积The peak area of cyclohexanone 9.14×109 8.58×109 3.40×109 1.06×109 注:“-”表示未检测到。
Note:“-” indicates undetected. -
[1] OLUWAFEMI J, CALEB O A, FAWOLE R R, et al.Impact of preharvest and postharvest factors on changes in volatile compounds of pomegranate fruit and minimally processed arils-Review[J].Scientia Horticulturae, 2015, 188. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=47f1865a8f11f91892d4389fd03e4283
[2] 陈薇薇, 孙海艳, 蒋赟等.枇杷香气成分固相微萃取条件的正交试验优化[J].食品科学, 2015, 36(24):35-39. DOI: 10.7506/spkx1002-6630-201524006 CHEN W W, SUN H Y, JIANG Y, et al.Orthogonal Array Optimization of Solid Phase Micro-Extraction Conditions for Loquat Aroma Compounds[J].Food Science, 2015, 36(24):35-39.(in Chinese) DOI: 10.7506/spkx1002-6630-201524006
[3] 清扬.又白, 又大, 又早——福建省农科院培育出系列特早熟枇杷新品种[J].果农之友, 2018(5):46-47. DOI: 10.3969/j.issn.1671-7759.2018.05.022 QING Y.White, large and early-A series of new varieties of loquat developed by Fujian Academy of Agricultural Sciences[J].Fruit Growers' Friend, 2018(5):46-47.(in Chinese) DOI: 10.3969/j.issn.1671-7759.2018.05.022
[4] 谢丽雪, 许家辉, 张立杰, 等. 24份白肉枇杷种质资源的ISSR分析[J].福建农业学报, 2012, 27(3):261-266. DOI: 10.3969/j.issn.1008-0384.2012.03.011 XIE L X, XU J H, ZHANG L J, et al.Genetic Relationship Analysis of 24 White-fleshed Loquat (Eriobotrya japonica)Germplasms by ISSR[J].Fujian Journal of Agricultural Sciences, 2012, 27(3):261-266.(in Chinese) DOI: 10.3969/j.issn.1008-0384.2012.03.011
[5] 郑少泉, 蒋际谋, 许家辉, 等.优质大果晚熟白肉枇杷新品系——新白1号、新白3号、新白8号[J].福建农业学报, 2006, 21(1):48-50. DOI: 10.3969/j.issn.1008-0384.2006.01.013 ZHENG S Q, JIANG J M, XU J H, et al.New white flesh loquat strains Xinbai 1, Xinbai 3 and Xinbai 8 with large-type, high-quality and late-ripening traits[J].Fujian Journal of Agricultural Sciences, 2006, 21(1):48-50.(in Chinese) DOI: 10.3969/j.issn.1008-0384.2006.01.013
[6] 李俊星, 钟玉娟, 罗剑宁, 等.基于顶空固相微萃取结合气相色谱-质谱技术分析香芋南瓜叶片的香气物质成分及特征[J].浙江大学学报(农业与生命科学版), 2019, 45(2):1-5. http://d.old.wanfangdata.com.cn/Periodical/zjdxxb-nyysm201902006 LI J X, ZHONG Y J, LUO J N, et al.Detection of volatile flavor compounds in leaf of Xiangyu pumpkin using headspace solid-phase microextraction-gas chromatography-mass spectrometry[J]. Journal of Zhejiang University (Agriculture & Life Sciences), 2019, 45(2):1-5.(in Chinese) http://d.old.wanfangdata.com.cn/Periodical/zjdxxb-nyysm201902006
[7] 李健隽.面积归一化法分析混合气体中各组分含量[J].计量与测试技术, 2012, 39(4):86, 88. DOI: 10.3969/j.issn.1004-6941.2012.04.046 LI J J.Analysis the Content of Each Component in Mixed Gas with Area Normalization Method[J].Metrology and Measurement Technique, 2012, 39(4):86, 88.(in Chinese) DOI: 10.3969/j.issn.1004-6941.2012.04.046
[8] 李好枝.体内药物分析[M].北京:中国医药科技出版社, 2011:212-214. LI H Z.Biopharmaceutical Analysis[M].Beijing:China Medical Science Press, 2011:212-214.(in Chinese)
[9] 张沛宇, 刘珞忆, 陈婷婷, 等.'奥林达'夏橙主要香气成分在贮藏保鲜过程中的变化[J].果树学报, 2018, 35(7):859-869. http://www.cnki.com.cn/Article/CJFDTotal-GSKK201807011.htm ZHANG P Y, LIU L Y, CHEN T T, et al.The variations in major aroma compounds in 'Olinda' Valencia orange(Citrus sinensis)during storage[J].Journal of Fruit Science, 2018, 35(7):859-869.(in Chinese) http://www.cnki.com.cn/Article/CJFDTotal-GSKK201807011.htm
[10] 吴文艳, 陈健乐, 陈荣荣, 等.HS-SPME-GC/MS结合PCA分析不同成熟度东魁杨梅香气组分差异[J].中国食品学报, 2017, 17(12):236-242. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgspxb201712030 WU W Y, CHEN J L, CHEN R R, et al.Volatiles of Chinese Bayberry during Different Using HS-SPME-GC/MS Combined with PCA[J].Journal of Chinese Institute of Food Science and Technology, 2017, 17(12):236-242.(in Chinese) http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgspxb201712030
[11] 王玲, 尹克林.'达赛莱克特''草莓果实发育成熟过程中香气物质的变化及其特征成分的确定[J].果树学报, 2018, 35(4):433-441. http://d.old.wanfangdata.com.cn/Periodical/dzxwxb200905010 WANG L, YIN K L.Changes in aroma of 'Darselect' strawberry during development and characterization of the key aroma components[J].Journal of Fruit Science, 2018, 35(4):433-441.(in Chinese) http://d.old.wanfangdata.com.cn/Periodical/dzxwxb200905010
[12] 张义, 高蓓, 徐玉娟, 等.顶空固相微萃取-气质联用方法分析龙眼中的挥发性化合物[J].食品科学, 2010, 31(16):156-160. http://d.old.wanfangdata.com.cn/Periodical/spkx201016032 ZHANG Y, GAO B, XU Y J, et al.Determination of Volatile Compounds in 'Chuliang' Longan Using Headspace Solid-phase Microextraction and GC-MS[J].Food Science, 2010, 31(16):156-160.(in Chinese) http://d.old.wanfangdata.com.cn/Periodical/spkx201016032
[13] 涂俊凡, 秦仲麒, 李先明, 等.砂梨和库尔勒香梨果实香气物质的GC-MS分析[J].湖北农业科学, 2011, 50(15):3186-3190. DOI: 10.3969/j.issn.0439-8114.2011.15.049 TU J F, QIN Z Q, LI X M, et al.Analysis of Fruit Aromatic Components of Pyrus pyrifolia Nakai and P.sinkiangensis yü by GC-MS[J].Hubei Agricultural Sciences, 2011, 50(15):3186-3190.(in Chinese) DOI: 10.3969/j.issn.0439-8114.2011.15.049
[14] 乌云塔娜, 蒋贺喜格, 康秀.中国秋子梨品种果实香气成分比较分析[J].中国南方果树, 2015, 44(3):103-107. http://d.old.wanfangdata.com.cn/Periodical/zgnfgs201503025 WU Y T N, JING H X G, KANG X.Comparative analysis of aroma components in Pyrus ussuriensis fruit[J].South China Fruits, 2015, 44(3):103-107.(in Chinese) http://d.old.wanfangdata.com.cn/Periodical/zgnfgs201503025
[15] 慈志娟, 田利光, 张序, 等.脱毒'烟富3号'与未脱毒'烟富3号'苹果香气成分差异分析[J].中国果树, 2019(2):50-52. http://d.old.wanfangdata.com.cn/Periodical/zhongggs201902012 CI Z J, TIAN L G, ZHANG X, et al.Analysis on the difference of aroma components between virus-free Yanfu 3 and non-detoxified Yanfu 3 apple[J].China Fruits, 2019(2);50-52.(in Chinese) http://d.old.wanfangdata.com.cn/Periodical/zhongggs201902012
[16] 丰珂珏, 刘琼琼, 杨晓萍.枇杷花袋泡茶香气特征及挥发性成分分析[J].湖北农业科学, 2014, 53(15):3582-3587. DOI: 10.3969/j.issn.0439-8114.2014.15.031 FENG K Y, LIU Q Q, YANG X P.Analyzing Aroma Characteristics and Volatile Components of Loquat Flower Tea-bag[J].Hubei Agricultural Sciences, 2014, 53(15):3582-3587.(in Chinese) DOI: 10.3969/j.issn.0439-8114.2014.15.031
[17] 芦艳, 鲁周民, 樊美丽, 等.枇杷花开放过程挥发性物质变化研究[J].园艺学报, 2013, 40(11):2245-2254. DOI: 10.3969/j.issn.0513-353X.2013.11.017 LU Y, LU Z M, FAN M F, et al.Changes of Volatile Components During Different Stages of Loquat Flowers[J].Acta Horticulturae Sinica, 2013, 40(11):2245-2254.(in Chinese) DOI: 10.3969/j.issn.0513-353X.2013.11.017
[18] 袁婷, 陈薇薇, 孙海艳, 等.不同果肉类型枇杷果肉挥发性成分分析[J].食品科学, 2018, 39(24):209-217. DOI: 10.7506/spkx1002-6630-201824032 YUAN T, CHEN W W, SUN H Y, et al. Analysis of the Volatile Components in Loquats with Different Flesh Colors[J].Food Science, 2018, 39(24):209-217.(in Chinese) DOI: 10.7506/spkx1002-6630-201824032
[19] BESADA C, SALVADOR A, SDIRI S, et al.A combination of physio logical and chemometrics analyses reveals the main associations between quality and ripening traits and volatiles in two loquat cultivars[J].Metabolomics, 2013, 9(2).324-336. DOI: 10.1007/s11306-012-0447-z
[20] 张巧, 顾欣哲, 吴永进, 等.枇杷果皮热风干燥前后功能性成分含量变化与挥发性成分分析[J].食品科学, 2016, 37(16):117-122. DOI: 10.7506/spkx1002-6630-201616019 ZHANG Q, GU X Z, WU Y J, et al.Analysis of Functional Components and Volatile Components from Loquat Peel Before and After Hot-Air Drying[J].Food Science, 2016, 37(16):117-122.(in Chinese) DOI: 10.7506/spkx1002-6630-201616019
[21] 吴霏霏.枇杷果实香气检测及AAT1基因克隆表达与酶活性分析研究[D].扬州: 扬州大学, 2015. http://cdmd.cnki.com.cn/Article/CDMD-11117-1015664764.htm WU F F.Aroma analysis and AAT1 gene cloning and expression and enzyme activity detection of loquat fruit[D].Yangzhou: Yangzhou University, 2015.(in Chinese) http://cdmd.cnki.com.cn/Article/CDMD-11117-1015664764.htm
[22] 胡文舜, 蒋际谋, 黄爱萍, 等.'晚香'龙眼果实香气成分的3种萃取头GC-MS效果分析[J].福建农业学报, 2015, 30(12):1149-1154. DOI: 10.3969/j.issn.1008-0384.2015.12.004 HU W S, JIANG J M, HUANG A P, et al.GC-MS Analysis on Aromatics of Wanxiang Longans Using Different Extraction Fibers[J].Fujian Journal of Agricultural Sciences, 2015, 30(12):1149-1154.(in Chinese) DOI: 10.3969/j.issn.1008-0384.2015.12.004
[23] 蒋际谋, 胡文舜, 许奇志, 等.枇杷品种香甜和解放钟及两者杂交子代优系果实香气成分分析[J].植物遗传资源学报, 2014, 15(4):894-900. http://d.old.wanfangdata.com.cn/Periodical/zwyczyxb201404032 JIANG J M, HU W S, XU Q Z, et al.Volatiles in Fruits of Two Loquat Cultivars Xiangtian, Jiefang zhong and Their Two Offspring Selections[J].Journal of Plant Genetic Resources, 2014, 15(4):894-900.(in Chinese) http://d.old.wanfangdata.com.cn/Periodical/zwyczyxb201404032
[24] 梁乘榜.枇杷果实品质分析及CCD1基因克隆与表达研究[D].扬州: 扬州大学, 2013. http://cdmd.cnki.com.cn/Article/CDMD-11117-1014112830.htm LIANG C B.Quality analysis and CCD1 gene cloning and expression of loquat (Eriobotrya japonica) fruit[D].Yangzhou: Yangzhou University, 2013.(in Chinese) http://cdmd.cnki.com.cn/Article/CDMD-11117-1014112830.htm
-
期刊类型引用(7)
1. 陈珣,肇莹,龚娜,刘国丽,马晓颖,张敏,肖军. 基于响应面法优化滑菇液体菌种发酵培养基配方. 南方农业学报. 2024(12): 3625-3635 .  百度学术
百度学术
2. 王焱,王竟夷,黄亮,班立桐,李奕葶,党红慧,王玉. 双孢蘑菇液体菌种固态化工艺的初步研究. 食品与发酵科技. 2021(01): 24-28+74 .  百度学术
百度学术
3. 尹川,杜冰冰,连洁,张弘扬,黄亮,班立桐,王玉. 气升式反应器中通气量和pH对双孢蘑菇液体菌种的影响. 食品与发酵科技. 2021(02): 35-39 .  百度学术
百度学术
4. 曾志恒,曾辉,蔡志欣,郭仲杰,卢园萍,陈美元,廖剑华,戴建清. 双孢蘑菇新型颗粒原种配方的优化. 生物技术通报. 2021(11): 134-141 .  百度学术
百度学术
5. 陈晨伟,丁榕,彭柳城,谢晶,杨福馨,杨新宇,于千惠. 外源营养物对菌丝体生物质材料的生长研究及其性能表征. 农业工程学报. 2021(21): 295-302 .  百度学术
百度学术
6. 曾志恒,曾辉,程翊,杨雷,施肖堃,戴建清. 双孢蘑菇发酵液还原糖和总糖的含量测定. 中国食用菌. 2018(06): 40-43+49 .  百度学术
百度学术
7. 林金盛,蒋宁,李辉平,侯立娟,曲绍轩,张晓华,马林. 工厂化袋栽杏鲍菇液体菌种制作与应用. 山西科技. 2017(06): 143-145 .  百度学术
百度学术
其他类型引用(2)




 下载:
下载: