A New Multiplex PCR Assay for Simultaneously Detecting Mycoplasma ovipneumoniae and Corynebacterium pseudotuberculosis in Diseased Goats and Sheep
-
摘要:目的 为实现临床上对绵羊肺炎支原体(Mycoplasma ovipneumoniae, Mo)和山羊伪结核棒状杆菌(Corynebacterium pseudotuberculosis, CP)两种病原混合感染的同时检测,建立Mo和CP的双重PCR检测方法。方法 应用基于Mo的P80基因和CP的PLD基因设计两对特异性引物,对反应体系和条件进行优化,验证方法的特异性、灵敏性和重复性;应用该方法和单一PCR方法对临床收集的70份样品进行检测,比较检测结果。结果 建立的Mo和CP的双重PCR检测方法能够同时扩增出Mo 700 bp和CP 290 bp左右的片段,而对其他羊病常见病原的DNA扩增均为阴性。Mo和CP的检测下限分别为1 530 pg·μL−1和3 500 pg·μL−1。该方法具有良好的重复性。临床样品检测结果显示:70份临床样品中Mo阳性率为25.71%,CP阳性率为18.57%,同时感染Mo和CP阳性率为7.14%,与单一PCR检测结果符合率为100%。结论 本研究建立的双重PCR检测方法具有特异性强、灵敏性较高、重复性好等特点,为临床上Mo和CP混合感染的快速检测以及流行病学调查提供了实用方法。Abstract:Objective To establish a multiplex PCR method for simultaneous clinic detection of Mycoplasma ovipneumoniae (Mo), one of the main pathogens causing Mycoplasma pneumonia of goats and sheep(MPGS), and Corynebacterium pseudotuberculosis (CP), the pathogen of goat pseudotuberculosis, in the livestock animals infected by both pathogens at a same time.Method Two pairs of specific primers were designed based on the P80 gene of Mo and the PLD gene of CP for the PCR. After optimizing the detection system and reaction conditions, the specificity, sensitivity, and repeatability of the new method were verified for methodology validation. The results obtained using two separate PCR and the multiplex PCR on 70 clinical specimens were comparatively analyzed.Result The newly developed multiplex PCR method amplified a 700 bp fragment from Mo and a 290 bp fragment from CP, with none from other common pathogens of goats and sheep. The method had a detection limit of 1 530 pg·μL−1 on Mo and 3 500 pg·μL−1 on CP with a high repeatability. A test on 70 clinical specimens using the new method yielded a 25.71% positive rate on Mo, 18.57% on CP, and 7.14% on Mo/CP infections. Its coincidence rate with the two single PCR results was 100%.Conclusion The newly established multiplex PCR detection methodology exhibited high specificity, sensitivity, and reproducibility. It appeared to be applicable for rapid and simultaneous clinic detection on Mo and CP as well as epidemiological studies on the disease infected by the pathogens.
-
0. 引言
【研究意义】绵羊肺炎支原体(Mycoplasma ovipneumoniae, Mo)是引起绵羊和山羊支原体性肺炎(Mycoplasma pneumonia of goats and sheep, MPGS)的一种经呼吸道传染的病原[1]。MPGS患病羊主要表现为肺炎、咳嗽、流鼻涕、体温升高、摄食量下降、腹泻便秘、精神状态恶化和生长发育迟缓等症状[2-3]。该病一年四季都会发生,冬春季节多发,发病率30%~50%[4-7],主要在甘肃、安徽、山东、四川、贵州、福建等地流行[8]。山羊伪结核棒状杆菌(Corynebacterium pseudotuberculosis, CP)是山羊伪结核病的病原,山羊伪结核病是一种人畜共患的接触性传染病[9],也称为干酪样淋巴结炎(Caseous lymphadenitis, CLA)。患病羊主要表现为消瘦、体温升高、食欲减退、生产性能降低,孕畜出现流产、死胎、畸胎等现象[10]。其发病率一般在8.36%~30%[11-12],一年四季均可发病[13],且患病率随年龄增大而升高[14]。目前在世界范围内广泛流行,我国内蒙古、陕西、贵州、新疆、云南和广东等地区均有该病发生的报道[15-16]。但是,临床上内脏型山羊伪结核病临床症状不明显,容易被忽视从而耽误治疗。为了解临床上是否存在Mo和CP混合感染,建立一种同时检测两种病原的PCR方法对上述两种病的监测和防控具有重要意义。【前人研究进展】在Mo和CP两种病原的检测方面,已经建立的方法有PCR、荧光定量PCR、血清学检测方法等。韩瑞鑫等[17]建立了检测Mo的TaqMan实时荧光定量PCR;林裕胜等[18]建立了Mo RPA;王娟等[19]建立了Mo恒温热隔绝式PCR;张双翔等[20]建立了Mo LAMP;赵萍等[21]建立了Mo间接ELISA;马玉馨等[13]建立了CP TaqMan荧光定量PCR;许国洋等[22]建立了CP PMA-PCR;郑敏等[23]、韦志锋等[24]和朱伟英等[25]建立CP PCR;王韡等[26]建立了CP ELISA。【本研究切入点】以上检测方法均为Mo或CP的单一检测方法,相比于同时检测CP和Mo病原的方法效率低。但国内尚未见同时检测CP和Mo 的双重PCR方法相关研究。【拟解决的关键问题】本研究建立Mo和CP双重PCR检测方法可用于临床样品中Mo和CP单一或混合感染的快速检测,为MPGS和羊伪结核病的快速诊断及流行病学调查提供实用方法。
1. 材料与方法
1.1 菌株及临床样品
大肠杆菌(Escherichia coli, Ec)、沙门氏杆菌(Salmonella enteriditis, SE)、金黄色葡萄球菌(Staphylococcus aureus, SA)由福建省农业科学院畜牧兽医研究所禽病研究室和猪病研究室馈赠;山羊支原体山羊亚种(Mycoplasma capricolum subsp. capricolum, Mcc)、山羊支原体山羊肺炎亚种(Mycoplasma capricolum subsp. capripneumoniae, Mccp)由中国农业科学院兰州兽医研究所馈赠;伪结核棒状杆菌(Corynebacterium pseudotuberculosis, CP)[27]、绵羊肺炎支原体(Mycoplasma ovipneumoniae, Mo)[28]、丝状支原体山羊亚种(Mycoplasma mycoides subsp. Capri, Mmc)[29]、山羊莱氏无胆甾原体(Acholeplasma laidlawii, AL)[30]、牛支原体(Mycoplasma bovis, Mb)[31]为本研究室分离、鉴定、保存。70份临床样品于2018年4月至2019年7月采集自福建省三明市(鼻拭子10份、肺组织9份)、宁德市(鼻拭子13份、肺组织7份)和福州市(鼻拭子20份、肺组织11份)的临床上有不同程度流鼻涕、咳嗽、消瘦的病羊。
1.2 主要试剂
LB培养基和DNA提取试剂盒购于生工生物工程(上海)有限公司;改良Frey氏培养基为青岛高科技园海博生物技术有限公司产品;Premix Taq(Ex Taq Version 2.0 plus dye)、DL2000 Marker等购自宝生物工程(大连)有限公司。
1.3 引物设计
Mo特异性引物F1/R1参照林裕胜等[32]设计;CP特异性引物F2/R2的设计参照许国洋等[22],由铂尚生物技术(上海)有限公司合成,其序列如表1。
表 1 引物序列Table 1. Primer sequence靶基因
Target gene引物名称
Primer name引物序列(5′→ 3′)
Primer sequence(5′→ 3′)扩增片段大小
Amplified fragment size/bpP80基因 F1 GCCTTGGGGTTGGAATTCCTTTGTCTTATTC 705 R1 CATTTGATGCTGAGGTCGGATTTGGACTAAC PLD基因 F2 GTGAGAAGAACCCCGGTATAAG 291 R2 TACCGCACTTATTCTGACACTG 1.4 细菌和支原体核酸的提取
细菌DNA和支原体DNA的提取及浓度测定参考林裕胜等[32]的方法。
1.5 单一PCR反应体系的建立及克隆测序
Mo和CP的单一PCR扩增体系均为20 μL:Premix Taq(Ex Taq Version 2.0 plus dye)10 μL,上、下游引物(10 μmol·L−1)各1 μL,DNA模板2 μL,ddH2O补足至20 μL。PCR反应程序为:94℃预变性5 min;94℃变性45 s,55℃退火45 s,72℃延伸1 min,30个循环;72℃终延伸10 min,4℃保存。经1%琼脂糖凝胶电泳检测PCR产物大小。将Mo和CP的单一PCR扩增产物交铂尚生物技术(上海)有限公司进行克隆测序,将获得的DNA序列与GenBank中的基因序列进行比对。
1.6 双重PCR体系优化
在Mo和CP单一PCR反应的基础上,分别对双重PCR体系中的引物浓度和退火温度进行优化。以Mo和CP混合DNA为模板。优化引物浓度时:两对特异性引物浓度均为10 μmol·L−1,双重 PCR 反应体系20 μL:Premix Taq(Ex Taq Version 2.0 plus dye)10 μL,混合DNA模板2 μL,引物分别为0.7、0.8、0.9、1.0、1.1、1.2 和1.3 μL,ddH2O补足至20 μL;PCR反应程序为:94℃预变性5 min;94℃变性45 s,55℃退火45 s,72℃延伸45 s,30个循环;72℃终延伸10 min,对PCR产物进行1%琼脂糖电泳分析,以确定最佳引物浓度。优化退火浓度时:设置7个温度:51、53、55、57、59、61和63℃,每个温度组加入已优化的引物量,其余条件固定不变进行双重PCR反应,反应结束后经1%琼脂糖凝胶电泳观察结果,以确定最佳退火温度。
1.7 双重PCR特异性试验
分别以Mo+CP、CP、Mo、Mmc、Mcc、Mccp、AL、Mb、SE、Ec、SA的DNA为模板,以ddH2O作为空白对照,按照优化后的双重PCR反应条件进行检测。反应结束后进行1%琼脂糖凝胶电泳观察结果。
1.8 双重PCR灵敏性试验
将已测定浓度的Mo和CP DNA,用ddH2O进行梯度稀释,稀释倍数分别为101、102、103、104、105、106、107、108。分别取2 μL各稀释度的Mo、CP 和Mo+CP的DNA进行单一和双重PCR反应,扩增体系和扩增条件同1.5和1.7,测定该方法的灵敏性。
1.9 双重PCR重复性试验
组内重复试验:取1份Mo+CP、4份Mo、5份CP的DNA样品,以Mccp、Mmc、AL、Ec、SA、SE的DNA样品各1份作阴性对照,以ddH2O作空白对照,每一份样品3个重复,进行双重PCR 扩增试验,扩增体系和扩增条件同1.7;组间重复试验:以上17份样品每间隔3 d分别用双重PCR方法检测1次,共检测3次,PCR扩增体系和扩增条件均同1.7。
1.10 临床样品检测试验
以DNA抽提试剂盒提取70份自福建省不同地区采集的临床样品的DNA,以此DNA为模板进行CP、Mo、Mo+CP检测,重复3次,具体试验方法参考林裕胜等[32]方法。
2. 结果与分析
2.1 Mo和CP单一PCR扩增及扩增产物的鉴定
应用基于Mo的P80基因和CP的PLD基因所设计的2对特异性引物,按照单一PCR反应体系分别进行PCR反应,将扩增得到的目的片段经1%琼脂糖凝胶电泳。电泳结果显示,Mo仅扩增出一条约700 bp左右的目的片段(图略),CP仅扩增出一条约290 bp左右的目的片段(图略),二者均与预期片段大小相符。克隆测序结果显示,所克隆的Mo序列为705 bp,与参考株(GenBank No. KF703747.1)序列同源性为100%;克隆的CP序列为291 bp,与GenBank中收录的山羊(GenBank No. CP039866.1)和绵羊(GenBank No. CP001829.1)伪结核棒状杆菌同源性均为100%。
2.2 双重PCR体系优化结果
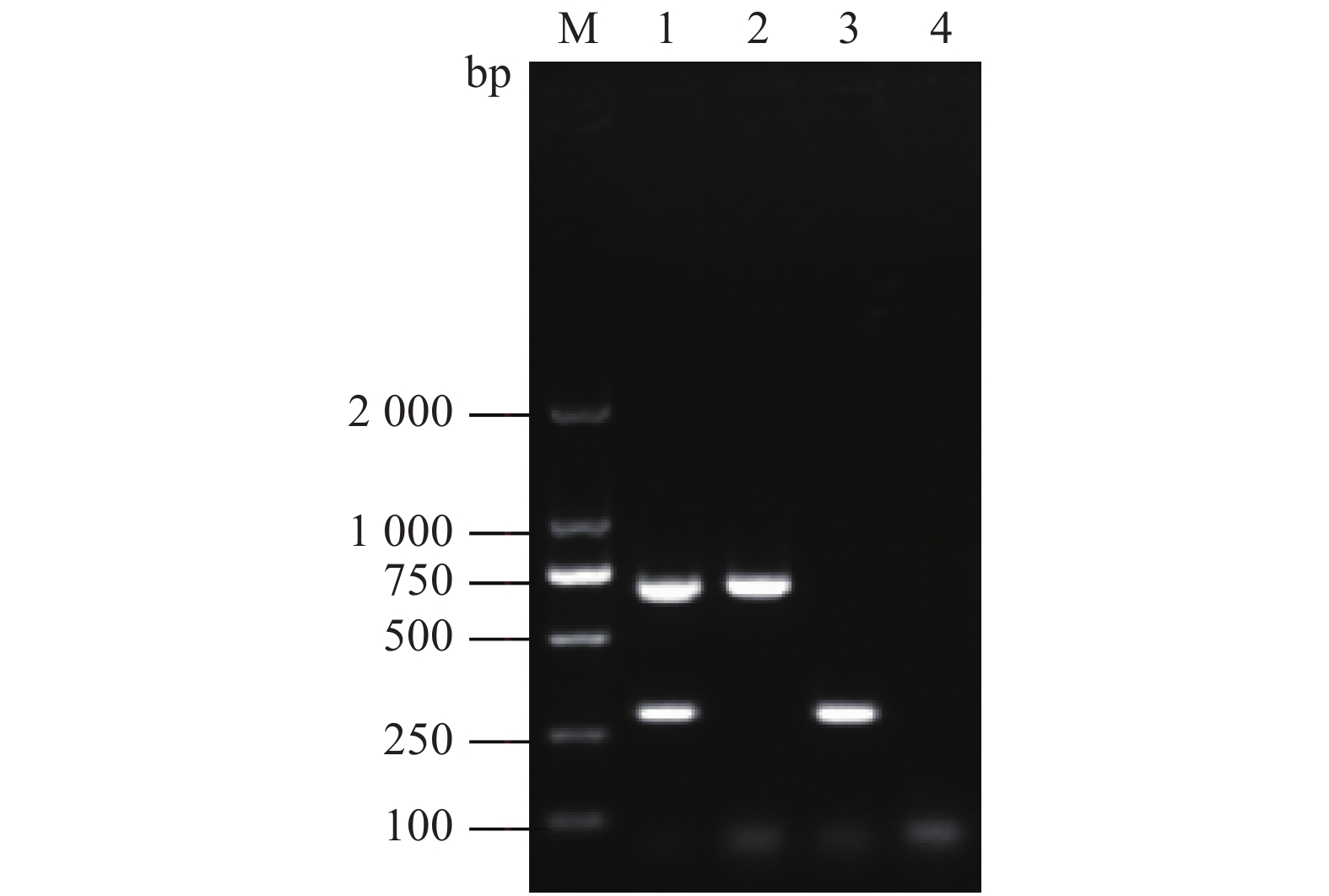
经过双重PCR体系优化,确定最佳反应体系为:总体积20 μL,Premix Taq(Ex Taq Version 2.0 plus dye)10 μL,上、下游两对特异性引物(10 μmol·L−1)各1 μL,Mo和CP的DNA混合模板2 μL,ddH2O补足至20 μL;最佳反应程序为:94℃ 5 min;94℃ 45 s,61℃ 45 s,72℃ 45 s,30个循环;72℃ 10 min。以Mo+CP、Mo、CP的 DNA为模板,以Mccp为阴性对照,进行双重PCR扩增。电泳结果显示,Mo+CP混合DNA样品同时扩增出与预期大小相符的约700 bp和290 bp的两个片段,Mo和CP单一DNA分别扩增出约为700 bp和290 bp的单一片段,而阴性对照无条带(图1)。
2.3 双重PCR特异性试验结果
采用优化的双重PCR扩增条件,以Mo+CP、CP、Mo、Mmc、Mcc、Mccp、AL、Mb、SE、Ec、SA的DNA为模板进行PCR扩增,以ddH2O作为空白对照。结果显示,只有Mo+CP、CP、Mo的DNA样品扩增出与预期大小一致的特异性片段,而Mmc、Mcc、Mccp、AL、Mb、SE、Ec、SA、和ddH2O均未扩增出目的片段(图2),表明本研究建立的双重PCR方法特异性好。
2.4 双重PCR灵敏性试验结果
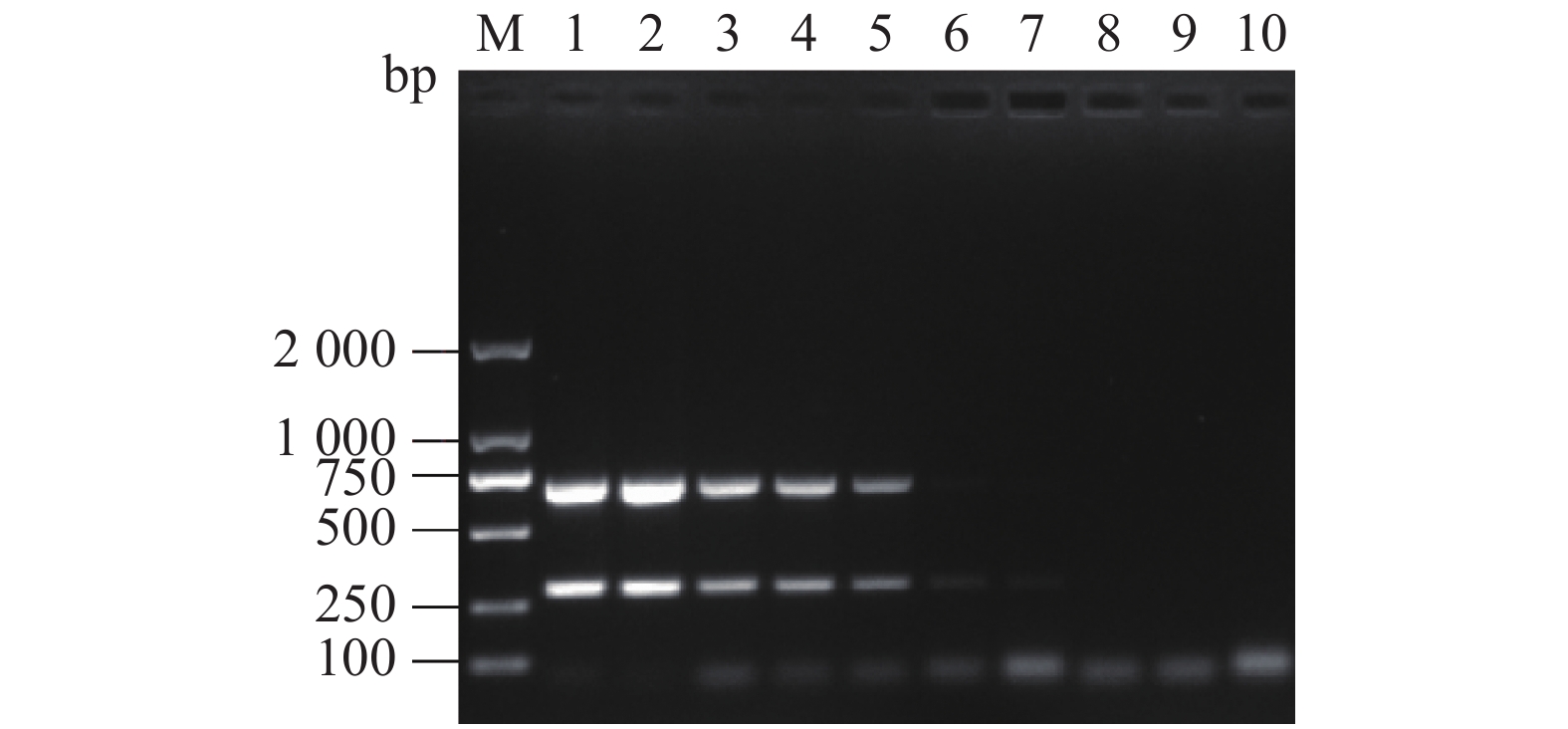
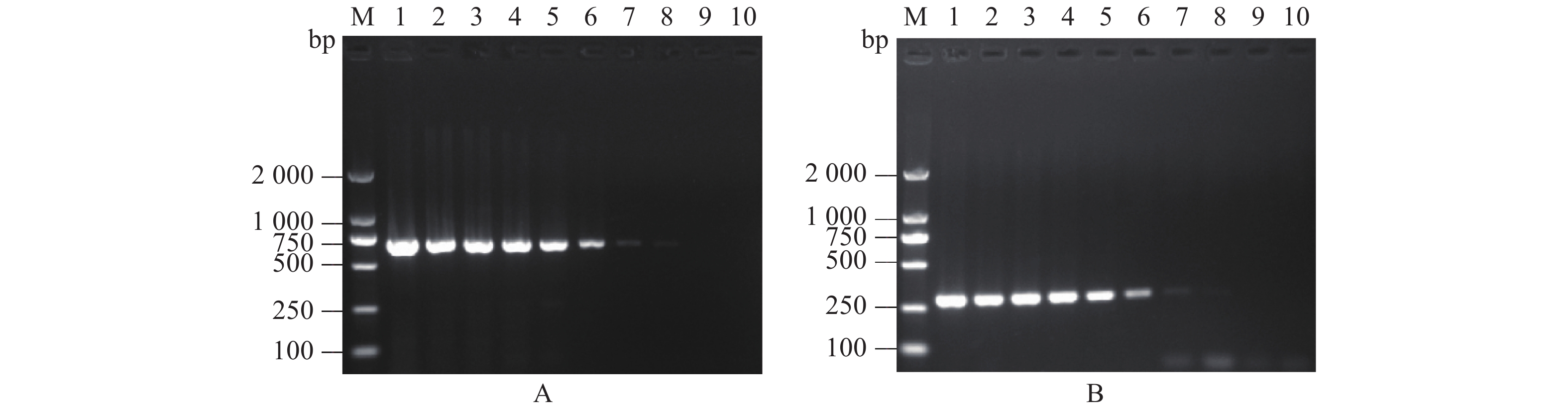
对Mo和CP的DNA进行浓度测定,Mo的DNA质量浓度约为153 ng·μL−1,CP的DNA质量浓度约为35 ng·μL−1。分别以101、102、103、104、105、106、107、108倍稀释,将稀释后的DNA作为模板进行双重PCR扩增。结果显示,当Mo和CP DNA稀释倍数达104和105时,双重PCR仍能扩增出约700 bp和290 bp的两个目的条带(图3),即Mo的检测下限为1 530 pg·μL−1、CP的检测下限为3 500 pg·μL−1,表明该方法的敏感性较高。而单一PCR检测结果显示(图4),Mo的检测灵敏度为15.3 pg·μL−1,CP的检测灵敏度为350 pg·μL−1,分别比双重PCR灵敏低100倍和10倍。
![]() 图 3 双重PCR灵敏性试验注:M: 2 000 DNA Ladder;1: Mo+CP阳性对照;2–9: 分别为101、102、103、104、105、106、107、108倍稀释的含Mo和CP的阳性样本;10: 阴性对照。Figure 3. Sensitivity of multiplex PCRNote:M: 2 000 DNA Ladder; 1: Mo and CP positive control; 2–9: positive specimens containing Mo and CP diluted 101, 102, 103, 104, 105, 106, 107, 108 times, respectively; 10: negative control.
图 3 双重PCR灵敏性试验注:M: 2 000 DNA Ladder;1: Mo+CP阳性对照;2–9: 分别为101、102、103、104、105、106、107、108倍稀释的含Mo和CP的阳性样本;10: 阴性对照。Figure 3. Sensitivity of multiplex PCRNote:M: 2 000 DNA Ladder; 1: Mo and CP positive control; 2–9: positive specimens containing Mo and CP diluted 101, 102, 103, 104, 105, 106, 107, 108 times, respectively; 10: negative control.![]() 图 4 单一PCR灵敏性试验注:A中,M: 2 000 DNA Ladder;1: Mo阳性对照;2–9: 分别为101、102、103、104、105、106、107、108倍稀释的含Mo的阳性样本;10: 阴性对照;B中,M: 2 000 DNA Ladder;1: CP 阳性对照;2–9分别为101、102、103、104、105、106、107、108倍稀释的含CP 的阳性样本;10: 阴性对照。Figure 4. Sensitivity of single PCRNote:A:M: 2 000 DNA Ladder; 1: Mo positive control; 2–9: positive specimens containing Mo diluted 101,102,103,104,105,106,107,108 times, respectively; 10: negative control; B: M: 2 000 DNA Ladder; 1: CP positive control; 2–9: positive specimens containing CP diluted 101,102,103,104,105,106,107,108 times, respectively; 10: negative control.
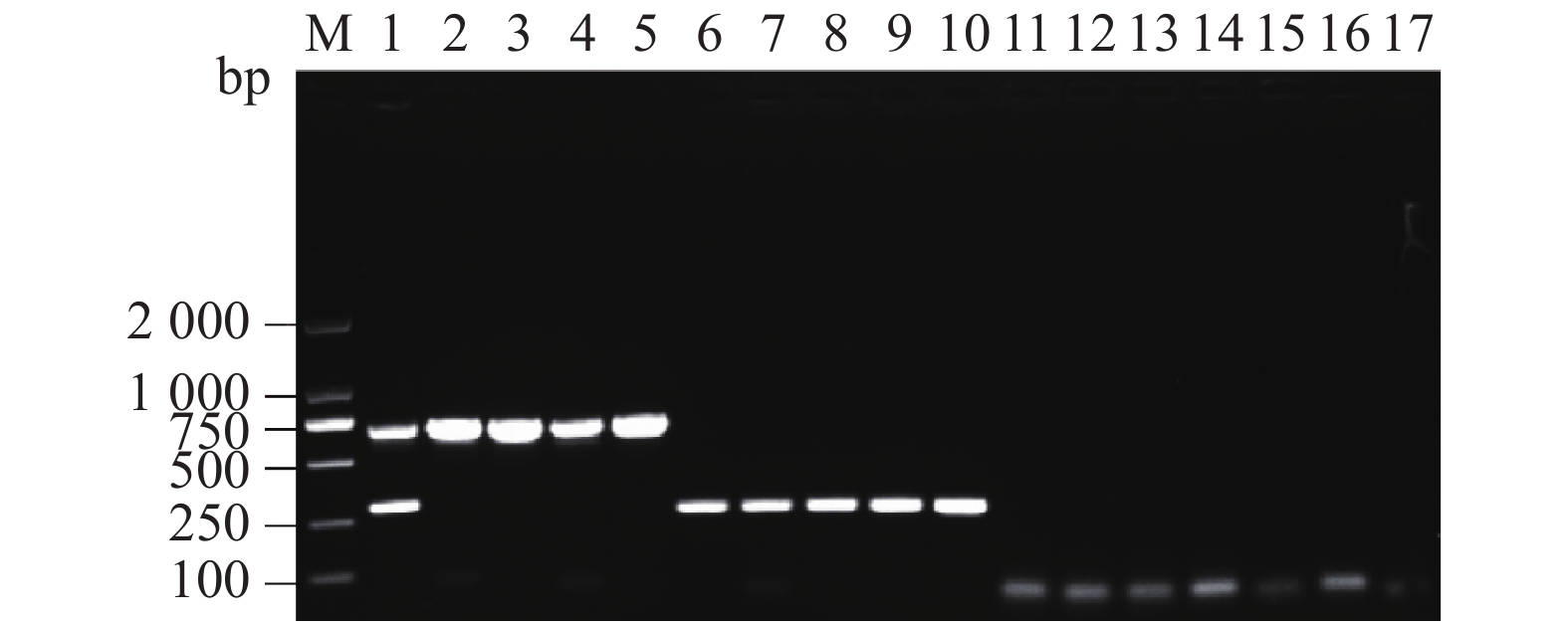
图 4 单一PCR灵敏性试验注:A中,M: 2 000 DNA Ladder;1: Mo阳性对照;2–9: 分别为101、102、103、104、105、106、107、108倍稀释的含Mo的阳性样本;10: 阴性对照;B中,M: 2 000 DNA Ladder;1: CP 阳性对照;2–9分别为101、102、103、104、105、106、107、108倍稀释的含CP 的阳性样本;10: 阴性对照。Figure 4. Sensitivity of single PCRNote:A:M: 2 000 DNA Ladder; 1: Mo positive control; 2–9: positive specimens containing Mo diluted 101,102,103,104,105,106,107,108 times, respectively; 10: negative control; B: M: 2 000 DNA Ladder; 1: CP positive control; 2–9: positive specimens containing CP diluted 101,102,103,104,105,106,107,108 times, respectively; 10: negative control.2.5 双重PCR重复性试验结果
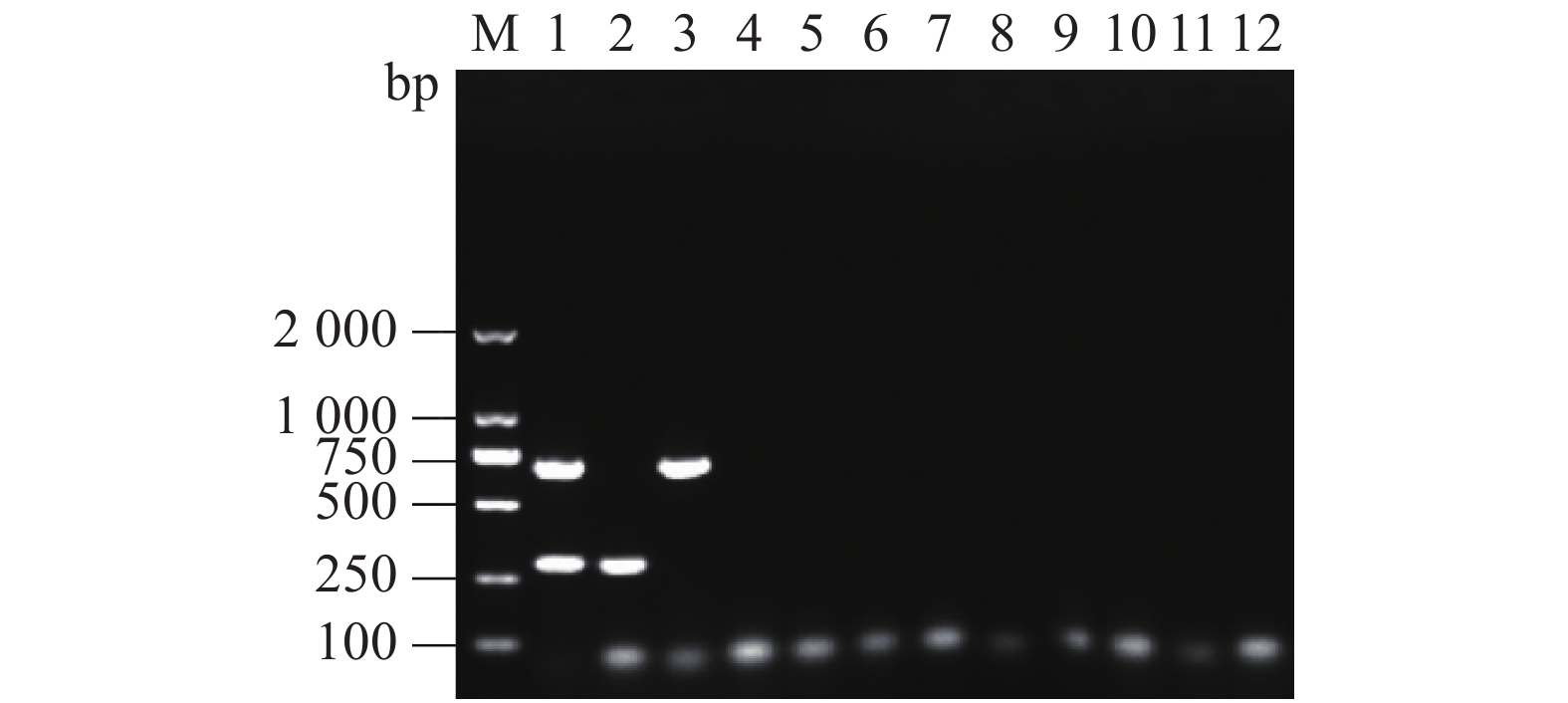
采用本试验建立的双重PCR方法对Mo + CP、Mo、CP、Mccp、Mmc、AL、Ec、SA、SE的DNA 样品进行3次组内重复试验。结果显示,Mo + CP的DNA样品均扩增出大小约为700 bp和290 bp的2个特异性片段,4份Mo DNA均扩增出大小约为700 bp的特异性片段,5份CP DNA都扩增出大小约为290 bp的特异性片段,其余样品和ddH2O均无扩增片段(图5);组间重复试验结果显示,3次PCR检测结果相同:Mo + CP、Mo、CP的DNA均有目的条带(图略),其余样品均无目的条带,表明该双重PCR重复性好。
2.6 双重PCR临床样品检测结果
应用Mo和CP单一PCR及本研究建立的双重PCR方法分别对来自福州市等不同地区的鼻腔棉拭子样品43份、肺组织27份进行检测。结果显示(表2),Mo和CP单一PCR与双重PCR检测结果完全一致,2种方法的符合率为100%。其中18份为Mo感染,13份为CP感染,5份为Mo和CP的混合感染,且应用Mo和CP单一PCR和双重PCR进行的3次检测结果相同。表明本研究建立的Mo、CP双重 PCR 检测方法可应用于临床样品的快速检测。
表 2 临床样品检测结果Table 2. Detection of pathogens on clinical specimens样品名称
Sample nameMo阳性率
Mo positive rate/%CP阳性率
CP positive rate/%Mo + CP阳性率
Mo + CP positive rate/%鼻拭子
Nasal cotton swab18.60 11.63 4.65 肺组织
Lung tissue37.04 29.63 11.11 所有样品
All samples25.71 18.57 7.14 3. 讨论与结论
随着养羊业的快速发展,羊的疾病日趋复杂化,单一病原引起的感染越来越少,混合感染呈现出上升趋势,对羊病的有效防控难度增加,给养羊业带来了严重的经济损失,已引起广大兽医工作者的关注[33-35]。为了解福建省Mo和CP混合感染情况,有效防治羊病,本研究应用Mo和CP的两对特异性引物,通过优化反应体系和条件以及特异性和灵敏性等试验,建立了Mo和CP的双重PCR检测技术。
双重PCR是指将多对引物同在一个反应体系里,扩增出多个不同大小产物的技术,广泛应用于病原微生物检测与鉴定[36]。双重PCR反应受众多因素的影响,其中影响较大的是退火温度和引物浓度。本试验就引物浓度和退火温度进行优化。优化引物浓度时,设置7个引物梯度(0.7、0.8、0.9、1.0、1.1、1.2 和1.3 μL),其他条件不变,最终确定Mo和CP的最佳引物浓度是上、下游引物(10 μmol·L−1)各1 μL;优化退火温度时,设置7个退火温度(51、53、55、57、59、61和63℃),用最佳引物浓度进行PCR,确定其最佳退火温度为61℃。采用所优化的双重PCR体系仅对Mo和CP有特异性扩增,而对Mmc、Mcc、Mccp、AL、Mb、SE、Ec、SA等病原体的扩增结果均为阴性,与侯宏艳等[37]、张洁[38]、王璇等[39]、李文杨等[9]一般的分离培养鉴定法相比,其特异性更好。该双重PCR方法对Mo和CP的最低检测限分别为1 530 pg·μL−1和3 500 pg·μL−1,表明该方法灵敏度较高;同时具有良好的重复性,可对病原体含量较低的样品进行快速检测。
为了验证该技术的实用效果,采用此方法和单一PCR分别对临床采集的70份样品进行检测。结果检出Mo阳性样品18份(阳性率为25.71%),CP阳性样品13份(阳性率为18.57%),同时感染Mo和CP的阳性样品5份(阳性率为7.14%),Mo、CP单一和双重PCR检测方法的符合率为100%,表明该方法的准确性好,可应用于临床样品的准确快速检测。同时,本次检测结果提示,福建省羊场存在Mo和CP共感染的现象,这与Thomas[40]和许国洋等[41]等的报道相似,应在今后羊病防控工作中引起重视。
-
图 3 双重PCR灵敏性试验
注:M: 2 000 DNA Ladder;1: Mo+CP阳性对照;2–9: 分别为101、102、103、104、105、106、107、108倍稀释的含Mo和CP的阳性样本;10: 阴性对照。
Figure 3. Sensitivity of multiplex PCR
Note:M: 2 000 DNA Ladder; 1: Mo and CP positive control; 2–9: positive specimens containing Mo and CP diluted 101, 102, 103, 104, 105, 106, 107, 108 times, respectively; 10: negative control.
图 4 单一PCR灵敏性试验
注:A中,M: 2 000 DNA Ladder;1: Mo阳性对照;2–9: 分别为101、102、103、104、105、106、107、108倍稀释的含Mo的阳性样本;10: 阴性对照;B中,M: 2 000 DNA Ladder;1: CP 阳性对照;2–9分别为101、102、103、104、105、106、107、108倍稀释的含CP 的阳性样本;10: 阴性对照。
Figure 4. Sensitivity of single PCR
Note:A:M: 2 000 DNA Ladder; 1: Mo positive control; 2–9: positive specimens containing Mo diluted 101,102,103,104,105,106,107,108 times, respectively; 10: negative control; B: M: 2 000 DNA Ladder; 1: CP positive control; 2–9: positive specimens containing CP diluted 101,102,103,104,105,106,107,108 times, respectively; 10: negative control.
表 1 引物序列
Table 1 Primer sequence
靶基因
Target gene引物名称
Primer name引物序列(5′→ 3′)
Primer sequence(5′→ 3′)扩增片段大小
Amplified fragment size/bpP80基因 F1 GCCTTGGGGTTGGAATTCCTTTGTCTTATTC 705 R1 CATTTGATGCTGAGGTCGGATTTGGACTAAC PLD基因 F2 GTGAGAAGAACCCCGGTATAAG 291 R2 TACCGCACTTATTCTGACACTG 表 2 临床样品检测结果
Table 2 Detection of pathogens on clinical specimens
样品名称
Sample nameMo阳性率
Mo positive rate/%CP阳性率
CP positive rate/%Mo + CP阳性率
Mo + CP positive rate/%鼻拭子
Nasal cotton swab18.60 11.63 4.65 肺组织
Lung tissue37.04 29.63 11.11 所有样品
All samples25.71 18.57 7.14 -
[1] 邓守全, 霍晓伟. 一株绵羊肺炎支原体的分离及鉴定 [J]. 中国生物制品学杂志, 2017, 30(11):1153−1156. DENG S Q, HUO X W. Separation and identification of a strain of sheep Mycoplasma pneumonia [J]. Chinese Journal of Biologicals, 2017, 30(11): 1153−1156.(in Chinese)
[2] 崔康康, 姚亚军, 肖虎锁, 等. 一起羊支原体性肺炎的诊疗 [J]. 山东畜牧兽医, 2017, 38(10):38. DOI: 10.3969/j.issn.1007-1733.2017.10.026 CUI K K, YAO Y J, XIAO H S, et al. A diagnosis and treatment of Mycoplasma pneumoniae of sheep [J]. Shandong Journal of Animal Science and Veterinary Medicine, 2017, 38(10): 38.(in Chinese) DOI: 10.3969/j.issn.1007-1733.2017.10.026
[3] 陆震, 吴翠兰, 李军, 等. 绵羊肺炎支原体病的诊断与防制 [J]. 今日畜牧兽医, 2019, 35(6):80−81. DOI: 10.3969/j.issn.1673-4092.2019.06.075 LU Z, WU C L, LI J, et al. Research Progress of Mycoplasma Pneumonia in Sheep [J]. Today Animal Husbandry and Veterinary Medicine, 2019, 35(6): 80−81.(in Chinese) DOI: 10.3969/j.issn.1673-4092.2019.06.075
[4] BESSER T E, CASSIRER E F, POTTER K A, et al. Association of Mycoplasma ovipneumoniae infection with population limiting respiratory disease in free-ranging Rocky Mountain bighorn sheep (Ovis canadensis canadensis) [J]. Journal of Clinical Microbiology, 2008, 46(2): 423−430. DOI: 10.1128/JCM.01931-07
[5] DASSANAYAKE R P, SHANTHALINGAM S, HERNDON C N, et al. Mycoplasma ovipneumoniae can predispose bighorn sheep to fatal Mannheimia haemolytica pneumonia [J]. Veterinary Microbiology, 2010, 145(3-4): 354−359. DOI: 10.1016/j.vetmic.2010.04.011
[6] RIFATBEGOVIC M, MAKSIMOVIC Z, HULAJ B. Mycoplasma ovipneumoniae associated with severe respiratory disease in goats [J]. Veterinary Record, 2011, 168(21): 565.
[7] YANG F, DAO X, RODRIGUEZ- PALACIOS A, et al. A Real-time PCR for detection and quantification of Mycoplasma ovipneumoniae [J]. Journal of Veterinary Medical Science, 2014, 76(12): 1631−1634. DOI: 10.1292/jvms.14-0094
[8] 储岳峰. 我国山羊(接触)传染性胸膜肺炎病原学、流行病学研究及灭活疫苗的研制[D]. 北京: 中国农业科学院研究生院兰州兽医研究所, 2011. CHU Y F. An etiological and epidemiological study on contagious caprine pleuropneumonia in China and development of a bacterin against it[D]. Beijing: Lanzhou Veterinary Research Institute, Graduate School of Chinese Academy of Agricultural Sciences, 2011. (in Chinese)
[9] 李文杨, 刘远, 张晓佩, 等. 山羊伪结核棒状杆菌的分离鉴定 [J]. 中国草食动物科学, 2014, 34(5):49−51. DOI: 10.3969/j.issn.2095-3887.2014.05.015 LI W Y, LIU Y, ZHANG X P, et al. Isolation and Identification of Corynebacterium pseudotuberculosis [J]. China Herbivore Science, 2014, 34(5): 49−51.(in Chinese) DOI: 10.3969/j.issn.2095-3887.2014.05.015
[10] BAIRD G J, FONTAINE M C. Corynebacterium pseudotuberculosis and its role in ovine caseous lymphadenitis [J]. Journal of Comparative Pathology, 2007, 137(4): 179−210. DOI: 10.1016/j.jcpa.2007.07.002
[11] 周作勇, 李和贤, 杨浩钺, 等. 伪结核棒状杆菌毒力因子的研究进展 [J]. 中国人兽共患病学报, 2017, 33(12):1115−1119. DOI: 10.3969/j.issn.1002-2694.2017.12.012 ZHOU Z Y, LI H X, YANG H Y, et al. Research advances on the virulence factors of Corynebacterium pseudotuberculosis [J]. Chinese Journal of Zoonoses, 2017, 33(12): 1115−1119.(in Chinese) DOI: 10.3969/j.issn.1002-2694.2017.12.012
[12] 徐志豪, 黄诗琴, 李乡城, 等. 四川省山羊皮下脓肿的流行病学调查及病原体分析 [J]. 中国兽医科学, 2016, 46(8):991−996. XU Z H, HUANG S Q, LI X C, et al. Epidemiological survey and etiological analysis in goat with subcutaneous abscess in Sichuan Province [J]. Chinese Veterinary Science, 2016, 46(8): 991−996.(in Chinese)
[13] 马玉馨, 李文贵, 郑国英, 等. 山羊伪结核棒状杆菌TaqMan荧光定量PCR检测方法的建立和初步应用 [J]. 畜牧与兽医, 2018, 50(10):82−87. MA Y X, LI W G, ZHENG G Y, et al. Establishment and preliminary application of TaqMan real-time PCR for detection of Corynebacterium pseudotuberculosis in goats [J]. Animal Husbandry & Veterinary Medicine, 2018, 50(10): 82−87.(in Chinese)
[14] 赵宏坤, 范伟兴, 胡敬东, 等. 羊伪结核病研究进展 [J]. 中国预防兽医学报, 2000, 22(3):77−78. ZHAO H K, FAN W X, HU J D, et al. Research progress of pseudotuberculosis in sheep [J]. Chinese Journal of Preventive Veterinary Medicine, 2000, 22(3): 77−78.(in Chinese)
[15] 王全溪, 李国平. 波尔山羊伪结核棒状杆菌的分离鉴定 [J]. 中国兽医杂志, 2004, 40(9):53−54. DOI: 10.3969/j.issn.0529-6005.2004.09.023 WANG Q X, LI G P. Isolation and Identification of pseudotuberculosis corynebacterium on Boer Goat [J]. Chinese Journal of Veterinary Medicine, 2004, 40(9): 53−54.(in Chinese) DOI: 10.3969/j.issn.0529-6005.2004.09.023
[16] 赵宏坤, 周维武, 色音巴亚尔, 等. 由溶解的山羊胎儿分离出一株羊伪结核棒状杆菌 [J]. 中国畜禽传染病, 1994, 16(2):31−32. ZHAO H K, ZHOU W W, SAYINBAYAR, et al. A strain of Corynebacterium pseudotuberculosis isolated from a dissolved goat fetus [J]. Chinese Journal of Animal and Poultry Infectious Diseases, 1994, 16(2): 31−32.(in Chinese)
[17] 韩瑞鑫, 申捷, 申之义. 绵羊肺炎支原体TaqMan实时荧光定量PCR检测方法的建立与应用 [J]. 中国兽医科学, 2018, 48(8):965−970. HAN R X, SHEN J, SHEN Z Y. Development and application of TaqMan real-time fluorescent quantitation PCR for the detection of Mycoplasma ovipneumoniae [J]. Chinese Veterinary Science, 2018, 48(8): 965−970.(in Chinese)
[18] 林裕胜, 江锦秀, 张靖鹏, 等. 绵羊肺炎支原体RPA检测技术的建立 [J]. 福建农业学报, 2019, 34(4):416−421. LIN Y S, JIANG J X, ZHANG J P, et al. Establishment of a RPA Method for Detecting Mycoplasma pneumoniae [J]. Fujian Journal of Agricultural Sciences, 2019, 34(4): 416−421.(in Chinese)
[19] 王娟, 刀筱芳, 刘海燕, 等. 绵羊肺炎支原体恒温热隔绝式PCR方法的建立 [J]. 中国预防兽医学报, 2019, 41(4):380−384. WANG J, DAO X F, LIU H Y, et al. Development of an insulated isothermal PCR for detection of Mycoplasma pneumoniae [J]. Chinese Journal of Preventive Veterinary Medicine, 2019, 41(4): 380−384.(in Chinese)
[20] 张双翔, 周碧君, 程振涛, 等. 绵羊肺炎支原体LAMP检测方法的建立及初步应用 [J]. 中国兽医学报, 2013, 33(3):362−366. ZHANG S X, ZHOU B J, CHENG Z T, et al. Development and application of a loop-mediated isothermal amplification assay for detection of Mycoplasma ovipneumoniae [J]. Chinese Journal of Veterinary Science, 2013, 33(3): 362−366.(in Chinese)
[21] 赵萍, 储岳峰, 高鹏程, 等. 绵羊肺炎支原体间接ELISA检测方法的建立及应用 [J]. 福建农林大学学报(自然科学版), 2008, 37(5):510−513. ZHAO P, CHU Y F, GAO P C, et al. Establishment and application of indirect ELISA method for Mycoplasma ovipneumoniae [J]. Journal of Fujian Agriculture and Forestry University (Natural Science Edition), 2008, 37(5): 510−513.(in Chinese)
[22] 许国洋, 付利芝, 龙小飞, 等. 山羊伪结核棒状杆菌PMA-PCR检测方法的建立 [J]. 现代畜牧兽医, 2018(11):9−13. XU G Y, FU L Z, LONG X F, et al. Establishment of PMA-PCR detection method for Corynebacterium pseudotuberculosis in Goat [J]. Modern Journal of Animal Husbandry and Veterinary Medicine, 2018(11): 9−13.(in Chinese)
[23] 郑敏, 胡杰, 欧绍毅, 等. 广西黑山羊伪结核棒状杆菌的分离与鉴定 [J]. 广西农业科学, 2010, 41(10):1128−1130. ZHENG M, HU J, OU S Y, et al. Isolation and Identification of Corynebacterium pseudotuberculosis from black goat in Guangxi [J]. Guangxi Agricultural Sciences, 2010, 41(10): 1128−1130.(in Chinese)
[24] 韦志锋, 李常挺, 陶立, 等. 山羊干酪性淋巴结炎病原的分离和鉴定 [J]. 中国动物检疫, 2011, 28(7):54−55, 59. DOI: 10.3969/j.issn.1005-944X.2011.07.028 WEI Z F, LI C T, TAO L, et al. Isolation and identification of goat caseinous lymphadenitis [J]. China Animal Health Inspection, 2011, 28(7): 54−55, 59.(in Chinese) DOI: 10.3969/j.issn.1005-944X.2011.07.028
[25] 朱伟英, 猴银行, 霍宁宁, 等. 一株奶山羊伪结核棒状杆菌的分离与鉴定 [J]. 动物医学进展, 2017, 38(5):127−132. DOI: 10.3969/j.issn.1007-5038.2017.05.029 ZHU W Y, HOU Y H, HUO N N, et al. Isolation and identification of corynebacterium pseudotuberculosis from goats [J]. Progress in Veterinary Medicine, 2017, 38(5): 127−132.(in Chinese) DOI: 10.3969/j.issn.1007-5038.2017.05.029
[26] 王韡, 张彦明, 邢福珊, 等. 羊伪结核棒状杆菌的分离鉴定及ELISA检测方法的建立 [J]. 中国兽医学报, 2005, 25(1):34−36. DOI: 10.3969/j.issn.1005-4545.2005.01.012 WANG W, ZHANG Y M, XING F S, et al. Isolation, identification of Corynebacterium pseudotuberculosis and establishment of ELISA detection method [J]. Chinese Journal of Veterinary, 2005, 25(1): 34−36.(in Chinese) DOI: 10.3969/j.issn.1005-4545.2005.01.012
[27] 黄丽丽, 林裕胜, 江锦秀, 等. 山羊伪结核棒状杆菌的分离鉴定及耐药性分析 [J]. 福建农业学报, 2019, 34(8):925−932. HUANG L L, LIN Y S, JIANG J X, et al. Isolation, identification and antibiotics resistance of corynebacterium pseudotuberculosis from goats [J]. Fujian Journal of Agricultural Sciences, 2019, 34(8): 925−932.(in Chinese)
[28] 江锦秀, 林甦, 林裕胜, 等. 绵羊肺炎支原体FJ01-CL株的分离和鉴定 [J]. 福建农业学报, 2015, 30(5):430−434. DOI: 10.3969/j.issn.1008-0384.2015.05.002 JIANG J X, LIN S, LIN Y S, et al. Isolation and identification of Mycoplasma ovipneumoniae FJ01-CL [J]. Fujian Journal of Agricultural Sciences, 2015, 30(5): 430−434.(in Chinese) DOI: 10.3969/j.issn.1008-0384.2015.05.002
[29] 江锦秀, 林裕胜, 游伟, 等. 丝状支原体山羊亚种FJ-GT株的分离和鉴定 [J]. 中国农学通报, 2016, 32(29):11−16. DOI: 10.11924/j.issn.1000-6850.casb16030148 JIANG J X, LIN Y S, YOU W, et al. Isolation and identification of Mycoplasma mycoides subsp. capri FJ-GT strain [J]. Chinese Agricultural Science Bulletin, 2016, 32(29): 11−16.(in Chinese) DOI: 10.11924/j.issn.1000-6850.casb16030148
[30] 江锦秀, 林裕胜, 游伟, 等. 山羊莱氏无胆甾原体FJ-NP株的分离鉴定 [J]. 中国畜牧兽医, 2016, 43(12):3329−3335. JIANG J X, LIN Y S, YOU W, et al. Isolation and identification of acholeplasma laidlawii FJ-NP strains in goat [J]. China Animal Husbandry & Veterinary Medicine, 2016, 43(12): 3329−3335.(in Chinese)
[31] 江锦秀, 林裕胜, 游伟, 等. 牛支原体FJ-HJ分离株的分离及鉴定 [J]. 中国农学通报, 2017, 33(20):107−112. JIANG J X, LIN Y S, YOU W, et al. Isolation and identification of mycoplasma bovis FJ-HJ strain [J]. Chinese Agricultural Science Bulletin, 2017, 33(20): 107−112.(in Chinese)
[32] 林裕胜, 江锦秀, 江斌, 等. ORFV和Mo双重PCR检测方法的建立及应用 [J]. 农业生物技术学报, 2017, 25(8):1374−1380. LIN Y S, JIANG J X, JIANG B, et al. Establishment and application of a duplex pcr assay for detection of orf virus (ORFV) and Mycoplasma ovipneumoniae (Mo) [J]. Journal of Agricultural Biotechnology, 2017, 25(8): 1374−1380.(in Chinese)
[33] ANDERSON D E, RINGS D M, KOWALSKI J. Infection with Corynebacterium pseudotuberculosis in five alpacas [J]. Journal of the American Veterinary Medical Association, 2004, 225(11): 1743−1747, 1702. DOI: 10.2460/javma.2004.225.1743
[34] STEHMAN S M. Paratuberculosis in small ruminants, deer, and south american camelids [J]. Veterinary Clinics of North America: Food Animal Practice, 1996, 12(2): 441−455. DOI: 10.1016/S0749-0720(15)30416-3
[35] DASSANAYAKE R P, SHANTHALINGAM S, HERNDON C N, et al. Mycoplasma ovipneumoniae can predispose bighorn sheep to fatal Mannheimia haemolytica pneumonia [J]. Veterinary Microbiology, 2010, 145(3/4): 354−359.
[36] 李庆超.多重PCR技术同时高效检测食源性致病菌的研究[D]. 吉林大学, 2017. LI Q C. Study of multiplex PCR technology in the simultaneously and efficiently detection of food-borne pathogenic bacteria[D]. Changchun: Jilin University, 2017. (in Chinese)
[37] 侯宏艳, 惠文巧, 张丹俊, 等. 山羊的绵羊肺炎支原体的分离和鉴定 [J]. 安徽农业科学, 2015, 43(28):159−160. DOI: 10.3969/j.issn.0517-6611.2015.28.062 HOU H Y, HUI W Q, ZHANG D J, et al. Isolation and Identification of Mycoplasma ovipneumoniae from goats [J]. Journal of Anhui Agricultural Sciences, 2015, 43(28): 159−160.(in Chinese) DOI: 10.3969/j.issn.0517-6611.2015.28.062
[38] 张洁, 曹军军, 祝明松, 等. 基于绵羊肺炎支原体EF-Tu蛋白间接ELISA方法的建立 [J]. 动物医学进展, 2019, 40(11):6−13. ZHANG J, CAO J J, ZHU M S, et al. Establishment of indirect ELISA method based on Mycoplasma pneumoniae EF-Tu protein [J]. Progress in Veterinary Medicine, 2019, 40(11): 6−13.(in Chinese)
[39] 王璇, 潘淑惠, 万一元. 山羊伪结核棒状杆菌病的ELISA诊断 [J]. 上海畜牧兽医通讯, 2009(2):29. DOI: 10.3969/j.issn.1000-7725.2009.02.013 WANG X, PAN S H, WAN Y Y. ELISA diagnosis of corynebacterium tuberculosis in goats [J]. Shanghai Journal of Animal Husbandry and Veterinary Medicine, 2009(2): 29.(in Chinese) DOI: 10.3969/j.issn.1000-7725.2009.02.013
[40] BESSER T E, HIGHLAND M, BAKER K, et al. Causes of pneumonia epizootics among Bighorn sheep, western United States, 2008–2010 [J]. Emerging Infectious Diseases, 2012, 18(3): 406−414. DOI: 10.3201/eid1803.111554
[41] 许国洋, 付利芝, 杨金龙, 等. 山羊淋巴结炎病原菌的分离鉴定及多重PCR检测方法的建立 [J]. 畜牧兽医学报, 2017, 48(2):324−330. DOI: 10.11843/j.issn.0366-6964.2017.02.016 XU G Y, FU L Z, YANG J L, et al. Isolation and identification of pathogenic bacteria of lymphadenitis in goat and establishment of multiplex PCR detection method [J]. Chinese Journal of Animal and Veterinary Sciences, 2017, 48(2): 324−330.(in Chinese) DOI: 10.11843/j.issn.0366-6964.2017.02.016
-
期刊类型引用(4)
1. 杨帅,段宏伟,吕建树,曾建林,闫振兴,胡俊杰,张勇,赵兴绪. 甘肃省庆阳地区湖羊皮下脓肿病的流行病学调查及病原体分析. 核农学报. 2023(12): 2510-2517 .  百度学术
百度学术
2. 杨鹏,吴燕,岳筠,陈静,李梅,王慧,张双翔,文明,程振涛. 绵羊肺炎支原体P113蛋白C末端基因真核表达载体的构建及其小鼠免疫应答. 中国兽医学报. 2022(03): 496-501+521 .  百度学术
百度学术
3. 杨鹏,杨源,岳筠,陈静,王慧,朱二鹏,张双翔,文明,程振涛. 绵羊肺炎支原体感染对贵州不同品种山羊肺脏和血液Toll样受体基因转录水平的影响. 动物医学进展. 2022(12): 1-9 .  百度学术
百度学术
4. 尹峥,刘刚,王晶晶,李晨露,徐海玲,张琪,许信刚. 基于PLD蛋白的伪结核棒状杆菌血清抗体间接ELISA检测方法的建立与应用. 中国兽医科学. 2021(01): 9-16 .  百度学术
百度学术
其他类型引用(4)




 下载:
下载: