Conditions for Germination of Mycogone perniciosa Chlamydospores
-
摘要:目的 研究影响有害疣孢霉厚垣孢子萌发的因素,为进一步开展有害疣孢霉生物学特性研究以及筛选可有效抑制其萌发的杀菌剂提供依据。方法 在−80℃、−20℃、0℃、4℃、10℃、15℃、20℃和25℃处理有害疣孢霉厚垣孢子,然后25℃培养,测定温度对破除有害疣孢霉厚垣孢子休眠的影响;测定不同培养基、pH值、碳源和氮源对有害疣孢霉厚垣孢子萌发的影响。结果 0℃、4℃处理12 h、24 h和48 h可破除有害疣孢霉厚垣孢子休眠,促进萌发;适合有害疣孢霉厚垣孢子萌发的pH值为6、7和8,其萌发率分别为8.66%、9.79%和8.40%;有害疣孢霉厚垣孢子在水琼脂培养基(WA)、双孢蘑菇浸出液培养基(MuEA)、双孢蘑菇煎汁培养基(MuDA)、马铃薯葡萄糖培养基(PDA)和V8培养基上的萌发率分别为0.00%、6.38%、8.43%、1.33%和6.23%,在MuDA培养基上萌发率最好,显著优于其他供试培养基;葡萄糖、蔗糖和山梨糖有利于有害疣孢霉厚垣孢子萌发,其萌发率分别为10.77%、9.96%和9.85%;在MuDA培养基中加入脯氨酸、丝氨酸、丙氨酸和鸟氨酸后有害疣孢霉厚垣孢子的萌发率分别为12.32%、13.45%、13.74%和11.64%,显著优于不加氮源的萌发率。结论 0℃、4℃处理12 h以上可破除有害疣孢霉厚垣孢子的休眠;适合有害疣孢霉厚垣孢子萌发的pH值为6、7和8;MuDA培养基是适宜有害疣孢霉厚垣孢子萌发的培养基;葡萄糖、蔗糖、D-乳糖、山梨糖和D-棉子糖是适宜有害疣孢霉厚垣孢子萌发的碳源;脯氨酸、丝氨酸、丙氨酸和鸟氨酸是适宜有害疣孢霉厚垣孢子萌发的氮源。Abstract:Objective To identify conditions that facilitate germination of Mycogone perniciosa chlamydospores for further research on effective control of the fungal disease on edible mushrooms.Method Chlamydospores were kept at −80℃, −20℃, 0℃, 4℃, 10℃, 15℃, 20℃ or 25℃ for various durations prior to culture on media at 25℃ to determine the effects of dormancy-breaking temperatures. And effects of varied pHs, culture conditions, carbon source and nitrogen source on the chlamydospores germination were detected.Result Dormancy of the chlamydospores was broken and germination promoted under 0℃ or 4℃ for 12 h, 24 h or 48 h. pH 6, 7 and 8 were conducive to the spore germination at the rates of 8.66%, 9.79%, and 8.40%, respectively. The germination rate varied according to the medium the spores grew on. It was 0.00% on WA, 6.38% on MuEA, 8.43% on MuDA, 1.33% on PDA, and 6.23% on V8. Thus, MuDA appeared significantly better than other media tested in this study. The chlamydospores showed a germination rate of 10.77% with glucose, 9.96% with sucrose or 9.85% with sorbose in the medium, indicating a significantly advantage of the presence of a carbon source. In so far as nitrogen is concerned, the addition of proline in MuDA delivered a 12.32% germination rate, serine 13.45%, alanine 13.74%, and ornithine 11.64%, which were significantly improved over control without the addition.Conclusion By keeping M. perniciosa chlamydospores at 0℃ or 4℃ for more than 12 h could break the spore dormancy. On MuDA of pH 6, 7 or 8, the chlamydospores germinated well. With the presences of glucose, sucrose, D-lactose, sorbic sugar or D-raffinose as carbon source and L-proline, L-serline, L-alanine or L-qrnithine as nitrogen source, the spore germination was further enhanced.
-
Keywords:
- Mycogone perniciosa /
- chlamydospore /
- germination /
- Agaricus bisporus
-
0. 引言
【研究意义】由疣孢霉属真菌Mycogone LK. ex Chev.侵染引起的双孢蘑菇疣孢霉病又称褐腐病和湿泡病,是一种世界性的土传真菌病害[1]。1888年,法国巴黎首次报道了双孢蘑菇褐腐病的大爆发,此后在英国、美国、荷兰、澳大利亚等国家均有不同程度的发生,造成了巨大的经济损失[2], 在我国的福建、浙江、江苏等地双孢蘑菇种植区均有该病害发生且日趋严重,发病菇房损失率通常达30%,严重的菇房损失率高达50%~60%,甚至绝收,严重影响双孢蘑菇的产量和质量[3]。疣孢霉产生无色小型的分生孢子和双细胞褐色的厚垣孢子[4],厚垣孢子具有抗逆特性,但在室内培养条件下不易萌发,目前对有害疣孢霉厚垣孢子萌发特性的研究报道较少,探寻影响有害疣孢霉厚垣孢子萌发的因子,建立稳定的有害疣孢霉厚垣孢子萌发技术体系,对筛选抑制厚垣孢子萌发的杀菌剂,减少疣孢霉病的初侵染源,控制疣孢霉的侵染循环具有重要意义。【前人研究进展】根据疣孢霉菌丝颜色、厚垣孢子颜色、厚垣孢子上下细胞的大小,疣孢霉属被鉴定出4个种,其中有害疣孢霉菌M. perniciosa Magn.是造成我国双孢蘑菇疣孢霉病的主要病原菌[5-10]。病原菌的厚垣孢子具有耐干燥、耐低温、生存周期长和不易受环境影响的特点[11],这些特性帮助病原菌度过不良环境条件而成为初侵染源,在病害循环中起到重要作用。有害疣孢霉的分生孢子、厚垣孢子均具致病作用[12],分生孢子极易萌发,而厚垣孢子不易萌发,在PDA培养基上的萌发率为2%~3%[8, 13],在双孢蘑菇培养料中不能萌发和生长[14]。【本研究切入点】疣孢霉主要通过覆盖土进入菇房,侵染双孢蘑菇子实体形成的任何一个阶段[15-16],因此采用杀菌剂消毒覆盖土是防治双孢蘑菇疣孢霉病的主要措施,而杀菌剂的防治效果在第一潮菇时通常较好,从第二潮菇时开始下降[17],这可能与疣孢霉厚垣孢子利用自身的抗逆性度过杀菌剂的药效期后再萌发侵染有关。因此,探寻疣孢霉厚垣孢子的萌发因子,破解疣孢霉厚垣孢子抗逆性,将为探寻防治双孢蘑菇疣孢霉病的新途径提供参考。【拟解决的关键问题】测定温度、pH值、培养基、碳源和氮源等条件对有害疣孢霉厚垣孢子萌发的影响,探寻影响有害疣孢霉厚垣孢子萌发的主要因子,以期为双孢蘑菇疣孢霉病的防治提供科学依据。
1. 材料与方法
1.1 供试材料
供试菌株:供试有害疣孢霉菌株FJ81采集自福建省莆田市仙游县园庄镇园庄村,由福建省农业科学院植物保护研究所分离保存。
供试培养基:①水琼脂培养基(WA培养基):取蒸馏水1 000 mL,加入琼脂粉16 g(用于制作MuEA培养基时加入琼脂粉32 g),加热至琼脂粉完全溶解,加水定容至1 000 mL,121℃下高压湿热灭菌25 min;②双孢蘑菇煎汁培养基(MuDA培养基):取200 g新鲜的双孢蘑菇洗净,切片,加水煮沸30 min,用四层纱布过滤,上清液加入琼脂粉16 g,加热至琼脂粉完全溶解,加水定容至1 000 mL,121℃下高压湿热灭菌25 min,调节pH值至7.0;③双孢蘑菇浸出液培养基(MuEA培养基):将钮扣状新鲜的双孢蘑菇洗净,切片,40℃烘干48 h,用研钵研磨成粉,取2 g粉末加入100 mL的无菌水中,35℃水浴1 h,并不断搅拌,然后用四层纱布过滤,上清液再用滤纸过滤,加水定容至100 mL,用除菌滤膜过滤后分别装入5 mL无菌离心管中,置于0℃冰箱,备用。使用时将5 mL上清液加入融化的5 mL 3.2%水琼脂培养基中,混合均匀后倒入灭菌的培养皿[18];④马铃薯葡萄糖琼脂培养基(PDA培养基):将马铃薯200 g切片,加水煮沸30 min,用四层纱布过滤,上清液加入葡萄糖20 g、琼脂粉16 g,加热至琼脂粉完全溶解,加水定容至1 000 mL,在121℃下高压湿热灭菌25 min。⑤V8培养基:V-8果汁100 mL,CaCO3 1.4 g,琼脂粉16 g,加热至琼脂粉完全溶解,加水定容至1 000 mL,121℃下高压湿热灭菌25 min。
1.2 方法
1.2.1 有害疣孢霉厚垣孢子悬浮液的制备
将保存于滤纸片上的供试菌株转至PDA培养基平板上,28℃培养5 d,再转接至新的PDA培养基平板上,28℃培养10 d,用无菌水洗下厚垣孢子,配制成1.0×105个孢子·mL−1的孢子悬浮液,备用。
1.2.2 温度对打破有害疣孢霉厚垣孢子休眠的影响
取MuDA培养基10 mL倒入9 cm培养皿中,制成培养基平板,将有害疣孢霉菌株FJ81的厚垣孢子悬浮液0.5 mL均匀涂布于MuDA培养基平板上,风干多余水分,分别置于−80℃、−20℃、0℃、4℃、10℃、15℃、20℃、25℃黑暗培养12 h、24 h、48 h破除休眠,再分别置于25℃黑暗培养12 h、24 h、48 h,在显微镜下随机观察300个有害疣孢霉厚垣孢子的萌发情况,统计其萌发率和萌发类型,当芽管长度超过萌发细胞的半径时则记为萌发[19],试验设置3次重复。
1.2.3 pH对有害疣孢霉厚垣孢子萌发的影响
分别用0.1 mol·L−1盐酸溶液和0.1 mol·L−1的氢氧化钠溶液调节MuDA培养基的pH值至3、4、5、6、7、8、9和10,取各pH值的MuDA培养基10 mL于9 cm培养皿中,制成培养基平板,将有害疣孢霉菌株FJ81的厚垣孢子悬浮液0.5 mL均匀涂布于MuDA培养基平板上,风干多余水分,置于4℃黑暗培养24 h,再置于25℃黑暗培养24 h,在显微镜下观察300个有害疣孢霉厚垣孢子的萌发情况,统计其萌发率和萌发类型,当芽管长度超过萌发细胞的半径时则记为萌发,试验设置3次重复。
1.2.4 培养基对有害疣孢霉厚垣孢子萌发的影响
分别取WA培养基、MuDA培养基、MuEA培养基、PDA培养基和V8培养基10 mL倒入9 cm培养皿中,制成培养基平板,将有害疣孢霉菌株FJ81的厚垣孢子悬浮液0.5 mL分别涂布于WA培养基、MuDA培养基、MuEA培养基、PDA培养基和V8培养基平板上,风干多余水分,置于4℃黑暗培养24 h,再置于25℃黑暗培养24 h,在显微镜下随机观察不少于300个有害疣孢霉厚垣孢子的萌发情况,当芽管长度超过萌发细胞的半径时则记为萌发,统计其萌发率和萌发类型,试验设置3次重复。
1.2.5 碳源对有害疣孢霉厚垣孢子萌发的影响
在每升MuDA培养基中分别加入20 g葡萄糖、蔗糖、麦芽糖、D-乳糖、海藻糖、山梨糖、D-棉子糖、肌醇和甘露醇9种碳源,分别取含各碳源的MuDA培养基10 mL倒入9 cm培养皿中,制成含有不同碳源的培养基平板,将有害疣孢霉菌株FJ81的厚垣孢子悬浮液0.5 mL涂布于含有各碳源的MuDA培养基平板上,风干多余水分,置于4℃黑暗培养24 h,再置于25℃黑暗培养24 h,以不加碳源的MuDA培养基为对照,在显微镜下随机观察不少于300个有害疣孢霉厚垣孢子的萌发情况,当芽管长度超过萌发细胞的半径时则记为萌发,统计其萌发率和萌发类型,试验设置3次重复。
1.2.6 氮源对有害疣孢霉厚垣孢子萌发的影响
在每升MuDA培养基中分别加入10 g蛋白胨、硫酸铵、硝酸钾、硝酸铵、脯氨酸(L-proline)、色氨酸(tryptophan)、丝氨酸(L-serline)、甘氨酸(glycine)、胱氨酸(L-cystine)、丙氨酸(L-alanine)、鸟氨酸(L-qrnithine)、酪氨酸(L-tyrosine)、天门冬氨酸(L-aspartic acid)13种氮源,分别取含不同氮源的MuDA培养基10 mL倒入9 cm培养皿中,制成含有不同氮源的培养基平板,将有害疣孢霉菌株FJ81的厚垣孢子悬浮液0.5 mL涂布于含有各氮源的MuDA培养基平板上,风干多余水分,置于4℃黑暗培养24 h,再置于25℃黑暗培养24 h,以不加氮源的MuDA培养基为对照,在显微镜下随机观察300个有害疣孢霉厚垣孢子的萌发情况,当芽管长度超过萌发细胞的半径时则记为萌发,统计其萌发率和萌发类型,试验设置3次重复。
1.2.7 数据处理
萌发率/%=(萌发的厚垣孢子数/观察的厚垣孢子总数)×100[20-21]。
采用DPS 9.5软件Duncan’s新复极差法进行各数据间差异显著性分析[20],用Excel 2007绘制柱形图,分析各因素对有害疣孢霉厚垣孢子萌发的影响。
2. 结果与分析
2.1 温度对打破有害疣孢霉厚垣孢子休眠的影响
在0℃、4℃黑暗培养12 h、24 h、48 h均能破除有害疣孢霉厚垣孢子的休眠,其中在0℃黑暗培养12 h再置于25℃黑暗培养24 h和48 h的萌发率分别为2.75%和6.40%,在0℃黑暗培养24 h再置于25℃黑暗培养24 h和48 h的萌发率分别为4.70%和7.36%,在0℃黑暗培养48 h再置于25℃黑暗培养24 h和48 h的萌发率分别为5.76%和7.44%;而在4℃黑暗培养12 h再置于25℃黑暗培养12 h、24 h和48 h的萌发率分别为0.71%、2.68%和6.77%,在4℃黑暗培养24 h再置于25℃黑暗培养12 h、24 h和48 h的萌发率分别为1.45%、8.40%和9.23%,在4℃黑暗培养48 h再置于25℃黑暗培养12 h、24 h和48 h的萌发率分别为1.40%、9.79%和9.62%。其中4℃黑暗培养24 h再25℃处理48 h,4℃黑暗培养48 h,再25℃分别处理24 h和48 h后有害疣孢霉厚垣孢子的萌发率显著高于其他温度处理。有害疣孢霉厚垣孢子先在20℃处理,再25℃处理48 h以上及25℃处理48 h以上有一定的萌发率,但萌发率均较低。其他供试温度有害疣孢霉厚垣孢子均未萌发(表1)。
表 1 温度对有害疣孢霉厚垣孢子萌发率的影响Table 1. Effect of temperature on germination rate of M. perniciosa chlamydospores(单位: %) 温度
Temperature萌发率 Germination rate 萌发率 Germination rate 萌发率 Germination rate 12 h/12 h 12 h/24 h 12 h/48 h 24 h/12 h 24 h/24 h 24 h/48 h 48 h/12 h 48 h/24 h 48 h/48 h −80 ℃/25 ℃ 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k −20 ℃/25 ℃ 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0 ℃/25 ℃ 0.00 k 2.75 gh 6.40 de 0.00 k 4.70 f 7.36 c 0.00 k 5.76 e 7.44 c 4 ℃/25 ℃ 0.71 jk 2.68 gh 6.77 cd 1.45 ij 8.40 b 9.23 a 1.40 ij 9.79 a 9.62 a 10 ℃/25 ℃ 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 15 ℃/25 ℃ 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 20 ℃/25 ℃ 0.00 k 0.00 k 0.72 jk 0.00 k 0.66 jk 0.95 jk 0.96 j 1.24 ij 1.43 ij 25 ℃/25 ℃ 0.00 k 0.00 k 1.38 ij 0.00 k 1.25 ij 2.36 h 1.53 ij 1.98 hi 3.25 g 注:数据后不同小写字母分别表示在5%水平上差异显著。
Note: Data with lowercase letters indicate significant difference at P<0.05.2.2 pH对有害疣孢霉厚垣孢子萌发的影响
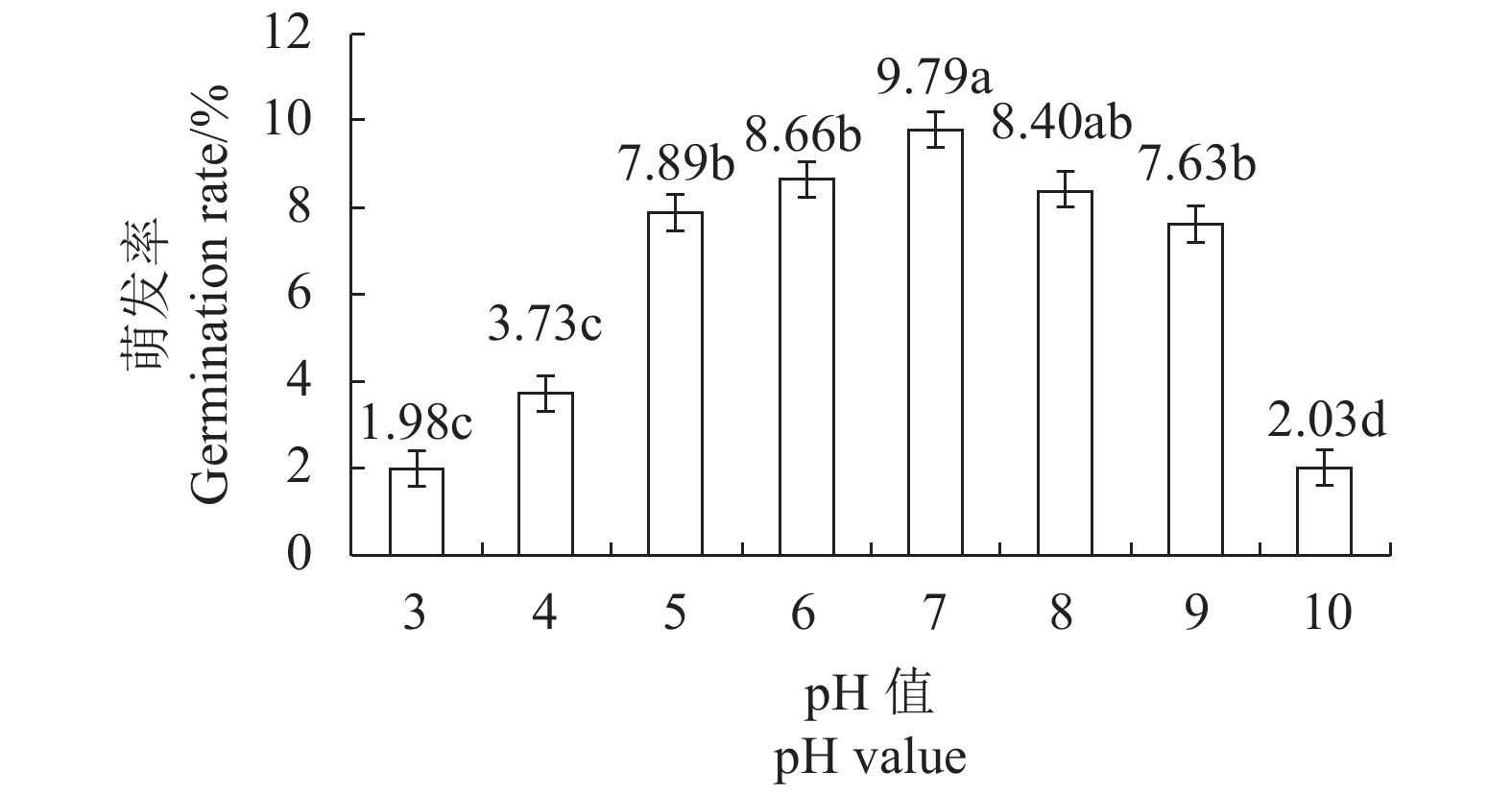
有害疣孢霉厚垣孢子在pH值为3、4、5、6、7、8、9和10的MuDA培养基上均可萌发,其中pH值6、7和8是较适合有害疣孢霉厚垣孢子萌发的酸碱度,其萌发率分别为8.66%、9.79%和8.40%,pH值7的萌发率与pH值6、pH值8的萌发率差异不显著,但显著高于其他供试pH值的萌发率(图1)。
2.3 培养基对有害疣孢霉厚垣孢子萌发的影响
有害疣孢霉厚垣孢子在WA培养基上未萌发,在MuEA培养基、MuDA培养基、PDA培养基和V8培养基上的萌发率分别为6.38%、8.43%、1.33%和6.23%,有害疣孢霉厚垣孢子在MuDA培养基上萌发率最好,显著优于其他供试培养基上的萌发率(图2)。
2.4 碳源对有害疣孢霉厚垣孢子萌发的影响
有害疣孢霉厚垣孢子在葡萄糖、蔗糖、麦芽糖、D-乳糖、海藻糖、山梨糖、D-棉子糖、肌醇和甘露醇上均可萌发,但萌发率有差异。有害疣孢霉厚垣孢子在葡萄糖、蔗糖和山梨糖的萌发率差异不显著,均显著优于麦芽糖、海藻糖、肌醇、甘露醇和不加碳源的萌发率。在加入肌醇和甘露醇的MuDA培养基上有害疣孢霉厚垣孢子的萌发率仅为6.13%和5.43%,不利于其萌发(图3)。
2.5 氮源对有害疣孢霉厚垣孢子萌发的影响
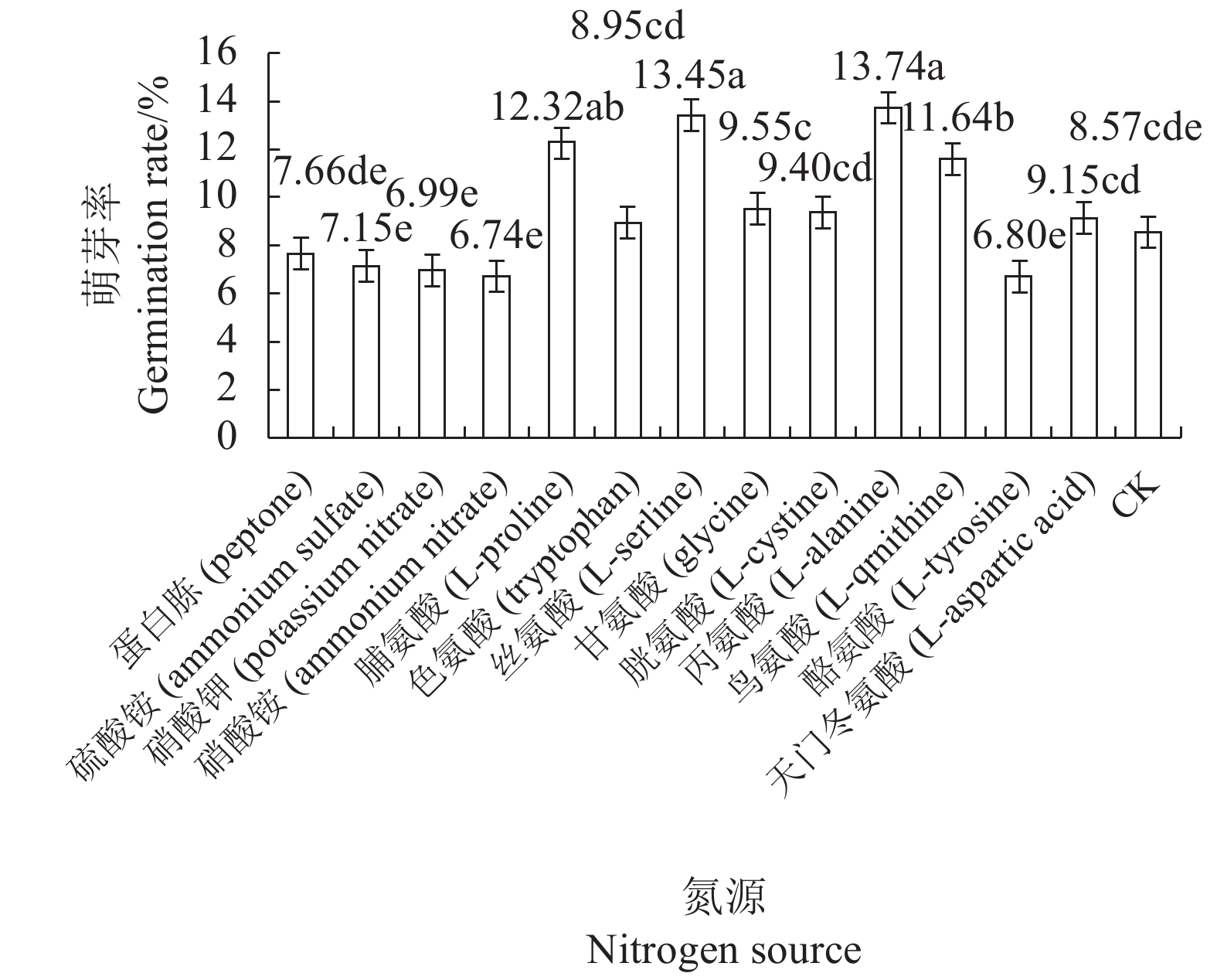
有害疣孢霉厚垣孢子在加入蛋白胨、硫酸铵、硝酸钾、硝酸铵、脯氨酸(L-proline)、色氨酸(tryptophan)、丝氨酸(L-serline)、甘氨酸(glycine)、胱氨酸(L-cystine)、丙氨酸(L-alanine)、鸟氨酸(L-qrnithine)、酪氨酸(L-tyrosine)和天门冬氨酸(L-aspartic acid)的MuDA培养基上均可萌发,加入脯氨酸、丝氨酸、丙氨酸和鸟氨酸后萌发率分别为12.32%、13.45%、13.74%和11.64%,显著优于不加任何氮源的对照处理(CK)的萌发率,而其他供试氮源对有害疣孢霉厚垣孢子的萌发无显著促进作用(图4)。
3. 讨论与结论
丝状真菌在其无性生长周期内可产生3种繁殖体,即菌丝体、分生孢子和厚垣孢子,其中厚垣孢子是菌体细胞原生质收缩、外面包裹厚壁的有抵抗能力的孢子[22],这种结构对真菌的生长和存活具有特别重要的意义。疣孢霉的菌丝、分生孢子和厚垣孢子均可致病,而厚垣孢子通常具有耐干燥、耐低温、耐土壤抑制作用、生存周期长和不易受环境影响的特点[11, 22-23]。真菌产生的厚垣孢子有休眠现象,未休眠的厚垣孢子通常容易萌发,稻曲病菌墨绿色的厚垣孢子不易萌发,需要破除休眠才能萌发,而黄褐色厚垣孢子易萌发,可在葡萄糖水溶液中萌发,25℃培养24 h的萌发率可达到50%以上[24-26];木霉产生的厚垣孢子极容易萌发,在水琼脂培养基上12 h就可以全部萌发[27]。疣孢霉厚垣孢子也存在休眠现象,休眠的厚垣孢子不易萌发,本研究中有害疣孢霉厚垣孢子在PDA培养基上几乎不萌发,这与王松的研究结果一致[28],在MuDA培养基上的萌发率最高,但萌发率仅为8.43%。Diana等报道疣孢霉厚垣孢子在MuEA培养基上可以获得20%~30%的萌发率,−5℃~10℃的温度下冷藏后可以将疣孢霉厚垣孢子的发芽水平提高到70%以上[18, 29],可见低温处理可以破除疣孢霉厚垣孢子的休眠。本研究的结果表明0℃和4℃的低温处理有助于疣孢霉厚垣孢子破除休眠,但并未获得70%以上的萌发率,其萌发率仅在10%左右,10℃冷藏不能起到破除休眠的作用。有害疣孢霉厚垣孢子在20℃、25℃长时间培养有少部分厚垣孢子萌发,萌发的厚垣孢子为刚成熟尚未进入休眠状态的厚垣孢子,这类似于稻曲病菌黄褐色厚垣孢子,不需要破除休眠。碳源和氮源对有害疣孢霉厚垣孢子的萌发有影响,其中葡萄糖、蔗糖和山梨糖适合其萌发,而脯氨酸、丝氨酸、丙氨酸和鸟氨酸则能显著提高其萌发率,但即使在MuDA培养基上加入适合的碳源或氮源,并在4℃的低温处理破除休眠后,有害疣孢霉厚垣孢子的萌发率仍然没有达到20%,如何进一步提高其萌发率,仍有待研究。
Smith研究表明疣孢霉顶端细胞极少通过其基底孔萌发,胚芽管通常直接从厚的细胞壁上萌发出来[30]。Diana 称这一特征令人费解,因为顶端细胞基底孔为原生质体的侵入物,并被非实质性的塞子堵塞[18],本研究中观察到疣孢霉厚垣孢子下细胞容易脱落,脱落下细胞的厚垣孢子萌发时不能判断是否是从顶端细胞基底孔萌发,同时观察到少量下细胞未脱落的厚垣孢子从顶端细胞的底孔萌发芽管的现象,这与Smith的描述有一定差异,这可能与菌株的特性有关。
-
表 1 温度对有害疣孢霉厚垣孢子萌发率的影响
Table 1 Effect of temperature on germination rate of M. perniciosa chlamydospores
(单位: %) 温度
Temperature萌发率 Germination rate 萌发率 Germination rate 萌发率 Germination rate 12 h/12 h 12 h/24 h 12 h/48 h 24 h/12 h 24 h/24 h 24 h/48 h 48 h/12 h 48 h/24 h 48 h/48 h −80 ℃/25 ℃ 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k −20 ℃/25 ℃ 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0 ℃/25 ℃ 0.00 k 2.75 gh 6.40 de 0.00 k 4.70 f 7.36 c 0.00 k 5.76 e 7.44 c 4 ℃/25 ℃ 0.71 jk 2.68 gh 6.77 cd 1.45 ij 8.40 b 9.23 a 1.40 ij 9.79 a 9.62 a 10 ℃/25 ℃ 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 15 ℃/25 ℃ 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 0.00 k 20 ℃/25 ℃ 0.00 k 0.00 k 0.72 jk 0.00 k 0.66 jk 0.95 jk 0.96 j 1.24 ij 1.43 ij 25 ℃/25 ℃ 0.00 k 0.00 k 1.38 ij 0.00 k 1.25 ij 2.36 h 1.53 ij 1.98 hi 3.25 g 注:数据后不同小写字母分别表示在5%水平上差异显著。
Note: Data with lowercase letters indicate significant difference at P<0.05. -
[1] TU C C, LIAO Y M. Major diseases of cultivated mushroom and their control in Taiwan [J]. Mushroom Science, 1989, 12: 615−626.
[2] FORER L B, WUEST P J, WAGNER V R. Occurrence and economic impact of fungal diseases of mushrooms in Pennsylvania [J]. The Plant Disease Reporter, 1974, 58: 987−991.
[3] 吴菊芳, 支月娥, 康素珍, 等. 蘑菇褐腐病菌生物学特性和防治 [J]. 植物保护学报, 1996, 23(3):235−240. DOI: 10.3321/j.issn:0577-7518.1996.03.009 WU J F, ZHI Y E, KANG S Z., et al Study on the biological characters and the control of Mycogone perniciosa Magn. [J]. Journal of plant protection, 1996, 23(3): 235−240.(in Chinese) DOI: 10.3321/j.issn:0577-7518.1996.03.009
[4] 周春元. 双孢蘑菇湿泡病病原学及其致病机理研究[D]. 长春: 吉林农业大学, 2014. ZHOU C Y. The Etiology and pathogenic mechanisms of mycogone perniciosa causing wet bubble disease on Agaricus bisporus[D]. Changchun: Jilin agricultural university, 2014.
[5] 魏景超. 真菌鉴定手册[M]. 上海: 上海科学技术出版社, 1979: 521-522. [6] GERRITE J P G. The influence of water in the preparation of mushroom compoat and its control [J]. Mushroom Science, 1972, 8: 43−47.
[7] 黄清铧, 王松, 张扬, 等. 有害疣孢霉菌与双孢蘑菇的互作关系 [J]. 菌物学报, 2014, 33(2):440−448. HUANG Q H, WANG S, ZHANG Y, et al. The interactions between mycogone perniciosa and Agaricus bisporus [J]. Mycosystema, 2014, 33(2): 440−448.(in Chinese)
[8] 周春元, 李玉. 双孢蘑菇不同品种感染有害疣孢霉后防御酶活性变化 [J]. 菌物学报, 2015, 34(3):504−510. ZHOU C Y, LI Y. Changes of defensive enzyme activities in different Agaricus bisporus varieties after inoculation with Mycogone perniciosa [J]. Mycosystema, 2015, 34(3): 504−510.(in Chinese)
[9] 张春兰, 徐济责, 李丹, 等. 有害疣孢霉与不同食用菌的培养关系 [J]. 西北农林科技大学学报, 2017, 45(1):112−118. ZHANG C L, XU J Z, LI D, et al. Cultivating relationship between Mycogone perniciosa and edible mushrooms [J]. Journal of Northwest A&F University(Natural Science Edition), 2017, 45(1): 112−118.(in Chinese)
[10] 张春兰, 徐济责, 柿岛真, 等. 双孢蘑菇疣孢霉病的发病过程及病原菌的核相研究 [J]. 微生物学报, 2017, 57(3):422−433. ZHANG C L, XU J Z, MAKOTO K, et al. The development of Agaricus bisporus wet bubble disease and the nuclear phase of pathogen [J]. Acta Microbiologica sinica, 2017, 57(3): 422−433.(in Chinese)
[11] ZHANG L, JIANG X L, YANG X Y, et al. Inhibition of chlamydospore germination and mycelial growth of Trichoderma spp. by chemical fungicides [J]. Agricultural Science & Technology, 2015, 16(7): 1494−1499.
[12] UMAR M H, GEELS F P, VAN GRIENSVEN L J L D. Pathology and pathogenesis of Mycogone perniciosa infection of Agaricus bisporus [J]. Mushroom Science, 2000, 15: 561−567.
[13] 王玉霞, 温志强, 林秋萍, 等. 福建省主要蘑菇产区疣孢霉菌生物学特性研究 [J]. 菌物学报, 2007, 26(S1):448−454. WANG Y X, WEN Z Q, LIN Q P, et al. Studies on biological characteristices of Mycogone perniciosa from main production areas of mushroom in Fujian [J]. Mycosysterna, 2007, 26(S1): 448−454.(in Chinese)
[14] 曾宪森, 李开本, 林兴生. 蘑菇疣孢霉病发生及综合防治研究 [J]. 福建农业学报, 2001, 16(4):13−17. DOI: 10.3969/j.issn.1008-0384.2001.04.004 ZENG X S, LI K B, LIN X S. Occurrence and integrated control of the Agaricus bisporus wet bull caused by Mycogone perniciosa magn [J]. Fujian Journal of Agricultural Sciences, 2001, 16(4): 13−17.(in Chinese) DOI: 10.3969/j.issn.1008-0384.2001.04.004
[15] FLETCHER J T, JAFFE B, MUTHUMEENASKSHI S, et al. Variations in isolates of Mycogone perniciosa and in disease symptoms in Agaricus bisporus [J]. Plant Pathol, 1995, 44: 130−140. DOI: 10.1111/j.1365-3059.1995.tb02725.x
[16] MANNING K, WOOD D A. Production and regulation of extracellular endocellulase by Agaricus bisporus [J]. Journal of General Microbiology, 1983, 129: 1839−1847.
[17] GEA F J, TELLO J C, NAVARRO M J. Efficacy and effects on yield of different fungicides for control of wet bubble disease of mushroom caused by mycoparasite Mycogone perniciosa [J]. Crop Prot, 2010, 29: 1021−1025. DOI: 10.1016/j.cropro.2010.06.006
[18] DIANA M H, MARY L P, COOKE R C, et al. Germination of bicellular conidia of mycogone perniciosa, the wet bubble pathogen of the cultivated mushroom [J]. Transactions of the british mycological society, 1985, 85(4): 730−735. DOI: 10.1016/S0007-1536(85)80272-2
[19] 侯颖, 徐建强, 宋宇州, 等. 三种杀菌剂对牡丹黑斑病菌菌丝生长及分生孢子萌发的影响 [J]. 植物保护学报, 2014, 41(3):367−371. HOU Y, XU J Q, SONG Y Z, et al. Effects of carbendazim' difenoconazole and azoxystrobin on mycelial growth and conidial germination of Alternaria suffruticosae [J]. Journal of plant protection, 2014, 41(3): 367−371.(in Chinese)
[20] 任海英, 戚行江, 梁森苗, 等. 环境因子对杨梅凋萎病菌分生孢子萌发及侵染的影响 [J]. 果树学报, 2015, 32(3):474−480. REN H Y, QI X J, LIANG S M, et al. Effects of environmental factors on conidial germination and infection of Pestalotiopsis spp. causing twig blight disease of bayberry(Myrica rubra) in China [J]. Journal of Fruit Science, 2015, 32(3): 474−480.(in Chinese)
[21] URBEZ-TORRES J R, BRUEZ E, HURTADO J, et al. Effect of temperature on conidial germination of Botryosphaeriaceae species infecting grapevines [J]. Plant disease, 2010, 94(12): 1476−1484. DOI: 10.1094/PDIS-06-10-0423
[22] 董佩佩, 孙漫红, 李世东, 等. 粉红螺旋聚孢霉67-1厚垣孢子生物学特性的研究 [J]. 菌物学报, 2014, 33(6):1242−1252. DONG P P, SUN M H, LI S D, et al. Biological characteristics of chlamydospores of Clonostachys rosea 67-1 [J]. Mycosystema, 2014, 33(6): 1242−1252.(in Chinese)
[23] BEAGLE-RISTAINO J E, PAPAVIZAS G C. Survival and proliferation of Trichoderma spp. and Gliocladium virens in soil and in plant rhizospheres [J]. Phytopathology, 1985, 75(6): 729−732. DOI: 10.1094/Phyto-75-729
[24] 李卫平, 王洪凯, 林福呈. 稻曲病菌厚垣孢子的萌发特性 [J]. 浙江农业学报, 2008, 20(4):278−281. DOI: 10.3969/j.issn.1004-1524.2008.04.013 LI W P, WANG H K, LIN F C. Germination characteristics of chlamydospore of Usilaginoidea virens [J]. Acta Agriculturae Zhejiangensis, 2008, 20(4): 278−281.(in Chinese) DOI: 10.3969/j.issn.1004-1524.2008.04.013
[25] 王国良. 影响稻曲病菌厚垣孢子萌发因素的研究 [J]. 植物保护学报, 1988, 15(4):241−245. WANG G L. Studies on the factors influencing the germination of the chlamydospores of Ustilaginoides virens [J]. Journal of plant protection, 1988, 15(4): 241−245.(in Chinese)
[26] 樊荣辉, 王永强, 刘兵, 等. 稻绿核菌无性孢子形成过程及厚垣孢子萌发率测定 [J]. 菌物学报, 2010, 29(2):188−192. FAN R H, WANG Y Q, LIU B, et al. The process of asexual spore formation and examination of chlamydospore germination of Ustilaginoidea virens [J]. Mycosystema, 2010, 29(2): 188−192.(in Chinese)
[27] 邹勇. 木霉厚垣孢子的产生、萌发和保存条件研究[D]. 雅安: 四川农业大学, 2006. ZOU Y. Study on the conditions of production germination and storage of chlamydospore of Trichoderma spp.[D]. Ya’an: Sichuan agricultural university, 2006.
[28] 王松. 有害疣孢霉菌(Mycogone perniciosa Magn)对双孢蘑菇致病机制的研究[D]. 福州: 福建农林大学, 2012. WANG S. Preliminary research of the pathogenicity mechanism of Mycogone perniciosa Magn to Agaricus bisporus[D]. Fuzhou: Fujian agriculture and forestry university, 2012.
[29] VINCENT-DAVIES, STEPHEN. Relationships between Mycogone perniciosa (Magnus) and its host Agaricus bisporus (Sing.), the cultivated mushroom[D]. Bath: University of Bath, 1973.
[30] SMITH, F E V, B. SC Three diseases of cultivated mushrooms [J]. Transactions of the british mycological society, 1924(10): 81−97.
-
期刊类型引用(1)
1. 方香玲,许世洋,南志标. 尖孢镰刀菌苜蓿专化型厚垣孢子的诱导形成方法及萌发特性. 草业学报. 2024(07): 130-141 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载: