Using SSR Markers from Brassica juncea Transcriptome for Germplasm Analysis
-
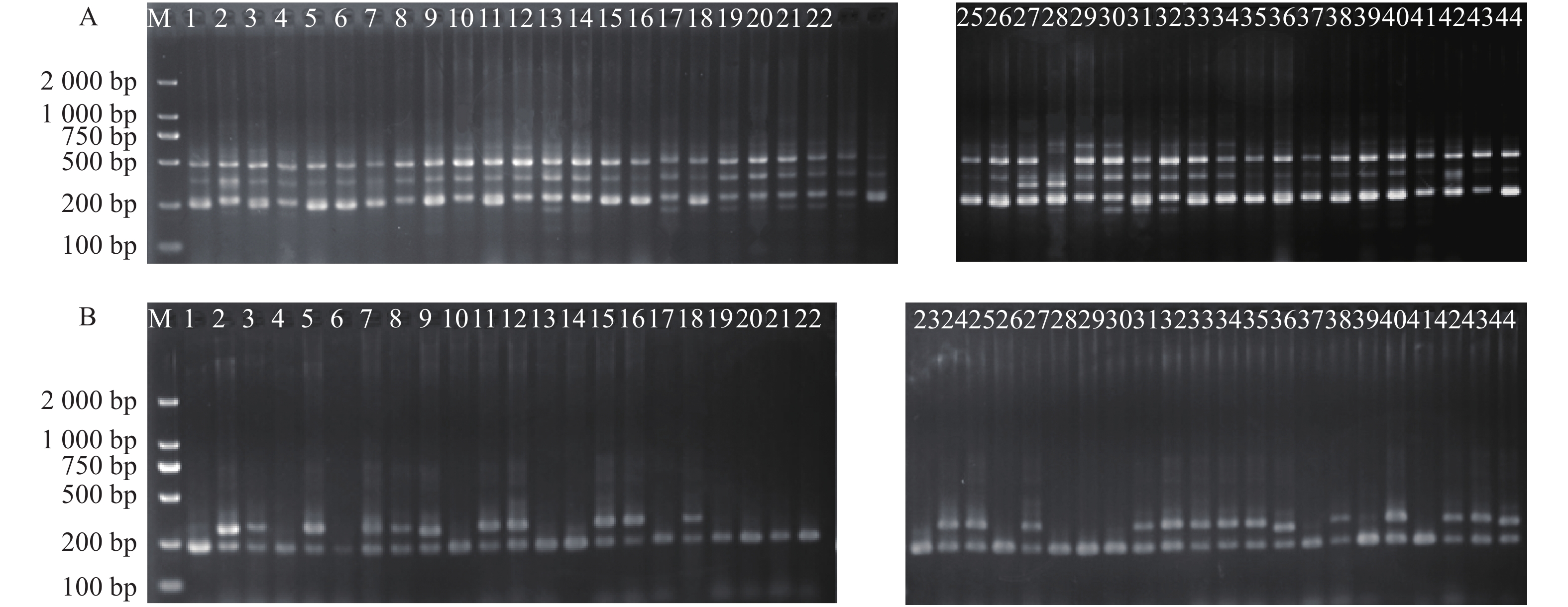
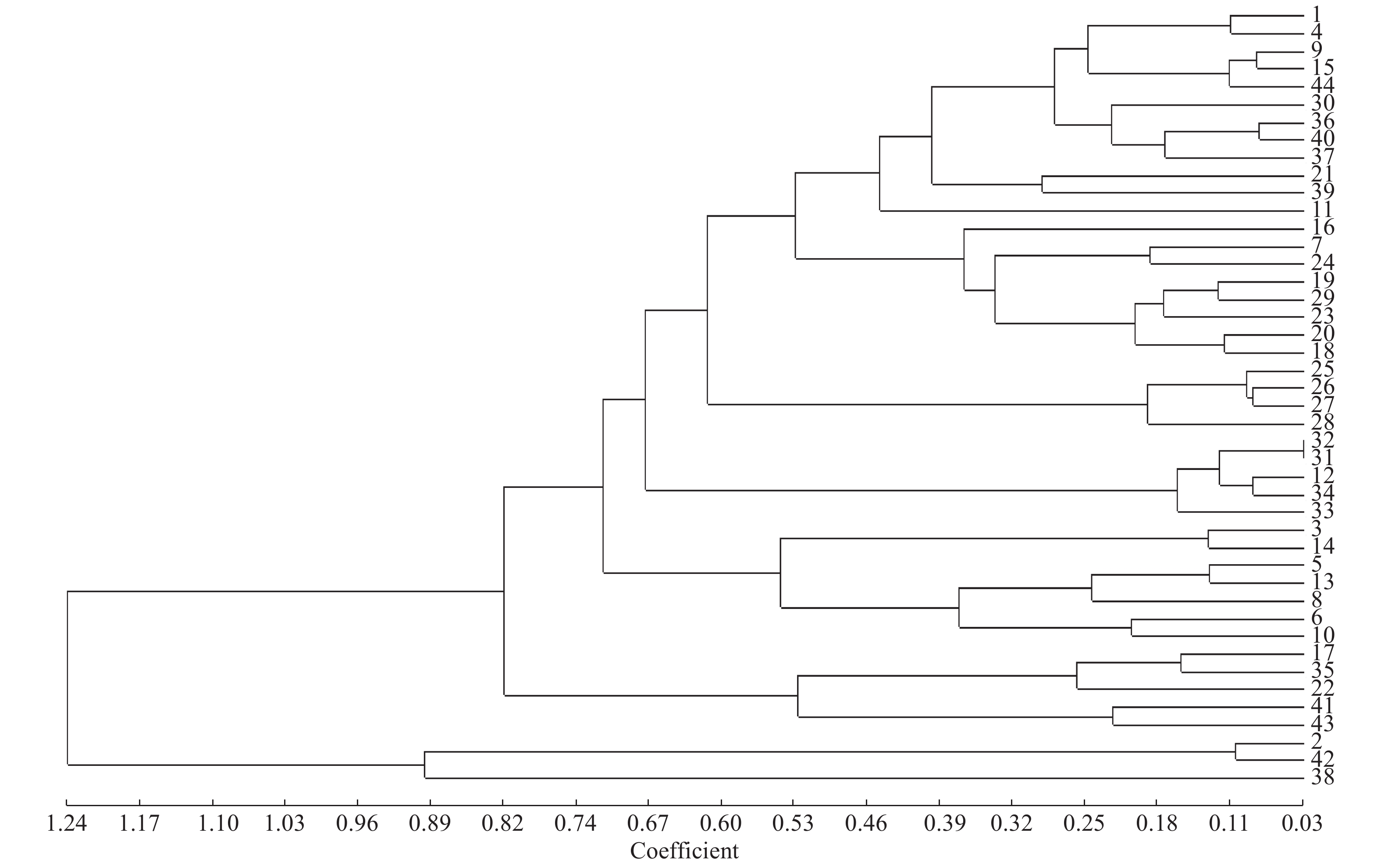
摘要:目的 为开发高效的芥菜Brassicajuncea.分子标记。方法 本研究通过对芥菜转录组测序的信息搜索SSR位点并分析其分布特点,应用Primer 3.0软件设计SSR引物,随机选择 50 对引物扩增44 份芥菜种质,检测其多态性。结果 芥菜转录组测序共获得55 636条unigene,全部序列有48 193 376 bp;有7 834条unigene包含SSR的序列,从中鉴定出9 526个SSR位点,其中有1 371条序列包含1个以上SSR,复合SSR有572个,SSR发生频率为14.08%。优势重复基序为三核苷酸和二核苷酸,分别占总SSR的51.12%和41.91%。二核苷酸重复基元中以AG/CT为优势重复基元,占总位点的34.74%,三核苷酸重复基元以AAG/CTT为主,占总位点的18.30%。共设计出21 282对SSR引物,随机选择 50 对引物进行 PCR 扩增,其中41对扩增出清晰可重复的预期条带,17对(占34%)在 44 份芥菜种质中表现出多态性。应用UPGMA得到将44份供试材料分为4大类聚类图,可准确地体现了芥菜种质材料的关系。结论 根据芥菜转录组数据能开发出类型丰富、效率较高的SSR标记,为芥菜亲缘关系分析和遗传图谱构建等提供更可靠的标记。Abstract:Objective To search for applicable molecular markers for studying Brassica juncea.Method SSR sites were searched from transcriptional sequencing of B. juncea. Potential primers were designed using Primer 3.0, and polymorphisms of 44 B. juncea germplasms detected from randomly selected 50 pairs of primers for the investigation.Result Totally, 55,636 unigenes were obtained from the transcriptome sequencing. The entire sequence was 48,193,376bp with 9,526 SSR loci identified from 7,834 unigenes at a rate of 14.08%. Of the loci, 1,371 contained more than one SSR locus and 572 compound loci. Of the major repeat types, 51.12% were trinucleotide dominated by AGA/TCT (18.30%), and 41.91% dinucleotide dominated by AG/CT (34.74%). Using Primer 3.0, from 21,282 pairs of SSR primers, 50 were randomly selected for the PCR amplification. Out of 44 amplifications, 41 showed clear and reproducible bands, and 17 with polymorphisms. The 44 germplasms were classified into 4 distinctive groups by UPGMA.Conclusion The SSR markers with high frequency and polymorphism could be acquired from the transcriptome to be used for the genetic diversity analysis and mapping construction on B. juncea.
-
Keywords:
- Brassica juncea /
- transcriptome /
- simple sequence repeat /
- polymorphism
-
0. 引言
【研究意义】植物种质资源的收集与保存是植物研究重要内容,其中超低温保存作为植物组织和细胞长期保存的理想方法,尤其适合营养繁殖作物的茎尖或分生组织的保存,具有直接再生完整小植株、减少遗传变异等优点[1]。海棠是蔷薇科(Rosaceae)苹果属(Malus)中果径较小(≤5 cm)的落叶乔木或小乔木,其中观赏海棠(Malus sp.)观赏价值高,是重要的优质绿化树种,研究海棠茎尖超低温保存在生产上具有重要意义。【前人研究进展】超低温保存后较高的存活率和再生率是主要的技术目标,已有研究显示,玻璃化超低温保存中活性氧(Reactive oxygen species, ROS)诱导的氧化应激是引起植物材料冻存后存活率下降的原因之一,因此,可以采用外源抗氧化剂来保护机体在超低温保存中免受伤害,如过氧化氢酶(Catalase, CAT)[2]、超氧化物歧化酶(Superoxide dismutase, SOD)[3]等酶类抗氧化剂以及抗坏血酸(Ascorbic acid, AsA)[4]和谷胱甘肽(Glutathione, GSH)[5]等非酶类抗氧化剂,均可以有效降低ROS生成量,减少氧化应激的发生,显著改善超低温保存效果。此外,细胞程序性死亡(Programmed cell death, PCD)作为一种基因编码主动性的死亡方式,在植物超低温保存中也扮演了重要的角色,添加细胞凋亡抑制剂D-CHO[6]、NO供体(Sodium Nitroprusside, SNP)[7]和乙烯(乙烯利Ethephon, Eth)[8] 等抑制PCD发生的物质可以提高存活率。【本研究切入点】目前除了对苹果属一些种类有少量超低温保存[9-12],特别是涉及观赏海棠的超低温保存研究极少,而极具观赏价值的北美海棠品种之一——红丽海棠(Malus Red Splendor)超低温保存鲜见报道。【拟解决的关键问题】本文以红丽海棠茎尖为试材,研究其超低温保存技术程序,探讨添加不同含量的抗氧化剂及PCD抑制剂对茎尖超低温保存冻后存活率的影响,建立红丽海棠玻璃化超低温保存技术程序,为观赏海棠种质资源保存提供一种技术思路,并为抗氧化剂和PCD抑制剂在超低温保存中的应用提供参考。
1. 材料与方法
1.1 试验材料
供试材料为观赏海棠品种红丽,以健康且带有饱满腋芽的当年生枝条为外植体(采自国家植物园海棠栒子园),在1/2MS+1.5 mg·L−1 6BA+0.1 mg·L−1 IAA的培养基中诱导无菌苗,并于1/2MS+1.0 mg·L−1 6-BA+0.5 mg·L−1 IAA的培养基中进行继代培养,诱导和继代培养条件:(23±3)℃,光照强度40 μmol·m−2·s−1,光照时间14 h·d−1,取生长旺盛的组培苗用于超低温保存试验。
1.2 试验方法
1.2.1 茎尖玻璃化法超低温保存
根据初步预试验设置玻璃化超低温保存的基本程序,再采用“逐步单因子法”对关键环节进行优化。(1)预培养:将红丽组培苗切成5 mm左右的带顶芽茎段,分别接种在不同蔗糖浓度(0.1、0.3、0.5、0.7、0.9 mol·L−1)的MS培养基中4 ℃下培养2 d,然后继续下述程序:(2)装载(Loading):在双目解剖镜下,用镊子和手术刀切下带3~4片叶原基、大小为1.5~2.0 mm的茎尖;将切下的茎尖放入1.5 mL 装有1 mL MS溶液的离心管中,吸出离心管中的MS溶液,加入1 mL Loading溶液(2 mol·L−1丙三醇+0.4 mol·L−1蔗糖,蒸馏水配置,pH 5.8),在室温下静置处理30 min;(3)PVS2处理:吸出离心管中的Loading溶液,加入1mL PVS2溶液[30%(m/V)丙三醇+15 %(m/V)乙二醇+15%(m/V)二甲基亚砜+0.4 mol·L−1蔗糖,1/2MS盐溶液配置,pH 5.8],在0 ℃于冰浴中处理90 min;(4)液氮冻存:更换新的1 mL PVS2溶液后,封紧离心管口,立即投入液氮,冻存1 h;(5)化冻:将装有PVS2和茎尖的离心管从液氮中取出,迅速放入38 ℃水浴中化冻1 min;(6)去装载(Unloading):将离心管中的PVS2溶液吸出,加入Unloading溶液(用1/2MS盐溶液配置的1.2 mol·L−1蔗糖,pH 5.8)后在室温下震荡洗涤2次,每次10 min。然后用于存活率或恢复生长率测定。相关步骤示意图见图1。
![]() 图 1 茎尖玻璃化超低温保存及存活率检测A.红丽海棠组培苗;B.预培养;C.切取1.5~2.5 mm茎尖;D.茎尖在离心管中;E.经TTC染色变红(左)与未染色(右)的茎尖;F.冻后茎尖接种到恢复培养基中。Figure 1. Survival rate of post-cryopreservation shoot tipsA: Crabapple tissue culture; B: pre-culture; C: 1.5-2.5 mm cut of shoot tip; D: shoot tip segment in centrifugal tube; E: TTC stained red (left) and original (right) shoot tips; F: post-frozen shoot tips inoculated on recovery medium.
图 1 茎尖玻璃化超低温保存及存活率检测A.红丽海棠组培苗;B.预培养;C.切取1.5~2.5 mm茎尖;D.茎尖在离心管中;E.经TTC染色变红(左)与未染色(右)的茎尖;F.冻后茎尖接种到恢复培养基中。Figure 1. Survival rate of post-cryopreservation shoot tipsA: Crabapple tissue culture; B: pre-culture; C: 1.5-2.5 mm cut of shoot tip; D: shoot tip segment in centrifugal tube; E: TTC stained red (left) and original (right) shoot tips; F: post-frozen shoot tips inoculated on recovery medium.关键环节的优化:在获得适宜预培养蔗糖浓度基础上,分别设置不同预处理时间(1、2、3 d),不同Loading溶液处理时间(0、10、20、30、40 min)和不同PVS2溶液处理时间(0、30、60、90、120 min),每个优化环节之前的步骤采用上一步已优化的处理方法,之后的步骤采用上述基本程序,直至完成所有关键环节的优化。每处理10~15个茎尖,重复3次。
1.2.2 存活率测定
采用氯化三苯基四氮唾(TTC)法检测冻存后茎尖的存活率。将经过Unloading溶液处理的茎尖置于含0.4%(m/V)的TTC溶液的离心管中,再放入37 ℃的水浴中黑暗处理30 min,将茎尖取出后,置于体视显微镜下,观察其染色情况。顶端分生组织被染红的茎尖记为存活的茎尖,而未被染红的茎尖记为死亡的茎尖。存活率/%=(被染红的茎尖/所有经过TTC处理的茎尖)×100%。每处理10~15个茎尖,重复3次。
1.2.3 恢复生长率测定
将经过液氮保存后的茎尖接种于MS培养基中暗培养2周后,然后转入正常光照条件(与组织培养的条件相同)下培养,茎尖长叶记为恢复生长。每处理10~15个茎尖,重复3次。
1.2.4 外源抗氧化剂和PCD抑制剂的添加
在建立的玻璃化超低温保存程序的基础上,根据课题组前人研究结果[4, 7-8, 13],分别在预培养基中添加Eth(100、200、400、800 mg·L−1);在Loading溶液中添加CAT,使其终浓度分别为50、100、200、400 U·mL−1和硝普钠(SNP),使其终浓度分别为50、100、200、1000 μmol·L−1;在PVS2溶液中添加GSH,使其终浓度分别为0.04、0.08、0.16、0.32 μmol·L−1;在Unloading溶液中添加AsA,使其终浓度分别为100、200、400、600 μmol·L−1,各处理均以原溶液为对照。
1.2.5 数据处理及分析
采用SPSS 26.0和Excel软件分别对试验数据进行单因素方差分析和数据整理、图表绘制。
2. 结果与分析
2.1 红丽海棠茎尖玻璃化超低温保存程序的建立
2.1.1 预培养基蔗糖浓度对液氮冻存后茎尖存活率的影响
将红丽海棠带顶芽茎段分别在含0.1、0.3、0.5、0.7、0.9 mol·L−1蔗糖的预培养基上进行2 d的培养,之后采用后续的基本程序,测定液氮冻存后茎尖存活率。如图2所示,茎尖冻后存活率随蔗糖浓度的升高先上升再下降,0.3 、0.5 、0.7 mol·L−1蔗糖浓度培养的茎尖存活率没有显著差异,但0.7 mol·L−1蔗糖浓度的预培养基上茎尖冻后存活率最高,为76.54%,显著高于0.1 、0.9 mol·L−1蔗糖浓度。因此红丽海棠超低温保存程序中预培养基的最适蔗糖浓度为0.7 mol·L−1,浓度过低过高则会降低茎尖的存活率。
2.1.2 预处理时间对液氮冻存后茎尖存活率的影响
将带顶芽的红丽海棠茎段接种于含0.7 mol·L−1蔗糖的预培养基上,在4 ℃条件下分别培养1 、2 和3 d,继续超低温保存基本程序的后续环节,液氮冻存后红丽茎尖存活率见图3。随预处理时间的增加,茎尖存活率逐渐升高,在2 d时存活率最高达到79.24%,后又下降。表明液氮冻后茎尖存活率受预培养环节冷锻炼时间的影响,适宜时长可以提高茎尖的抗冻能力。
2.1.3 Loading溶液处理时间对液氮冻存后茎尖存活率的影响
红丽海棠茎段在含0.7 mol·L−1蔗糖浓度的预培养2 d后,将茎尖分别在Loading溶液中处理不同时间,继续超低温保存基本程序的后续环节,从液氮取出化冻后茎尖存活率的结果如图4所示。Loading处理20 min时茎尖存活率最高,为60.61%,而随着处理时间的继续延长逐渐下降,处理40 min时的茎尖存活率为0。因此,Loading溶液处理时间不宜过长,否则可能会造成茎尖过度脱水而降低存活率。红丽海棠茎尖超低温保存的适宜Loading处理时间为20 min。
2.1.4 PVS2溶液处理时间对液氮冻存后茎尖存活率的影响
红丽海棠茎段在4 ℃下,含0.7 mol·L−1蔗糖浓度的预培养基上培养2 d后,Loading溶液处理20 min,分别采用PVS2溶液处理不同时间,继续超低温保存基本程序的后续环节,结果如图5。未经PVS2溶液处理的茎尖全部死亡,说明PVS2处理对玻璃化超低温保存过程起着至关重要的作用,随处理时间的增加,茎尖冻后存活率逐渐升高,处理90 min时茎尖存活率最高,为62.88%,后随时间的延长而显著下降。红丽海棠茎尖超低温保存PVS2处理适宜时间为90 min。
2.2 外源添加剂对茎尖超低温保存效果的影响
2.2.1 预培养环节添加外源Eth对液氮冻存后茎尖存活率的影响
在红丽海棠茎尖超低温保存中预培养环节添加4个质量浓度的外源Eth,继续超低温保存优化后的后续环节,茎尖冻后存活率见图6。添加100~400 mg·L−1与对照没有显著差异,200 mg·L−1时存活率稍高,而100 、400 mg·L−1时存活率稍低,而质量浓度过高时(800 mg·L−1)存活率显著下降。说明在预培养环节导入200 mg·L−1Eth时可能起到一定保护作用,小幅度提高冻后存活率,高浓度反而会导致其存活率降低。
2.2.2 Loading环节添加外源CAT或SNP对液氮冻存后茎尖存活率的影响
采用预培养优化方案后,在Loading环节添加不同浓度的外源CAT,之后继续超低温保存优化后的后续环节,茎尖液氮冻存后存活率见图7。添加200 U·mL−1时,茎尖的存活率最高,为86.67%,显著高于其他处理;含量为50 U·mL−1稍有提高,但差异不显著,其余含量显著下降。由此可知,Loading环节添加适宜浓度的外源CAT浓度可以发挥抗氧化保护作用,显著提高茎尖冻后存活率。
采用预培养优化方案后,在Loading环节添加不同浓度的外源SNP,之后继续超低温保存优化后的后续环节,茎尖超低温保存后存活率如图8所示。各浓度处理后冻后存活率均下降,但添加100和1000 μmol·L−1SNP时与对照无明显差异,而添加50和200 μmol·L−1SNP时存活率显著下降,相比对照分别降低了23.25%和13.25%。表明对PCD有拮抗作用的SNP在这里没有显示其作用。
2.2.3 PVS2环节添加外源GSH对液氮冻存后茎尖存活率的影响
采用优化的预培养和Loading方案后,在PVS2环节添加不同浓度的外源GSH,之后继续超低温保存后优化的后续环节,茎尖液氮冻存后存活率见图9。添加各种浓度的GSH,较对照均显著提高了茎尖冻后的存活率,其中导入浓度为0.04 μmol·L−1时存活率最高,为94.19%。由此表明,在PVS2环节导入外源GSH可有效发挥抗氧化保护作用,提高存活率。
2.2.4 Unloading环节添加外源AsA对液氮冻存后茎尖存活率的影响
采用优化的保存程序后,在Unloading环节导入不同浓度的外源AsA,茎尖超低温保存后存活率如图10所示,除200 μmol·L−1存活率下降外,其余浓度均可提高冻后存活率,效果最好的浓度为400 μmol·L−1,说明外源AsA起到了一定的抗氧化保护作用,小幅度提高了存活率。
2.3 红丽海棠茎尖超低温保存后恢复培养
采用优化后的超低温保存程序,在PVS2环节添加0.04 μmol·L−1的外源GSH,之后继续超低温保存后优化的后续环节,并进行恢复培养。没有添加GSH的对照组恢复生长率为16.67%,添加0.04 μmol·L−1外源GSH的恢复生长率为41.39%,提高了24.73%。
3. 讨论
冷锻炼能够提高植物茎尖的抗冻能力[14],通过在含有一定浓度的高糖、山梨醇或DMSO的培养基中培养植物茎尖,可以显著提高冻存后茎尖的存活率[15]。在大部分苹果属玻璃化超低温保存中,都至少需要3~4周的4 ℃或5 ℃的冷锻炼[16-19]。本试验通过4 ℃预培养,起到冷锻炼作用,预培养2 d,超低温保存后的茎尖存活率可到79.24%。在苹果属其他茎尖超低温保存的研究中,有不使用Loading处理直接脱水处理[20-22],本试验不经Loading溶液处理也可达到36.11%的存活率,但经Loading溶液处理20 min的茎尖冻后存活率更高,因为装载阶段是实现玻璃化而脱水处理的过渡阶段,能够避免高浓度玻璃化溶液引起的剧烈渗透变化导致的材料损伤。另外在本试验中0 ℃条件下PVS2处理90 min后茎尖冻后存活率最高,也有研究在室温下进行脱水处理,如将苹果品种嘎啦、望山红在室温下用PVS2处理30 min[10]或40 min[11]后再生率分别为55.6%和17.9%,但Uragami等[23]认为低温能降低玻璃化溶液的高渗作用导致的植物损伤,因此在大多数植物的超低温研究中,玻璃化步骤均在0 ℃下进行[24, 25]。
ROS是需氧生物中细胞有氧代谢的副产物,在正常状态下,机体可以在ROS的产生和清除之间保持动态平衡,但当ROS在逆境胁迫下产生过量时,自身的抗氧化系统,包括CAT、SOD和POD等酶类,以及AsA和GSH等非酶类系统会协同作用清除抵抗ROS可能带来的伤害,但当抗氧化能力不足以清除过量的ROS时,机体就会出现氧化应激。这启发研究人员们通过导入外源抗氧化剂来抵御氧化损伤,研究证明外源CAT[4, 13, 26]、AsA[4, 27]和GSH[6]均有抑制氧化应激的作用。本研究结果也显示,外源抗氧化剂CAT、AsA和GSH可以提高红丽海棠茎尖冻后存活率,说明外源抗氧化剂可能抑制了ROS造成的氧化损伤。3种外源抗氧化剂在不同环节中使用,分别提高了红丽海棠茎尖冻后存活率20.28%、6.75%、27.61%。
PCD作为一种自发性、有序的细胞死亡方式,受基因调控,是生物生活的基本过程。多项研究表明植物PCD存在于植物的各个生长发育过程及植物对非生物胁迫的响应中[28]。有研究显示超低温保存中预培养是PCD的一个信号起始环节,PCD相关调控基因显著上调[7],由于细胞凋亡存在一定的延迟性,预培养后的Loading环节也成为超低温保存中PCD研究的另一重要环节。本试验在预培养和Loading环节添加了PCD抑制剂,结果显示预培养环节添加外源Eth只是小幅度提高了红丽海棠茎尖冻后存活率,而在Loading环节添加外源SNP冻后存活率反而下降了,SNP通过抑制PCD信号分子NO而其作用,而NO调控PCD具有双重作用,可以促进PCD的发生[29, 30],也可以抑制PCD的发生[31, 32],而添加环节对NO在PCD发生的作用也十分关键,如在春石斛类原球茎中预培养环节导入NO供体(SNP)促进了PCD的发生,降低了存活率,而在Loading环节添加则抑制了PCD的发生[7],故推测外源SNP对不同的植物和不同添加环节可能有不同的影响效果。
4. 结论
红丽海棠茎尖采用以下程序可以实现超低温保存:取组培苗4~5 mm带顶芽茎段,接种在含0.7 mol·L−1蔗糖的预培养基,4 ℃冰箱培养2 d;切取1.5~2.0 mm的茎尖,Loading溶液室温下处理20 min;PVS2溶液0 ℃下处理90 min,可存入液氮保存;需用时将其取出放入38 ℃水浴快速化冻1 min;在室温下Unloading溶液震荡洗涤2次,每次10 min;进行恢复培养,存活率为66.58%,恢复生长率为16.67%。在Loading、PVS2和Unloading环节导入适宜浓度的抗氧化物质CAT、GSH、AsA可明显提高冻后存活率,最佳添加量分别为200 U·ml−1、0.04 μmol·L−1和400 μmol·L−1,较对照存活率分别提高了20.28%、27.61%和6.75%,而添加PCD抑制剂没有显示明显作用
-
表 1 44份芥菜种质材料主要性状
Table 1 Major properties of 44 B. juncea germplasms
编号
Code品种名称
Cultivar品种来源
Source株型
Plant type叶特征(叶形、叶面光滑与否、有无刺毛、蜡粉)
Leaf characteristics(leaf shape, smooth or not, with or without bristles, wax powder)抽䑓性
Bolting property结球性(是/否)
Heading ability(Y/N)食用器官
Edible organ1 龙岩青皮芥菜
Longyan Green Mustard福建龙岩市
Fujian Longyan直立
Upright卵圆形、皱、无刺毛、无蜡粉
Ovoid, wrinkled, spineless, no wax powder中
Medium否
No茎
Stem2 连城紫芥菜
Liancheng Pulse Purple Mustard福建龙岩市
Fujian Longyan开展
Expansion阔椭圆、微皱、无刺毛、有蜡粉
Broad oval, slightly wrinkled, spineless, wax powder中
Medium否
No叶
Leaf3 抗热四季
ok甜芥菜
Hot Resistant Four Seasons OK Sweet Mustard广西横县
Guangxi Hengxian直立
Upright阔椭圆、平滑、无刺毛、有蜡粉
Broad oval, smooth, spineless, wax powder早
Early否
No叶
Leaf4 华517 Hua517 湖北武汉市
Hubei Wuhan直立
Upright倒卵、微皱、无刺毛、无蜡粉
Obovate, slightly wrinkled, spineless, no wax powder中
Medium否
No茎
Stem5 厦门芥菜
Xiamen Mustard福建龙岩市
Fujian Longyan开展
Expansion扇形、皱、无刺毛、有蜡粉
Fan-shaped, wrinkled, spineless, wax powder中
Medium否
No叶
Leaf6 华515 Hua515 华中农大
Central China Agricultural University开展
Expansion阔椭圆、皱、无刺毛、无蜡粉
Broad oval, wrinkled, spineless, no wax powder中
Medium否
No叶
Leaf7 平和芥菜
Pinghe Mustard福建龙岩市
Fujian Longyan直立
Upright椭圆、微皱、无刺毛、有蜡粉
Oval, slightly wrinkled, spineless, wax powder中
Medium否
No叶
Leaf8 特选竹芥菜
Selected Bamboo Mustard广东广州市
Guangdong Guangzhou直立
Upright阔椭圆、平滑、无刺毛、有蜡粉
Broad oval, smooth, spineless, wax powder早
Early否
No叶
Leaf9 龙岩长茎芥菜2
Longyan Long stem Mustard 2北京市
Beijing直立
Upright卵圆形、皱、无刺毛、无蜡粉
Ovoid, wrinkled, spineless, no wax powder中
Medium否
No茎
Stem10 细叶雪里蕻
Spire Potherb Mustard福建龙岩市
Fujian Longyan半直立
Semi-upright倒披针、平滑、无刺毛、有蜡粉
Inverted lanceolate, smooth, spineless, wax powder中
Medium否
No叶
Leaf11 龙岩芥菜3
Longyan Mustard 3福建龙岩市
Fujian Longyan半直立
Semi-upright倒卵、皱、无刺毛、有蜡粉
Obovate, wrinkled, spineless, wax powder中
Medium否
No茎
Stem12 客家甜芥菜
Kejia Mustard广东兴宁市
Guangdong Xingning半直立
Semi-upright阔椭圆、平滑、无刺毛、有蜡粉
Broad oval, smooth, spineless, wax powder早
Early否
No叶
Leaf13 四季甜客家芥
Four-season sweet hakka Mustard江西宜春市
Jiangxi Yichun直立
Upright阔椭圆、平滑、无刺毛、有蜡粉
Broad oval, smooth, spineless, wax powder早
Early否
No叶
Leaf14 本地大菜
Local Mustard广东兴宁市
Guangdong Xingning直立
Upright倒卵、皱、无刺毛、有蜡粉
Obovate, wrinkled, spineless, wax powder早
Early否
No叶
Leaf15 张白土茎用芥菜
Zhangbaitu stem Mustard福建龙岩市
Fujian Longyan直立
Upright卵圆形、皱、无刺毛、无蜡粉
Ovoid, wrinkled, spineless, no wax powder中
Medium否
No茎
Stem16 漳州芥菜2
Zhangzhou Mustard福建龙岩市
Fujian Longyan直立
Upright倒卵、皱、无刺毛、有蜡粉
Obovate, wrinkled, spineless, wax powder早
Early否
No叶
Leaf17 特选大坪埔大肉包心芥菜
Specially selected Dapingpu big meat stuffed mustard广西横县
Guangxi Hengxian开展
Expansion扁圆、皱、无刺毛、无蜡粉
Oval, wrinkled, spineless, no wax powder中
Medium是
Yes叶球
Leaf Bulb18 广东鸡那菜
Guangdong jina Mustard福建龙岩市
Fujian Longyan直立
Upright倒披针、微皱、无刺毛、有蜡粉
Inverted lanceolate, slightly wrinkled, spineless, wax powder早
Early否
No叶
Leaf19 美口宽杆芥菜
Meikou Mustard甘肃省武威市
Gansu Wuwei开展
Expansion卵圆、皱、无刺毛、有蜡粉
Ovoid, wrinkled, spineless, wax powder晚
Later否
No叶
Leaf20 闽清大芥菜
Minqin big Mustard福建福州市
Fujian Fuzhou半直
Upright倒卵、微皱、无刺毛、无蜡粉
Obovate, slightly wrinkled, spineless, no wax powder中
Medium否
No叶
Leaf21 精品大肉大坪包心芥
Premium Dapingpu big meat stuffed Mustard江西宜春市
Jiangxi Yichun开展
Expansion扁圆、皱、无刺毛、有蜡粉
Oval, wrinkled, spineless, wax powder中
Medium是
Yes叶球
Leaf Bulb22 台湾芥菜1
Taiwan Mustard福建龙岩市
Fujian Longyan半直立
Semi-upright长倒卵、平滑、无刺毛、无蜡粉
Long obovate, smooth, spineless, no wax powder中
Medium否
No叶
Leaf23 宽帮青菜
Wide petiole Mustard四川省绵阳市
Sichuan Mianyang开展
Expansion阔椭圆、微皱、无刺毛、有蜡粉
Broad oval, slightly wrinkled, spineless, wax powder中
Medium否
No叶
Leaf24 四川大肉青
Sichuan big meat Mustard四川省广汉市
Sichuan Guanghan开展
Expansion阔倒卵、皱、无刺毛、有蜡粉
Broad oval, wrinkled, spineless, wax powder中
Medium否
No叶
Leaf25 华513 Hua513 湖北武汉市
Hubei Wuhan开展
Expansion倒卵、微皱、有刺毛、无蜡粉
Obovate, slightly wrinkled, spine, no wax powder中
Medium否
No叶
Leaf26 华512 Hua512 湖北武汉市
Hubei Wuhan开展
Expansion阔椭圆、微皱、有刺毛、无蜡粉
Broad oval, slightly wrinkled, spine, no wax powder中
Medium否
No叶
Leaf27 华516 Hua516 湖北武汉市
Hubei Wuhan开展
Expansion阔椭圆、微皱、有刺毛、有蜡粉
Broad oval, slightly wrinkled, spine, wax powder中
Medium否
No叶
Leaf28 上杭毛芥菜
Shanghang Hairy Mustard福建龙岩市
Fujian Longyan半直立
Semi-upright卵圆形、微皱、有刺毛、无蜡粉
Ovoid, slightly wrinkled, spine, no wax powder中
Medium否
No叶球
Leaf Bulb29 宽叶厚肉高脚芥
Broadleaf Thick Meat Tall Mustard广东兴宁市
Guangdong Xingning直立
Upright倒卵、微皱、无刺毛、有蜡粉
Obovate, slightly wrinkled, spine, wax powder中
Medium否
No叶
Leaf30 连城芥菜
Liancheng Mustard福建龙岩市
Fujian Longyan直立
Upright卵圆形、皱、无刺毛、有蜡粉
Ovoid, wrinkled, spineless, wax powder中
Medium否
No茎
Stem31 香港客家甜芥菜
Hong Kong Hakka Sweet Mustard广东兴宁市
Guangdong Xingning半直立
Semi-upright阔椭圆、平滑、无刺毛、有蜡粉
Broad oval, smooth, spineless, wax powder极早
Very Early否
No叶
Leaf32 福州宽杆芥菜
Fuzhou Wide pole Mustard福建福州
Fujian Fuzhou半直立
Semi-upright阔椭圆、皱、无刺毛、有蜡粉
Broad oval, slightly wrinkled, spineless, wax powder中
Medium否
No叶
Leaf33 闽清大挂菜
Minqing Large Mustard福建福州
Fujian Fuzhou半直立
Semi-upright倒卵、微皱、无刺毛、有蜡粉
Obovate, slightly wrinkled, spine, wax powder中
Medium否
No叶
Leaf34 特选甜脆客家芥菜
Special sweet and crisp Hakka Mustard广东深圳市
Guangdong Shenzhen半直立
Semi-upright阔椭圆、平滑、无刺毛、有蜡粉
Broad oval, smooth, spineless, wax powder极早
Very Early否
No叶
Leaf35 皱叶芥
Crinkle Mustard福建龙岩市
Fujian Longyan直立
Upright阔椭圆、皱、无刺毛、无蜡粉
Broad oval, smooth, spineless, wax powder中
Medium是
Yes叶球
Leaf Bulb36 永定客家芥
Yongding Mustard福建龙岩市
Fujian Longyan直立
Upright卵圆形、皱、无刺毛、有蜡粉
Ovoid, wrinkled, spineless, wax powder中
Medium否
No茎
Stem37 万安客家芥菜
Wanan Mustard福建龙岩市
Fujian Longyan直立
Upright倒卵、微皱、无刺毛、有蜡粉
Obovate, slightly wrinkled, spine, wax powder中
Medium否
No茎
Stem38 桂林甜芥菜薹
Guilin Mustard Stalk广西横县
Guangxi Hengxian开展
Expansion阔椭圆、平滑、无刺毛、无蜡粉
Broad oval, smooth, spineless, no wax powder中
Medium是
Yes叶、花
Leaf and Flower 薹
Bolting39 绿欣芥菜
Luxin Mustard福建龙岩市
Fujian Longyan直立
Upright倒卵、皱、无刺毛、有蜡粉
Obovate, wrinkled, spine, wax powder中
Medium否
No茎
Stem40 龙芥1号
Long Mustard 1福建龙岩市
Fujian Longyan直立
Upright卵圆形、皱、无刺毛、有蜡粉
Ovoid, wrinkled, spineless, wax powder中
Medium否
No茎
Stem41 大排芥菜
Dapai Mustard福建龙岩市
Fujian Longyan直立
Upright阔椭圆、微皱、无刺毛、有蜡粉
Broad oval, slightly wrinkled, spineless, wax powder中
Medium是
Yes叶球
Leaf Bulb42 紫脉芥
Purple vein Mustard福建龙岩市
Fujian Longyan开展
Expansion倒卵、皱、无刺毛、有蜡粉
Obovate, wrinkled, spine, wax powder中
Medium否
No叶
Leaf43 台湾芥菜2 Taiwan Mustard 2 福建龙岩市
Fujian Longyan开展
Expansion阔倒卵、微皱、无刺毛、有蜡粉
Broad oval, slightly wrinkled, spineless, wax powder中
Medium是
Yes叶球
Leaf Bulb44 龙岩长茎芥菜
Longyan Long stem Mustard福建龙岩市
Fujian Longyan直立
Upright卵圆形、皱、无刺毛、有蜡粉
Ovoid, wrinkled, spineless, wax powder中
Medium否
No茎
Stem表 2 芥菜SSR的类型分布
Table 2 Distribution of SSR types in B. juncea
SSR类型
SSR type重复次数 Repeat number 总计
Total比例/%
Ratio4 5 6 7 8 9 10 11~14 ≥ 15 二核苷酸 Di 0 0 1 510 1 011 645 362 226 134 104 3 992 41.91 三核苷酸 Tri 0 3 108 1 185 403 78 20 32 29 15 4 870 51.12 四核苷酸 Tetra 273 55 17 5 1 0 1 0 0 308 3.70 五核苷酸 Penta 99 24 6 1 2 0 0 1 0 122 1.40 六核苷酸 Hexa 133 34 4 4 2 0 0 2 0 183 1.87 总计 Total 505 3 221 2 722 1 424 728 382 259 166 119 9 526 比例% Ratio 5.30 33.82 28.57 14.95 7.64 4.01 2.72 1.74 1.25 100 表 3 芥菜转录中不同SSR重复基序出现的频率
Table 3 Frequency of different SSR repeat motifs in B. juncea transcriptome
SSR类型
SSR type重复基序种类数
Repeat species重复基序类型
Repeat motif type数量
Number发生频率/%
Frequency比例/%
Proportion二核苷酸 Di 4 AG/CT 3 309 34.74 82.89 AC/GT 388 4.07 9.72 AT/AT 291 3.05 7.29 CG/CG 4 0.04 0..10 三核苷酸 Tri 10 AAG/CTT 1743 18.30 35.79 AGG/CCT 827 8.68 16.98 ATC/ATG 740 7.77 15.20 AAC/GTT 461 4.84 9.47 ACC/GGT 390 4.09 8.00 AGC/CTG 320 3.36 6.57 CCG/CGG 138 1.45 2.83 ACG/CGT 94 0.99 1.93 ACT/AGT 83 0.87 1.70 AAT/ATT 74 0.78 1.52 四核苷酸 Tetra 25 AAAG/CTTT 74 0.78 24.02 AAAC/GTTT 68 0.71 22.08 AAGG/CCTT 41 0.43 12.99 AATC/ATTG 40 0.43 12.99 其他 Other 85 0.89 27.60 五核苷酸 Penta 41 AAGAG/CTCTT 14 0.15 11.48 AATCG/ATTCG 13 0.14 10.66 AAAAC/GTTTT 12 0.13 9.84 其他 Other 83 0.87 68.03 六核苷酸 Hexa 92 AAGGAG/CCTTCT 15 0.16 8.20 AAGAGG/CCTCTT 12 0.13 6.56 AAAAAC/GTTTTT 10 0.10 5.46 其他 Other 146 1.53 79.78 表 4 芥菜17对SSR多态性引物信息
Table 4 Information on 17 pairs of SSR primers for studying polymorphism of B. juncea
引物名称
Primer name引物序列(5′→3′)
Primer sequenceSSR基元
SSR motif产物长度/bp
Length of product多态条带数
Number of polymorphic bands多态信息量
PICBaSSR002 TCACCGAGCTTCTTCGTCTT/CTCCTTTCTATTCGGTTGCG (AG)9 235 3 0.54 BaSSR003 TGACTTGGGCCAAAGCTTAC/CACTTCTCTTTCGGGTCCAG (AG)20 247 3 0.63 BaSSR007 CCTCTCCGAATCAAGTCTCG/TGTTAAACCTCAACCTCGCA (AG)9 286 1 0.43 BaSSR009 GGGAACATACATATCAGATTGTGG/TTCCCACAGAAGCCATTCTC (AG)23 225 3 0.67 BaSSR012 ACGAAACCCCAGAAGAAAGC/GATCATTCCTCCCCTCTTCC (AGA)7 181 3 0.71 BaSSR013 AAAGTGGAACCCTGTGAACG/AATCGGCGGTAACTCCTTCT (GAA)8 264 2 0.58 BaSSR015 TGGATAAGGGAACAAGGCTG/GAAGATTCACGAGCTCCAGG (GCT)8 241 3 0.58 BaSSR016 AGCACCTCACCAAACTGGAC/CAACAGTTCCAGCAGCTTCA (TGC)8 169 2 0.53 BaSSR019 GAAGTCTTTGCGATTGAGAAAAA/TCCCATTGTACACGACCCTT (GAA)15 280 4 0.72 BaSSR020 CAAAAAGTGGGTTCGAGGAG/CGCAAAACTCTTCCTTCCAC (AAG)7 238 3 0.71 BaSSR022 CATCACCTAACCGATTGCCT/TCTTGTTTCTGTGGCGTGAG (AACC)6 131 3 0.70 BaSSR023 GTCGAGAGAACCTTTCGTGC/GCCCATATCAGCCTCGTTTA (TTTC)7 257 2 0.51 BaSSR032 TAAGGAAGGCGAAAGTTGGA/AGAGAATCAGCTTCCCGTCA (TTGGT)7 249 2 0.53 BaSSR037 GATTCTCTTTCGCGATTCGT/ATCTTGTTTTCGCCCTGACA (TTTGG)6 278 2 0.53 BaSSR043 TAGCTGCAGCAACAATCGTC/GATGTGCAAGCAAGGATTGA (AAAAG)5 217 2 0.47 BaSSR045 TCCATCTGAACGGTTCTTTG/CATAGATCCATTGCTTAGCGG (CTGTTA)6 185 2 0.50 BaSSR046 CACGAATGTGAAGCAGCAGT/GTAGCCAGGTCGTGGTTGTT (CACCCA)5 277 6 0.82 -
[1] 刘佩瑛. 中国芥菜[M]. 北京: 农业出版社, 1996: 47. [2] VAUGHAN J G, GORDON E I. A taxonomic study of Brassica juncea using the techniques of electrophoresis, gas-liquid chromatography and serology [J]. Annals of Botany, 1973, 37(1): 167−184. DOI: 10.1093/oxfordjournals.aob.a084670
[3] 孟秋峰, 王毓洪, 皇甫伟国, 等. 芥菜类蔬菜植物学性状鉴定及聚类分析 [J]. 浙江农业科学, 2006, 47(3):254−257. DOI: 10.3969/j.issn.0528-9017.2006.03.006 MENG Q F, WANG Y H, HUANGPU W G, et al. Identification and cluster analysis of botanical characters of Brassicajuncea [J]. Journal of Zhejiang Agricultural Sciences, 2006, 47(3): 254−257.(in Chinese) DOI: 10.3969/j.issn.0528-9017.2006.03.006
[4] KALIA R K, RAI M K, KALIA S, et al. Microsatellite markers: an overview of the recent progress in plants [J]. Euphytica, 2011, 177(3): 309−334. DOI: 10.1007/s10681-010-0286-9
[5] KUMAR B, KUMAR U, YADAV H K. Identification of EST–SSRs and molecular diversity analysis in Mentha piperita [J]. The Crop Journal, 2015, 3(4): 335−342. DOI: 10.1016/j.cj.2015.02.002
[6] 张瑞杰, 田蓉, 闫晋强, 等. 甘蓝种和芥菜型油菜细胞质的遗传多样性 [J]. 西北农业学报, 2012, 21(10):59−64. ZHANG R J, TIAN R, YAN J Q, et al. Cytoplasmic diversity of Brassica oleracea and Brassica juncea [J]. Acta Agriculturae Boreali-Occidentalis Sinica, 2012, 21(10): 59−64.(in Chinese)
[7] 高天翔, 蔡宇良, 冯瑛, 等. 中国樱桃14个自然居群遗传多样性和遗传结构的SSR评价 [J]. 园艺学报, 2016, 43(6):1148−1156. GAO T X, CAI Y L, FENG Y, et al. Genetic diversity and genetic structure of Prunus pseudocerasus populations from China as revealed by SSR markers [J]. Acta Horticulturae Sinica, 2016, 43(6): 1148−1156.(in Chinese)
[8] 赵振卿, 盛小光, 虞慧芳, 等. 花椰菜新品种浙801杂交种纯度的SSR鉴定 [J]. 长江蔬菜, 2011(18):18−20. DOI: 10.3865/j.issn.1001-3547.2011.18.006 ZHAO Z Q, SHENG X G, YU H F, et al. Hybrid purity identification of A new cauliflower cultivar Zhe 801 by SSR marker [J]. Journal of Changjiang Vegetables, 2011(18): 18−20.(in Chinese) DOI: 10.3865/j.issn.1001-3547.2011.18.006
[9] 李丽, 郑晓鹰. 用于白菜和大白菜品种鉴定的EST-SSR复合标记的建立 [J]. 园艺学报, 2009, 36(11):1627−1634. DOI: 10.3321/j.issn:0513-353X.2009.11.010 LI L, ZHENG X Y. The development of multiplex EST-SSR markers to identification Chinese cabbage[Brassica campestris chinensis (L.) Makino and Brassica campestris L. pekinensis(lour.) olsson]cultivars [J]. Acta Horticulturae Sinica, 2009, 36(11): 1627−1634.(in Chinese) DOI: 10.3321/j.issn:0513-353X.2009.11.010
[10] 张婉, 崔继哲, 于拴仓, 等. 白菜品种的SSR指纹图谱数据库的构建 [J]. 分子植物育种, 2013, 11(6):843−857. ZHANG W, CUI J Z, YU S C, et al. Construction of SSR fingerprint database of Chinese cabbage varieties(Brassica campestris L. ssp. Pekinensis) [J]. Molecular Plant Breeding, 2013, 11(6): 843−857.(in Chinese)
[11] 王庆彪, 张扬勇, 庄木, 等. 中国50个甘蓝代表品种EST-SSR指纹图谱的构建 [J]. 中国农业科学, 2014, 47(1):111−121. DOI: 10.3864/j.issn.0578-1752.2014.01.012 WANG Q B, ZHANG Y Y, ZHUANG M, et al. EST-SSR fingerprinting of fifty cabbage representative varieties from China [J]. Scientia Agricultura Sinica, 2014, 47(1): 111−121.(in Chinese) DOI: 10.3864/j.issn.0578-1752.2014.01.012
[12] 刘峰, 王运生, 田雪亮, 等. 辣椒转录组SSR挖掘及其多态性分析 [J]. 园艺学报, 2012, 39(1):168−174. LIU F, WANG Y S, TIAN X L, et al. SSR mining in pepper(Capsicum annuum L.) transcriptome and the polymorphism analysis [J]. Acta Horticulturae Sinica, 2012, 39(1): 168−174.(in Chinese)
[13] 李荣华, 王直亮, 陈静芳, 等. 菜薹转录组中SSR信息与可用性分析 [J]. 园艺学报, 2016, 43(9):1816−1824. LI R H, WANG Z L, CHEN J F, et al. Analysis of SSR information in transcriptome and their usability in flowering Chinese cabbage [J]. Acta Horticulturae Sinica, 2016, 43(9): 1816−1824.(in Chinese)
[14] 潜宗伟, 陈海丽, 崔彦玲. 菠菜转录组SSR位点分析及其分子标记的开发 [J]. 农业生物技术学报, 2016, 24(11):1688−1697. QIAN Z W, CHEN H L, CUI Y L. Analysis of the SSR loci and development of molecular markers in Spinacia oleracea transcriptome [J]. Journal of Agricultural Biotechnology, 2016, 24(11): 1688−1697.(in Chinese)
[15] 忻雅, 崔海瑞, 卢美贞, 等. 白菜EST-SSR信息分析与标记的建立 [J]. 园艺学报, 2006, 33(3):549−554. DOI: 10.3321/j.issn:0513-353X.2006.03.018 XIN Y, CUI H R, LU M Z, et al. Data mining for SSRs in ESTs and EST-SSR marker development in Chinese cabbage [J]. Acta Horticulturae Sinica, 2006, 33(3): 549−554.(in Chinese) DOI: 10.3321/j.issn:0513-353X.2006.03.018
[16] 陈琛, 庄木, 李康宁, 等. 甘蓝EST-SSR标记的开发与应用 [J]. 园艺学报, 2010, 37(2):221−228. CHEN C, ZHUANG M, LI K N, et al. Development and utility of EST-SSR marker in cabbage [J]. Acta Horticulturae Sinica, 2010, 37(2): 221−228.(in Chinese)
[17] 李满堂, 张仕林, 邓鹏, 等. 洋葱转录组SSR信息分析及其多态性研究 [J]. 园艺学报, 2015, 42(6):1103−1111. LI M T, ZHANG S L, DENG P, et al. Analysis on SSR information in transcriptome of On Ion and the polymorphism [J]. Acta Horticulturae Sinica, 2015, 42(6): 1103−1111.(in Chinese)
[18] LI D J, DENG Z, QIN B, et al. De novo assembly and characterization of bark transcriptome using Illumina sequencing and development of EST-SSR markers in rubber tree (Hevea brasiliensis Muell. Arg.) [J]. BMC Genomics, 2012, 13(1): 192. DOI: 10.1186/1471-2164-13-192
[19] YOU Y N, LIU D C, LIU H B, et al. Development and characterisation of EST-SSR markers by transcriptome sequencing in taro (Colocasia esculenta (L.) Schoot) [J]. Molecular Breeding, 2015, 35(6): 134. DOI: 10.1007/s11032-015-0307-4
[20] 王东, 曹玲亚, 高建平. 党参转录组中SSR位点信息分析 [J]. 中草药, 2014, 45(16):2390−2394. DOI: 10.7501/j.issn.0253-2670.2014.16.021 WANG D, CAO L Y, GAO J P. Data mining of simple sequence repeats in Codonopsis pilosula transcriptome [J]. Chinese Traditional and Herbal Drugs, 2014, 45(16): 2390−2394.(in Chinese) DOI: 10.7501/j.issn.0253-2670.2014.16.021
[21] 崔娜, 邱杨, 李锡香, 等. 萝卜EST资源的SSR信息分析及EST-SSRs标记开发 [J]. 园艺学报, 2012, 39(7):1303−1312. CUI N, QIU Y, LI X X, et al. Data mining for SSRs in EST rescources and EST-SSR markers development in radish [J]. Acta Horticulturae Sinica, 2012, 39(7): 1303−1312.(in Chinese)
[22] BISWAS M K, CHAI L J, MAYER C, et al. Exploiting BAC-end sequences for the mining, characterization and utility of new short sequences repeat (SSR) markers in Citrus [J]. Molecular Biology Reports, 2012, 39(5): 5373−5386. DOI: 10.1007/s11033-011-1338-5
[23] ZHAI L L, XU L, WANG Y, et al. Novel and useful genic-SSR markers from de novo transcriptome sequencing of radish (Raphanus sativus L.) [J]. Molecular Breeding, 2014, 33(3): 611−624. DOI: 10.1007/s11032-013-9978-x
[24] ZHANG H Y, WEI L B, MIAO H M, et al. Development and validation of genic-SSR markers in sesame by RNA-seq [J]. BMC Genomics, 2012, 13(1): 316. DOI: 10.1186/1471-2164-13-316
[25] WU J, CAI C F, CHENG F Y, et al. Characterisation and development of EST-SSR markers in tree peony using transcriptome sequences [J]. Molecular Breeding, 2014, 34(4): 1853−1866. DOI: 10.1007/s11032-014-0144-x
[26] 李永平, 刘建汀, 陈敏氡, 等. 利用黄秋葵转录组信息挖掘SSR标记及用于种质分析 [J]. 园艺学报, 2018, 45(3):579−590. LI Y P, LIU J T, CHEN M D, et al. SSR markers excavation and germplasm analysis using the transcriptome information of Hibiscus esculentus [J]. Acta Horticulturae Sinica, 2018, 45(3): 579−590.(in Chinese)
[27] XIANG X Y, ZHANG Z X, WANG Z G, et al. Transcriptome sequencing and development of EST-SSR markers in Pinus dabeshanensis, an endangered conifer endemic to China [J]. Molecular Breeding, 2015, 35(8): 158. DOI: 10.1007/s11032-015-0351-0
[28] TEMNYKH S. Computational and experimental analysis of microsatellites in rice (Oryza sativa L.): frequency, length variation, transposon associations, and genetic marker potential [J]. Genome Research, 2001, 11(8): 1441−1452. DOI: 10.1101/gr.184001
[29] SINGH H, DESHMUKH R K, SINGH A, et al. Highly variable SSR markers suitable for rice genotyping using agarose gels [J]. Molecular Breeding, 2010, 25(2): 359−364. DOI: 10.1007/s11032-009-9328-1
[30] BOTSTEIN D, WHITE R, SKOLNICK M, et al. Construction of a genetic linkage map in man using restriction fragment length polymorphisms [J]. Am J Hum Genet, 1980, 32(3): 314−331.
[31] 李宁, 司军, 任雪松, 等. 芥菜种质资源遗传多样性和亲缘关系的SRAP分析 [J]. 中国蔬菜, 2014(5):26−33. DOI: 10.3969/j.issn.1000-6346.2014.05.005 LI N, SI J, REN X S, et al. SRAP analysis of mustard germplasm genetic diversity and genetic relationship [J]. China Vegetables, 2014(5): 26−33.(in Chinese) DOI: 10.3969/j.issn.1000-6346.2014.05.005
[32] FU J. Genetic diversity and phylogenetic relationship among Chinese mustard as revealed by RAPD and microsatellite markers[D]. Hangzhou: Zhejiang University, 2005.(in Chinese)
[33] 齐晓花. 中国芥菜系统进化研究及重要数量性状的遗传分析[D]. 杭州: 浙江大学, 2009. Qi X H. Phylogeny of Chinese mustard and genetic analysis of important quantitative characters[D]. HangZhou: Zhejiang University, 2009. (in Chinese)
[34] 齐晓花. 中国芥菜系统进化研究及重要数量性状的遗传分析[D]. 杭州: 浙江大学, 2009. QI X H. Phylogenetic evolution and quantitative genetic analysis of major traits for Chinese vegetable mustard (Brassica juncea)[D]. Hangzhou: Zhejiang University, 2009.(in Chinese)[知网]
[35] 宋明, 刘婷, 汤青林, 等. 芥菜种质资源的RAPD和ISSR分析 [J]. 园艺学报, 2009, 36(6):835−842. DOI: 10.3321/j.issn:0513-353X.2009.06.009 SONG M, LIU T, TANG Q L, et al. Genetic diversity analysis of mustard germplasm based on RAPD and ISSR [J]. Acta Horticulturae Sinica, 2009, 36(6): 835−842.(in Chinese) DOI: 10.3321/j.issn:0513-353X.2009.06.009
-
期刊类型引用(1)
1. 戴惠新,吴金洋,张梦樵,张湘菊,吴丽娜. 喷涂机器人用改性聚天门冬氨酸酯腻子制备及性能测试. 粘接. 2024(12): 42-45 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载: