Prokaryotic Expression and Purification of JsMYB305 Transcription Factor in Jasminum sambac
-
摘要:目的 获得茉莉花香气调控转录因子JsMYB305的重组蛋白,为深入研究JsMYB305调控茉莉萜类香气代谢的分子机理及筛选其他互作蛋白提供基础。方法 通过酶切连接的方式,将JsMYB305的编码序列构建到原核表达载体pGEX-4T-1,转化BL21(DE3)表达菌株,通过IPTG诱导蛋白表达、GST亲和树脂分离纯化,最后Western Blot鉴定重组蛋白。结果 重组蛋白的诱导条件为0.2 mmol·L−1 IPTG,最适宜纯化的温度和时间为28 ℃诱导4 h,经20 mmol·L−1 GSH洗脱的蛋白纯度较好,Western Blot结果表明重组蛋白的大小正确。结论 成功获得了JsMYB305重组蛋白,为后期利用GST-pull down技术筛选互作蛋白及EMSA研究JsMYB305对特定启动子位点的结合提供基础。Abstract:Objective The recombinant protein of fragrance-regulating transcription factor JsMYB305 was obtained in preparation for studies on the molecular mechanism of terpenoid-regulation and interacting proteins of the gene in Jasminum sambac.Methods Coding sequence of JsMYB305 was constructed into prokaryotic expression vector pGEX-4T-1 by enzyme digestion and ligation, then, transformed into the BL21 (DE3) expressing strain. The protein expression was induced by IPTG, and the recombinant protein separated and purified using GST affinity resin followed by western blot for positive identification.Result After induction by 0.2 mmol·L−1 IPTG, the recombinant protein was purified at the optimized temperature of 28 ℃ for 4 h and eluted with 20 mmol·L−1 GSH for purification. The western blot confirmed the protein weight to be as expected.Conclusion The recombinant protein of JsMYB305 was successfully obtained to pave the way for further studies on the search for the interacting proteins by GST-pull down technique and the binding of the gene to specific promoter sites by EMSA.
-
0. 引言
【研究意义】鳄梨Persea americana Mill.,又称牛油果、油梨、酪梨、幸福果等,为樟科Lurcee鳄梨属Persea常绿落叶乔木[1]。鳄梨脂肪含量高,含有大量的酶,有健胃清肠的作用,并具有降低胆固醇和血脂、保护心血管和肝脏系统等重要生理功能,味如乳酪,有“森林黄油”之美称,是一种集营养与保健为一身的水果[2]。随着人们对鳄梨认识的提高,鳄梨需求量逐年大幅增长。2016年中国鳄梨进口量已达到42 510 t,是2012年进口量的14.8倍, 进口额达12 176.7万美元[3]。
鳄梨自然分布是以中美洲为中心,分布范围从热带的哥伦比亚至墨西哥南部的高山亚热带地区。根据原产地生态条件的不同,鳄梨主要分为3个种系,即危地马拉系、墨西哥系和西印度系。由于鳄梨的3个种系之间不存在杂交障碍,目前大多数商业鳄梨品种是这3个种系间的杂交种[4]。中国引进的资源主要是危地马拉系及其杂交种,云南、海南、广西、广东、福建、四川、浙江、贵州等省(区)都有种植,且种植面积和产量呈快速上升趋势。缅甸及云南等地现存丰富的鳄梨资源,经历了各种不良气候和病虫害侵袭,自然适者生存,迄今拥有良好的适应性、抗逆性以及其他多种优异性状。因此,系统开展缅甸及云南地区野生、半野生鳄梨种质资源的调查、收集、保存及利用,选育新品种,对促进产业健康发展和开发利用该地区独特鳄梨资源具有重要意义。
【前人研究进展】AFLP(扩增片段长度多态性)是限制性酶切与PCR扩增结合的一种分子标记技术,由荷兰科学家Zabeau[5]发明,是对DNA酶切片段存在的差异进行PCR扩增,进而产生片段多态性[6]。AFLP具有可靠性好,重复性强,可信度高等优点,广泛应用于建立鳄梨遗传图谱[7]、鳄梨根腐病[8]、鳄梨遗传多样性分析[9]等领域研究。【本研究切入点】尽管鳄梨产业发展迅速,但目前鳄梨产区栽培品种比较单一,中国90%以上种植美国选育的Hass(哈斯)品种,十分不利于产业的健康发展。【拟解决的关键问题】本研究搜集缅甸及云南等地鳄梨资源,调查滇缅鳄梨种质90份,采用AFLP标记对其进行遗传多样性分析,旨在明确鳄梨种质间的亲缘关系,为指导鳄梨新品种选育和种质创新研究提供借鉴。
1. 材料与方法
1.1 试验材料
试验材料共90份(表1),主要采集地点在滇缅边境地区,包括缅甸克钦邦的八莫、掸邦的南坎以及云南省西双版纳、德宏州、红河州、普洱及保山。
表 1 供试鳄梨种质资源信息Table 1. Avocado germplasms studied序号
Number种质编号
Germplasm code序号
Number种质编号
Germplasm code序号
Number种质编号
Germplasm code来源地:缅甸克钦邦八莫市
Origin: Bhamo, Kachin state,
Myanmar来源地:云南省普洱市孟连县
Origin: Menglian County, Pu'er City,
Yunnan Province62 EL0062 63 EL0063 64 EL0064 1 EL0001 32 EL0032 65 EL0065 2 EL0002 33 EL0033 来源地:云南省德保山市潞江坝
Origin: Lujiangba, Baoshan City,
Yunnan Province3 EL0003 34 EL0034 4 EL0004 35 EL0035 5 EL0005 36 EL0036 66 EL0066 6 EL0006 37 EL0037 67 EL0067 7 EL0007 38 EL0038 68 EL0068 8 EL0008 39 EL0039 69 EL0069 9 EL0009 40 EL0040 70 EL0070 10 EL0010 41 EL0041 来源地:云南省德宏州盈江县
Origin: Yingjiang County, Dehong Prefecture, Yunnan Province11 EL0011 42 EL0042 12 EL0012 43 EL0043 13 EL0013 71 EL0071 来源地:缅甸掸邦南坎
Origin: Namhkam, Shan State,
Myanmar来源地:云南省热带作物科学研究所
Origin: Yunnan Institute of
Tropical Crops72 EL0072 73 EL0073 74 EL0074 14 EL0014 44 EL0044 75 EL0075 15 EL0015 45 EL0045 76 EL0076 16 EL0016 46 EL0046 来源地:云南省德宏州瑞丽市
Origin: Ruili City, Dehong Prefecture,
Yunnan Province17 EL0017 47 EL0047 18 EL0018 48 EL0048 19 EL0019 49 EL0049 77 EL0077 20 EL0020 50 EL0050 78 EL0078 21 EL0021 51 EL0051 79 EL0079 22 EL0022 52 EL0052 80 EL0080 23 EL0023 53 EL0053 81 EL0081 来源地:云南省红河州元阳县
Origin: Yuanyang County, Honghe Prefecture, Yunnan Province54 EL0054 82 EL0082 55 EL0055 83 EL0083 56 EL0056 84 EL0084 24 EL0024 57 EL0057 85 EL0085 25 EL0025 来源地:云南省西双版纳州景洪县
Origin: Jinghong County, Xishuangbanna
Prefecture, Yunnan Province86 EL0086 26 EL0026 来源地:云南省德宏州芒市
Origin: Mangshi City, Dehong Prefecture,
Yunnan Province27 EL0027 28 EL0028 58 EL0058 87 EL0087 29 EL0029 59 EL0059 88 EL0088 30 EL0030 60 EL0060 89 EL0089 31 EL0031 61 EL0061 90 EL0090 1.2 基因组总DNA的提取
每种材料采取6个单株叶片混合,装入含有硅胶的自封袋,干燥后放入−20℃冰箱中,采用CTAB法[10]提取样品基因组DNA,0.8%琼脂糖凝胶电泳检测DNA质量及浓度,将样品稀释到20 ng·uL−1,−20℃保存备用。
1.3 主要试剂及引物
Taq 酶 (2 U·uL−1)、10×PCR buffer、dNTP (10 mmol· L−1)、引物(10 mmol·L−1)、内切酶(10 U·uL−1) (NEB公司)、T4DNA连接酶(5 U·uL−1) 购自NEB公司。Marker为DL2000、100 bp DNA Ladder,分子量内标为ROX500(ABI公司)。8对引物(3-2、3-3、3-6、4-2、7-1、7-3、9-2、10-2) 由北京鼎国昌盛生物技术有限责任公司合成,正向引物均为FAM标记,试验所用接头和引物信息见表2。
表 2 引物系列Table 2. Primer sequence接头与引物 Connector and primer 系列(5′-3′) Sequence Eco RI 接头1(Eco RI Connector 1) CTCGTAGACTGCGTACC Eco RI 接头2 (Eco RI Connector 2) AATTGGTACGCAGTCTAC Mse I 接头1 (Mse IConnector 1) GACGATGAGTCCTGAG Mse I 接头2 (Mse I Connector 2) TACTCAGGACTCAT 3-2引物 (3-2 primer) E-AAC/M-CAC 3-3引物 (3-3 primer) AAC/M-CAG 3-6引物 (3-6 primer) E-AAC/M-CTC 4-2引物 (4-2 primer) E-AAG/M-CAC 7-1引物 (7-1 primer) E-ACC/M-CAA 7-3引物 (7-3 primer) E-ACC/M-CAG 9-2引物 (9-2 primer) E-AGC/M-CAC 10-2引物 (10-2 primer) E-AGG/M-CAC 1.4 AFLP扩增及检测
首先选用6个鳄梨品种(1、15、25、40、60、70号)进行引物筛选,从24对引物中筛选出8对引物,然后进行90份材料的整体试验。
酶切-连接:对所选样品采用 EcoRⅠ/MseⅠ双酶切,酶切与连接反应同步进行。
(1)酶切与连接体系为: 10×Reacton buffer 2.5 uL, Adapter 1. 0 uL,Eco RI /Mse I 2 uL,10 mmol·L−1ATP 2.5 uL,T4 Ligase 1 uL,模板DNA 4 μL(50 ng·uL−1),补ddH2O至20 uL。酶切-连接反应条件为37℃保温5 h,8℃保温4 h,4℃过夜,1.5%琼脂糖凝胶电泳检测。
(2)预扩增反应体系:模板DNA 2 uL,Pre-ampmix(预扩引物)1 uL,dNTPs 1 uL,10×PCR buffer 2.5 uL,Tap酶0.5 uL,加ddH2O至25 uL。PCR扩增程序为94℃预变性2 min;94℃变性30 s;56℃复性30 s;72℃延伸80 s,30个循环。
(3)选择性扩增反应体系:Eco RI引物1 uL,Mse I引物1 uL,10×PCR buffer 2.5 uL,dNTP 0.5 uL,Taq酶0.5 uL,模板DNA 2 uL,加ddH2O至25 uL。PCR扩增程序为:95℃预变性5 min,94℃变性30 s,65℃复性30 s,72℃延伸80 s,12个循环,94℃变性30 s,55℃复性30 s,72℃延伸80 s,23个循环。
(4)将甲酰胺与分子量内标按100∶1的体积比混匀后,取9 uL加入上样板中,再加入1 uL稀释10倍的PCR产物,然后使用ABI377测序仪进行电泳检测。
1.5 数据分析
利用GENESCAN3.1软件将90份样品、8对引物组合扩增得到的原始数据进行分析,软件每2个碱基读取1次,Marker片段范围为70~500 bp,软件BinThere设置范围为69.5~501.5,一共读取216条条带,在原始数据基础上,有记作“1”,无则记为“0”,构成0,1数据矩阵。根据Nei等的方法[11-12],利用POPGENE 32软件分析有效等位基因数(Ne)、Nei’s基因多样性指数(H)和Shannon 信息指数(I)等。同时使用NTSYSpc-2.11F软件计算遗传相似系数(GS)[13],根据相似性系数进行UPGMA聚类分析[14]和PCA主效应分析。
2. 结果与分析
2.1 AFLP扩增条带的多态性及遗传多样性分析
选用8对AFLP引物组合对90份鳄梨种质资源进行扩增,结果见表3和图1。8对引物组合共扩增出1 165条带,其中多态性条带为1 163条,占总条带数的99.83%,表明利用这8对引物可以进行基因多态性检测,且90份鳄梨种质资源多态性较高;有效等位基因数(Ne)范围1.257 9~1.329 1个,平均1.294 4个;Nei’s基因多样性指数(H)范围0.188 5~0.225 8,平均0.209 5;Shannon 信息指数(I)范围0.325 0~0.374 3,平均0.353 0,具有较丰富的遗传多样性。
表 3 8对引物组合扩增的AFLP条带Table 3. Amplification bands with 8 pairs of AFLP primers引物组合
Primer pair总条带数
Total bands多态性条带数
Polymorphic bands多态性比率
Polymorphic rate/%有效等位基因数
NeNei’s基因多样性
HShannon’s多样性
IE-AAC/M-CAC 144 144 100 1.306 1 0.215 3 0.359 9 F-AAC/M-CAG 145 144 99.31 1.257 9 0.188 5 0.325 0 E-AAC/M-CTC 136 135 99.26 1.329 1 0.225 6 0.372 2 E-AAG/M-CAC 147 147 100 1.294 8 0.209 9 0.353 3 E-ACC/M-CAA 147 147 100 1.322 5 0.225 8 0.374 3 E-ACC/M-CAG 150 150 100 1.268 6 0.197 2 0.337 9 E-AGC/M-CAC 141 141 100 1.313 7 0.218 8 0.365 2 E-AGG/M-CAC 155 155 100 1.262 1 0.194 9 0.335 8 平均 Mean 145.63 145.38 99.83 1.294 4 0.209 5 0.353 0 总和 Total 1 165 1 163 2.2 聚类分析
根据遗传相似系数,用UPGMA法对90份鳄梨种质进行聚类分析(图2)。从图2可知,在相似性系数0.752处切割时,可划分为四大类群,第I类群有1份种质,采集于保山潞江坝70号;第II类群共有24份种质,其中包括20份采集于德宏的全部资源71~90号,此外还包括4份采集于保山的65、67、68、69号;第III类群有1份种质,采集于西双版纳 的景洪59号;第IV类群有64份种质。在相似性系数0.763处切割,可将IV类群划分为3个亚群(A、B和C)。A亚群包含1份采集于西双版纳云南省热带作物科学研究所的52号;B亚群包含27份种质,其中采集于缅甸的20份,红河元阳7份24~30号;C亚群包括36份种质,其中包括1份采集于红河元阳的31号,3份采集于缅甸八莫的1、3、4号,1份采集于保山潞江坝的77号,12份采集于普洱孟连、19份采集于西双版纳(12份采集于云南省热带作物科学研究所、7份采集于景洪)。
2.3 主效应分析
主效应分析显示了不同鳄梨种质的分类位置,结果如图3所示,将位置靠近的材料归为一类,可分为3个主要类群。其中2~30号共29份材料聚为一个类群,主要采集地为缅甸和红河;31~64号以及1号、66号和88号共37份材料聚在一个类群,主要采集地为普洱孟连和西双版纳;67~87号以及65、89、90号共24份材料聚在一个类群,主要采集地为保山和德宏。主效应分析结果与聚类分析结果基本一致,缅甸和红河元阳采集的资源聚为一类,普洱孟连和西双版纳采集的资源聚为一类,保山和德宏采集的资源聚为一类。集中在一个区域的种质亲缘关系较为紧密,1号虽然采集地为缅甸,但2种聚类结果都将其划分到普洱孟连和西双版纳一类,所以1号种质与孟连及西双版纳资种质的亲缘关系更为紧密。
3. 讨论与结论
3.1 AFLP分子标记是研究鳄梨遗传多样性的有效工具
具有丰富多样性的种质资源是果树育种的前提和重要基础,多种分子标记已应用于鳄梨的物种分类、亲缘关系鉴定、病毒检测、遗传特性评价及指纹图谱构建等领域[15-23]。利用AFLP分子标记是检测种质亲缘关系和种质资源遗传多样性的有效手段。Dohuan等[9]利用AFLP标记在83个鳄梨砧木品种中,共鉴定出61个多态性标记,并通过UPMGA进行遗传多样性分析和各基因型材料的聚类分析,将这些鳄梨砧木资源对根腐病的抗性分为易感、中度耐受、耐受和高度耐受等4类。Rodriguez等[24]利用AFLP、ISTR,SSR、同工酶标记以及形态标记共5种标记对17份鳄梨种质进行多态性水平分析,结果证明单独用AFLP或ISTR就可以将所有的材料鉴定出来。本试验利用8对AFLP引物组合共扩增出1 165条带,其中多态性条带为1 163条,占总条带数的99.83%,表明利用这8对引物可以进行基因多态性检测,Shannon多态性信息指数平均0.353 0,说明这些资源具有较丰富的遗传多样性。
3.2 聚类分析和主成分分析在鳄梨种质资源遗传多样性中的应用
本试验通过AFLP聚类分析得出,在相似系数为0.752时,将90份资源分为四大类,第I大类和第III大类各有1份种质,分别来源于保山潞江坝和西双版纳景洪,说明这2份资源的亲缘关系较其他材料较远,其中来自于保山潞江坝的70号果实具有较浓的苦味,相比其他资源品质特色,其苦味成分及含量有待下一步研究。第II类,共有24份种质,占总资源的26.67%,主要来源于德宏和保山,说明德宏和保山的资源亲缘关系较近。第IV大类群共有64份种质,占总资源的71.11%,在相似系数为0.763时,又可将其划分为3个亚群,其中A亚群只有1份材料来自于西双版纳的52号;B亚群共有27份材料,来源于缅甸和红河,说明采集于缅甸和红河的种质资源亲缘关系相对较亲密;C亚群共有36份材料,主要来源于普洱孟连和西双版纳,说明这2个地方的资源亲缘关系较近。从地理位置来说,德宏和保山相邻,普洱和西双版纳相邻,但红河和缅甸相隔较远,相反德宏、普洱和西双版纳都与缅甸接壤,但可能原因是红河引进的资源来源于缅甸。主成分分析结果和聚类分析结果相似,呈现明显的地域性分布规律,相同和相近地理来源的材料能聚在一起。
本研究系统开展了缅甸及云南地区野生、半野生鳄梨种质资源的调查、收集与保存。通过AFLP分子标记技术,综合分析了90份鳄梨资源的遗传多样性水平,为选育新品种促进产业健康可持续发展和开发利用该地区独特鳄梨资源奠定良好基础。
-
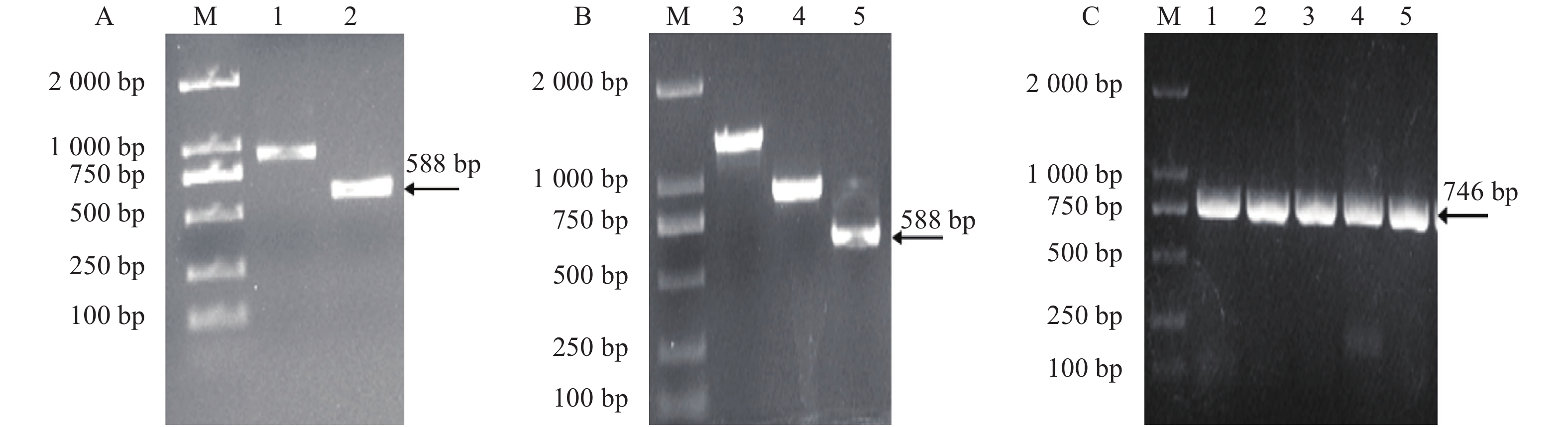
图 1 茉莉JsMYB305基因编码序列的扩增、酶切回收及菌液PCR鉴定
注:M为DL2000 Marker ;A为茉莉JsMYB305基因编码序列的扩增,其中2为JsMYB305基因;B为JsMYB305基因扩增产物酶切回收后的产物,其中5为目的基因,1、3、4为其他基因条带;C为重组载体pGEX-4T-1-JsMYB305的菌液PCR鉴定,1~5为阳性条带。
Figure 1. Amplification of JsMYB305 coding sequence, recovery of PCR product after enzyme digestion, and PCR identification of bacteria
Note: M: DL 2000 marker; A: amplification of JsMYB305 encoding sequence, 2: JsMYB305; B: amplification product of JsMYB305 after enzyme digestion and recovery; 5: JsMYB305; 1, 3, and 4: bands of other genes; C: identification of recombinant vector pGEX-4T-1-JsMYB305; 1-5: positive bands.
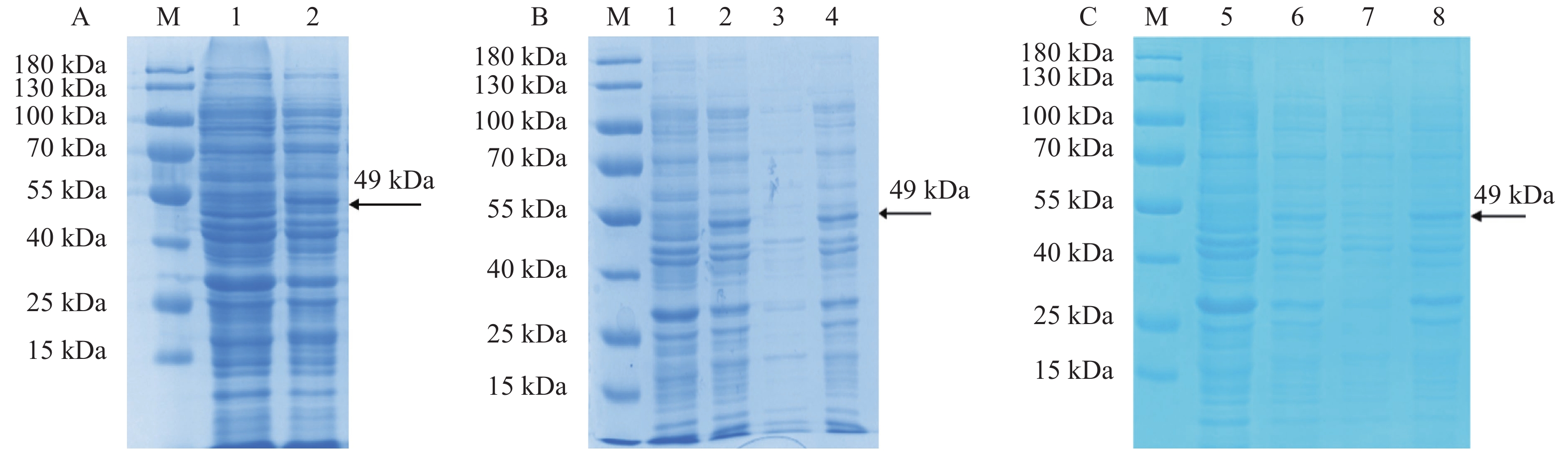
图 2 JsMYB305重组蛋白的诱导表达及可溶性检测
注:M:Protein ladder。A:JsMYB305重组蛋白的诱导表达,1:未诱导的菌体蛋白,2:0.2 mmol·L−1 IPTG诱导后的菌体蛋白。B:37 ℃诱导重组蛋白表达,1:未诱导的菌体蛋白;2、3、4分别为37 ℃ 0.2 mmol·L−1 IPTG诱导的菌体蛋白、上清、沉淀。C:28 ℃诱导重组蛋白表达,5:未诱导的菌体蛋白,6、7、8分别为28 ℃ 0.2 mmol·L−1 IPTG诱导的菌体蛋白、上清、沉淀。
Figure 2. Inducible expression and soluble detection of JsMYB
305 recombinant protein Note: M: protein ladder; A: induced expression of recombinant protein of JsMYB305; 1: uninduced bacterial protein; 2: bacterial protein induced by 0.2 mmol·L−1 IPTG; B: recombinant protein expression induced at 37 ℃; 1: uninduced bacterial protein; 2, 3 and 4: bacterial protein, supernatant, and precipitate, respectively, induced by 0.2 mmol·L−1 IPTG at 37 ℃; C: recombinant protein expression induced at 28 ℃; 5: uninduced bacterial protein; 6, 7, and 8: bacterial protein, supernatant, and precipitate, respectively, induced by 0.2 mmol·L−1 IPTG at 28 ℃.
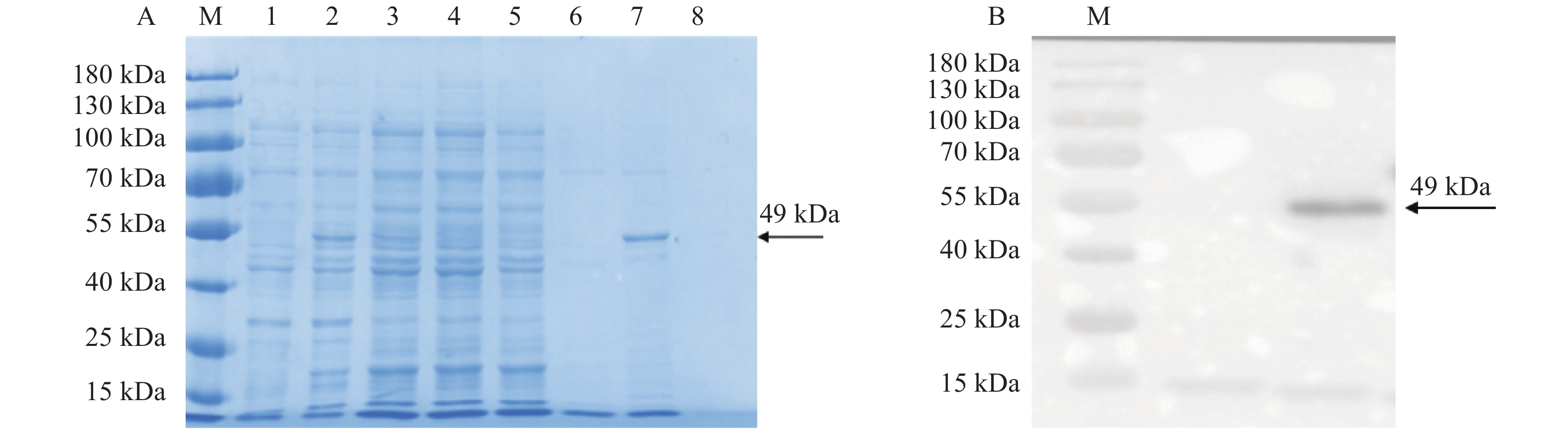
图 3 重组蛋白的纯化及Western Blot 检测
注:M:protein ladder 。A:重组蛋白的纯化 ,1:未诱导的菌体蛋白;2:0.2 mmol·L−1 IPTG诱导后的菌体蛋白;3:超声破碎后的菌体蛋白上清;4:流出液;5:洗涤液;6:10 mmol·L−1 GSH洗脱液;7:20 mmol·L−1 GSH洗脱液;8:30 mmol·L−1 GSH洗脱液;箭头标注的是纯化的重组蛋白。B:纯化蛋白的Western Blot 检测,箭头标注的是JsMYB305重组蛋白与GST单克隆抗体杂交后的条带。
Figure 3. Purification and western blot identification of recombinant protein
Note: M: 15-180 kDa protein ladder; A: purification of recombinant protein; 1: uninduced bacterial protein; 2: bacterial protein induced by 0.2 mmol·L−1 IPTG; 3: supernatant of bacterial protein after ultrasonic crushing; 4: effluent; 5: washing liquid; 6: eluent of 10 mmol·L−1 GSH; 7: eluent of 20 mmol·L−1 GSH; 8: eluent of 30 mmol·L−1 GSH; arrow points at purified recombinant protein; B: detection of purified protein by western blot; arrow points at band after hybridization of JsMYB305 recombinant protein with GST monoclonal antibody.
表 1 构建原核表达载体时扩增JsMYB305编码序列的引物序列
Table 1 Primer sequences for amplifying JsMYB305 coding sequence in prokaryotic expression vector construction
引物名称
Primer name引物序列
Primer sequence(5′-3′ )JsMYB305-F gagagaGGA TCCATGGACAAGAAA ATATGCAAT AGCTCTC JsMYB305-R gagagaGTCGACTTAATCCCCATTAAGTAA CTGGATG 注:上游引物中划线部分为Bam H I酶切位点,下游引物中划线部分为Sal I酶切位点。
Note: The underlined sequence in the forward primer is the Bam H I restriction site, in the reverse primer is the Sal I restriction site. -
[1] 朱建新, 程福建, 杨江帆. 茉莉花茶香气影响因素研究进展 [J]. 中国茶叶, 2021, 43(1):40−43. DOI: 10.3969/j.issn.1000-3150.2021.01.007 ZHU J X, CHENG F J, YANG J F. Research progress on factors influencing aroma of jasmine tea [J]. China Tea, 2021, 43(1): 40−43.(in Chinese) DOI: 10.3969/j.issn.1000-3150.2021.01.007
[2] BERA P, KOTAMREDDY J N R, SAMANTA T, et al. Inter-specific variation in headspace scent volatiles composition of four commercially cultivated jasmine flowers [J]. Natural Product Research, 2015, 29(14): 1328−1335. DOI: 10.1080/14786419.2014.1000319
[3] BERA P, MUKHERJEE C, MITRA A. Enzymatic production and emission of floral scent volatiles in Jasminum sambac [J]. Plant Science, 2017, 256: 25−38. DOI: 10.1016/j.plantsci.2016.11.013
[4] SPITZER-RIMON B, MARHEVKA E, BARKAI O, et al. EOBII, a gene encoding a flower-specific regulator of phenylpropanoid volatiles' biosynthesis in Petunia [J]. The Plant Cell, 2010, 22(6): 1961−1976. DOI: 10.1105/tpc.109.067280
[5] SPITZER-RIMON B, FARHI M, ALBO B, et al. The R2R3-MYB-like regulatory factor EOBI, acting downstream of EOBII, regulates scent production by activating ODO1 and structural scent-related genes in Petunia [J]. The Plant Cell, 2012, 24(12): 5089−5105.
[6] VAN MOERKERCKE A, HARING M A, SCHUURINK R C. The transcription factor emission of benzenoids ii activates the MYB odorant1 promoter at a MYB binding site specific for fragrant petunias [J]. The Plant Journal:for Cell and Molecular Biology, 2011, 67(5): 917−928. DOI: 10.1111/j.1365-313X.2011.04644.x
[7] MEDINA-PUCHE L, MOLINA-HIDALGO F J, BOERSMA M, et al. An R2R3-MYB transcription factor regulates eugenol production in ripe strawberry fruit receptacles [J]. Plant Physiology, 2015, 168(2): 598−614. DOI: 10.1104/pp.114.252908
[8] JIAN W, CAO H H, YUAN S, et al. SlMYB75, an MYB-type transcription factor, promotes anthocyanin accumulation and enhances volatile aroma production in tomato fruits [J]. Horticulture Research, 2019, 6: 22. DOI: 10.1038/s41438-018-0098-y
[9] 孙君, 陈雪津, 陈笛, 等. 茉莉花JsPAL基因及其启动子克隆与表达分析 [J]. 西北植物学报, 2020, 40(6):949−956. SUN J, CHEN X J, CHEN D, et al. Cloning and expression analysis of phenylalanine ammonia-lyase gene from Jasminum sambac and isolation of its promoter [J]. Acta Botanica Boreali-Occidentalia Sinica, 2020, 40(6): 949−956.(in Chinese)
[10] 陈笛, 王鹏杰, 郑玉成, 等. 茉莉花MVD基因及其启动子的克隆与表达 [J]. 福建农林大学学报(自然科学版), 2019, 48(3):309−315. CHEN D, WANG P J, ZHENG Y C, et al. Cloning and expression of MVD gene and its promoter in Jasminum sambac [J]. Journal of Fujian Agriculture and Forestry University (Natural Science Edition), 2019, 48(3): 309−315.(in Chinese)
[11] 陈笛, 陈雪津, 郭永春, 等. 茉莉花芳樟醇生物合成关键基因的克隆与表达分析[J]. 西北植物学报, 2019, 39(8): 1344−1352. CHEN D, CHEN X J, GUO Y C, et al. Cloning and expression analysis of JsNEL/LINS from Jasminum sambac[J]. Acta Botanica Boreali-Occidentalia Sinica, 2019, 39(8): 1344−1352.(in Chinese)
[12] 崔萌, 刘志钦, 叶乃兴, 等. 茉莉花香气相关基因JsGDS启动子的克隆及功能分析 [J]. 分子植物育种, 2021, 19(2):441−447. CUI M, LIU Z Q, YE N X, et al. Cloning and functional analysis of the aroma-related gene JsGDS promoter from Jasminum sambac [J]. Molecular Plant Breeding, 2021, 19(2): 441−447.(in Chinese)
[13] 陈桂信, 俞滢, 刘雨轩, 等. 茉莉香气释放相关基因分离及JsBEBT的克隆与表达分析 [J]. 分子植物育种, 2021, 19(20):6662−6670. CHEN G X, YU Y, LIU Y X, et al. Isolation of related genes cloning and expression analysis of JsBEBT in jasmine aroma [J]. Molecular Plant Breeding, 2021, 19(20): 6662−6670.(in Chinese)
[14] 陈笛, 郑玉成, 林浥, 等. 茉莉花MK基因及启动子克隆与表达分析 [J]. 分子植物育种, 2020, 18(3):772−779. CHEN D, ZHENG Y C, LIN Y, et al. Cloning and expression analysis of mevalonate kinase gene and its promoter from Jasminum sambac [J]. Molecular Plant Breeding, 2020, 18(3): 772−779.(in Chinese)
[15] 崔萌. 茉莉花香气合成相关基因JsGDS启动子的分离与活性分析[D]. 福州: 福建农林大学, 2020. CUI M. Isolation and activity analysis of promoter of JsGDS gene associated with aroma synthesis from Jasminum sambac[D]. Fuzhou: Fujian Agriculture and Forestry University, 2020. (in Chinese)
[16] 孙君, 陈桂信, 叶乃兴, 等. 茉莉花香气相关基因JsDXS及其启动子的克隆与表达分析 [J]. 园艺学报, 2014, 41(6):1236−1244. SUN J, CHEN G X, YE N X, et al. Cloning and expression analysis of deoxyoxylulose-5-phosphate synthase gene related to aroma from Jasminum sambac and isolation of its promoter [J]. Acta Horticulturae Sinica, 2014, 41(6): 1236−1244.(in Chinese)
[17] 张月, 袁媛, 何弦, 等. 茉莉花JsMYB108和JsMYB305基因的克隆及其对TPS基因的激活作用 [J]. 热带作物学报, 2021, 42(6):1539−1548. DOI: 10.3969/j.issn.1000-2561.2021.06.005 ZHANG Y, YUAN Y, HE X, et al. Cloning of JsMYB108 and JsMYB305 and analysis of their activation on TPS gene in Jasminum sambac [J]. Chinese Journal of Tropical Crops, 2021, 42(6): 1539−1548.(in Chinese) DOI: 10.3969/j.issn.1000-2561.2021.06.005
[18] 张磊, 唐永凯, 李红霞, 等. 促进原核表达蛋白可溶性的研究进展 [J]. 中国生物工程杂志, 2021, 41(S1):138−149. ZHANG L, TANG Y K, LI H X, et al. Advances in promoting solubility of prokaryotic expressed proteins [J]. China Biotechnology, 2021, 41(S1): 138−149.(in Chinese)
[19] 邱淑彬, 荆韧威, 郭正隆, 等. 两种不同的原核表达载体蛋白表达及纯化的比较 [J]. 基因组学与应用生物学, 2020, 39(9):4136−4144. QIU S B, JING R W, GUO Z L, et al. Comparison of two different prokaryotic expression vectors in protein expression and purification [J]. Genomics and Applied Biology, 2020, 39(9): 4136−4144.(in Chinese)
[20] 黄传臻, 刘香利, 曹汝菲, 等. 小麦CWI-B1的原核表达、纯化与多克隆抗体制备 [J]. 农业生物技术学报, 2017, 25(7):1102−1110. HUANG C Z, LIU X L, CAO R F, et al. Prokaryotic expression, purification and preparation of polyclonal antibody for wheat (Triticum aestivum) CWI-B1 [J]. Journal of Agricultural Biotechnology, 2017, 25(7): 1102−1110.(in Chinese)
[21] 陈明, 陈文静. 几种微生物表达系统的比较 [J]. 安徽农学通报(上半月刊), 2011, 17(3):68−71. CHEN M, CHEN W J. Comparisons of some microbial expression systems [J]. Anhui Agricultural Science Bulletin, 2011, 17(3): 68−71.(in Chinese)
[22] 胡京蕊, 沈金宝, 李晶岚, 等. 拟南芥耐盐相关基因AtSTK原核表达载体的构建及表达 [J]. 华北农学报, 2013, 28(2):38−41. DOI: 10.3969/j.issn.1000-7091.2013.02.007 HU J R, SHEN J B, LI J L, et al. Prokaryotic expression vector construction and expression of tolerance related gene AtSTK in Arabidopsis [J]. Acta Agriculturae Boreali-Sinica, 2013, 28(2): 38−41.(in Chinese) DOI: 10.3969/j.issn.1000-7091.2013.02.007
[23] 孙伟, 任家鑫, 腾峰, 等. ZmAGO18b的原核表达载体的构建与表达 [J]. 基因组学与应用生物学, 2020, 39(12):5647−5651. SUN W, REN J X, TENG F, et al. Construction and expression of a prokaryotic expression vector of ZmAGO18b [J]. Genomics and Applied Biology, 2020, 39(12): 5647−5651.(in Chinese)
[24] HARPER S, SPEICHER D W. Purification of proteins fused to glutathione S-transferase [J]. Methods in Molecular Biology (Clifton, N J ), 2011, 681: 259−280.
[25] 朱炳森. 玉米转录因子ZmYY1、ZmYY2与RNA结合蛋白ZmRBM25互作调控ZmABR1表达的研究[D]. 泰安: 山东农业大学, 2020. ZHU B S. Maize transcription factors ZmYY1, ZmYY2 interact with RNA-binding protein ZmRBM25 to regulate ZmABR1 expression[D]. Taian: Shandong Agricultural University, 2020. (in Chinese)
[26] 王意程. 油菜素内酯调控红肉苹果类黄酮合成的机理研究[D]. 泰安: 山东农业大学, 2021. WANG Y C. Mechanism of brassinosteroid on regulation flavonoid biosynthesis in red-fleshed apple[D]. Taian: Shandong Agricultural University, 2021. (in Chinese)
[27] 赵杰, 王兵, 骆梅, 等. GST-pull down技术筛选毛白杨天冬氨酸蛋白酶PtoAED3互作蛋白 [J]. 北京林业大学学报, 2021, 43(5):64−74. DOI: 10.12171/j.1000-1522.20200365 ZHAO J, WANG B, LUO M, et al. Identification of aspartic acid protease PtoAED3-interacting proteins through GST pull-down assays in Populus tomentosa [J]. Journal of Beijing Forestry University, 2021, 43(5): 64−74.(in Chinese) DOI: 10.12171/j.1000-1522.20200365
[28] 窦万福, 祁静静, 胡安华, 等. GST pull-down联合LC-MS/MS筛选柑橘抗溃疡病转录因子CsBZIP40的互作蛋白 [J]. 中国农业科学, 2019, 52(13):2243−2255. DOI: 10.3864/j.issn.0578-1752.2019.13.005 DOU W F, QI J J, HU A H, et al. Screening of interacting proteins of anti-canker transcription factor CsBZIP40 in Citrus by GST pull-down combined with LC-MS/MS [J]. Scientia Agricultura Sinica, 2019, 52(13): 2243−2255.(in Chinese) DOI: 10.3864/j.issn.0578-1752.2019.13.005
-
期刊类型引用(9)
1. 孙雨桐,刘德帅,冯美,齐迅,姚文孔. 果树分子标记辅助育种研究进展. 江苏农业学报. 2024(01): 183-192 .  百度学术
百度学术
2. 白玉娥,李今普,师鹏飞,王荣学,高颖,胡志健,杨荣. 基于表型性状的不同梨品种遗传多样性分析. 山东农业科学. 2024(02): 30-38 .  百度学术
百度学术
3. 刘东,孟瑾瑾,王盼,陈红刚,王惠珍,杜弢. 不同生态类型菘蓝SLAF-seq分子标记. 中草药. 2024(07): 2375-2382 .  百度学术
百度学术
4. 代建菊,李茂富,赵俊,慕尧,普天磊,袁建民,金杰. 云南不同栽培区域油梨果实品质差异分析. 西北植物学报. 2023(04): 656-666 .  百度学术
百度学术
5. 张雪芹,欧阳海波,谢志南,林丽霞,赖瑞云,钟赞华,林建忠. 不同品种油梨果实品质、光合特性比较及其相关分析. 南方农业学报. 2023(02): 405-413 .  百度学术
百度学术
6. 陈勇,李汶锺,彭林润,王明怀. 银木种子园及基于SNP标记的遗传分析. 湖南林业科技. 2023(03): 37-43 .  百度学术
百度学术
7. 李永涛,王振猛,杨庆山,周健,王莉莉,刘德玺,魏海霞. 山东省6个豆梨野生群体的遗传多样性分析. 中南林业科技大学学报. 2022(01): 138-145 .  百度学术
百度学术
8. 梁燕,韩传明,孙超,王翠香,闵旭峰,王静,王清海. 基于AFLP标记的薄壳山核桃种质资源遗传多样性分析. 江苏林业科技. 2022(01): 1-7 .  百度学术
百度学术
9. 郑斌,施晓龙,邹明宏. 基于枝条、叶和花的油梨种质表型多样性分析. 广东农业科学. 2020(09): 37-46 .  百度学术
百度学术
其他类型引用(4)




 下载:
下载: