Effects of Temperature and Media on Cocultivation of Pleurotus pulmonarius and Trichoderma harzianum
-
摘要:目的 探究秀珍菇和木霉菌丝适宜生长的条件和特性。方法 应用生长速率测定法和平板共培养法,对比了秀珍菇5个菌株菌丝在不同温度和营养培养基条件下生长及与木霉共培养情况。结果 秀珍菇不同菌株在相同温度,不同培养基条件下,86-1菌株菌丝生长速度与其他4个菌株均有极显著差异。不同温度条件,Y710-14菌株25 ℃与28 ℃菌丝生长速度无显著性差异,它们与其余3个温度有极显著差异。 X98ly-13、XD-13、903-1和86-1在25~30 ℃温度条件下,菌株菌丝生长速度均无显著性差异,但均与32和34 ℃条件有极显著差异。木霉菌丝的生长温度范围与秀珍菇菌丝一样(25~32 ℃),但木霉菌丝生长速度明显快于秀珍菇菌丝,秀珍菇与木霉菌丝共培养时,秀珍菇菌丝对木霉未观察到拮抗现象,秀珍菇菌丝很快就被木霉菌丝完全覆盖。5个秀珍菇菌株在PDYA培养基中的生长势最强,其次为PDSYA培养基,PDSA和PDA培养基中的菌丝生长势正常,86-1菌株菌丝生长速度均最慢。PDA和PDSYA培养基条件,X98ly-13、Y710-14、XD-13与901-1菌株菌丝生长速度无显著差异。PDSA培养基条件,X98ly-13、Y710-14与901-1菌株菌丝生长速度无显著差异。结论 供试的5个秀珍菇菌株,Y710-14最适生长温度为30 ℃,其余4个菌株菌丝的最适生长温度均为25 ℃。秀珍菇菌丝适宜的生长温度范围与木霉菌丝相同,但秀珍菇菌丝的生长速度和耐高温能力明显弱于木霉菌丝。添加酵母粉培养基菌丝更浓密,生长势最强,添加淀粉培养基的菌丝更白。Abstract:Objective Growth and characteristics of 5 strains of Pleurotus pulmonarius and Trichoderma harzianum in cocultivation on different media at different temperatures were studied for the potential application in the mushroom cultivation.Method The growth rate and plate confrontation culture methods were used to observe the mycelial growth or antagonism of 5 strain of P. pulmonarius and T. harzianum in cocultivation on different media at different temperatures.Result Under same culture conditions, the mycelial growth of the mushroom strain 86-1 significantly differed from the rest of the 5 strains. The growth of Y710-14 at 25 ℃and 28 ℃ showed no significant differences but did from other 3 tested temperatures. The mycelial growth rates of X98ly-13, XD-13, 903-1, and 86-1 at 25-30 ℃did not differ significantly but significantly at 32 ℃and 34 ℃. Both T. harzianum and P. pulmonarius grew well at 25-32 ℃. The former grew significantly faster than the latter, and thus, covered all over the latter in time of coculture on medium. However, no apparent antagonism between the two species was evident. Insofar as culture medium is concerned, PDYA provided the strongest mycelial growth followed by PDSYA, while PDSA and PDA being average. Among the various strains, 86-1 grew the slowest on any of the media. On PDA or PDSYA, X98ly-13, Y710-14, XD-13, and 903-1 grew without any significant differences, so did X98ly-13, Y710-14, or 903-1 on PDSA. When starch was present as an ingredient in PDSA, the strains of mushrooms appeared whiter with milky white color, and no significant differences on the mycelia growth rate of X98ly-13, Y710-14, and 901-1.Conclusion The optimum growth temperature for Y710-14 was 30 ℃, and for the other strain 25 ℃. Both P. pulmonarius and T. harzianum grew well in same range of temperature, but the mushroom mycelia grew slower with lower tolerance to high temperature than T. harzianum. The medium containing yeast powder produced thicker mycelia with the strongest vitality, while that consisted of starch, whiter in color than otherwise. It appeared that there was an application potential of the cocultivation of P. pulmonarius and T. harzianum for the mushroom industry.
-
Keywords:
- Pleurotus pulmonarius /
- temperature /
- culture medium /
- Trichoderma harzianum
-
简单序列重复区间扩增多态性(inter-simple sequence repeat,ISSR)是基于简单重复序列扩增多态性(simple sequence repeat, SSR)建立的一种分子标记技术[1]。与SSR技术相比,ISSR无须知道物种基因组信息即可在全基因组范围上分析物种的遗传多样性,与常用的分子标记RAPD、RFLP、AFLP和SSR相比,具有操作简便、检测成本低、稳定性好等优点,目前已广泛应用在食用菌菌株鉴定[2]、遗传分析[3]及杂交育种[4]等方面。
DNA甲基化是广泛存在于生物体中的一种DNA转录后修饰过程,是表观遗传学研究的热点之一,主要研究在DNA序列不改变的情况下通过DNA序列的甲基化修饰进而影响基因表达和生物体的表型变化,如真菌的生长发育[5]、环境胁迫[6]等现象。研究表明,甲基化在物种进化中发挥着重要作用,且基因组中单核苷酸甲基化多态性通常高于DNA序列本身的变异,由于部分甲基化变异导致的表观遗传学变化可以在后代中稳定遗传[7],因此通过甲基化位点多样性分析进而发掘与重要农艺性状相关的基因位点,可为分子辅助育种提供帮助。甲基化敏感扩增多态性(methylation sensitive amplified polymorphism, MSAP)技术因其敏感度高、操作简便,成为动物、植物及微生物全基因组DNA甲基化水平与模式常用的技术手段[5-8]。而荧光标记甲基化敏感扩增多态性F-MSAP (fluorescence-labeled methylation sensitive amplified polymorphism)基于MSAP利用荧光标记选择性扩增引物,通过毛细管电泳检测,具有更高的灵敏性和检测效率。
本研究采用ISSR和F-MSAP两种分子研究方法对20株香菇菌株基因组DNA进行分析,以期为香菇表观遗传学研究及香菇高产优质新品种的选育提供理论依据。
1. 材料与方法
1.1 材料
20株香菇菌株均为福建省农业科学院食用菌研究所收集保藏,其中17株为栽培菌株,3株为采自福建建瓯的野生菌株(L2016-1、L2016-2、L2016-5)。
限制性内切酶、T4 DNA连接酶购自纽英伦生物技术(北京)有限公司。Taq酶和dNTPs购自宝生物工程(大连)有限公司。
1.2 菌丝培养与DNA提取
香菇菌丝的培养参考Möller等[9]的方法,采用改良的CTAB法进行DNA提取[10]。
1.3 引物
8个ISSR引物(P2、P4、P5、P6、P7、P8、P16、P20)[3]和15对F-MSAP引物(选择性扩增引物HM1、HM2、HM3在5′端加上FAM荧光标记)[6]由上海生工生物工程公司合成。
1.4 ISSR和F-MSAP分析
ISSR的PCR扩增体系(25 μL)为:DNA约50 ng,10 × PCR Buffer 2.5 μL,引物0.3 μmol·L-1,dNTPs 1 μmol·L-1,MgCl2 1.5 mmol·L-1,Taq DNA聚合酶1.25 U。PCR反应条件为:94℃ 5 min;94℃ 45 s, 55~62℃ 45 s,72℃ 1.5 min,35个循环;72℃ 10 min,16℃保存。PCR产物经2%琼脂糖凝胶电泳检测。
F-MSAP的酶切、连接、预扩增及选择性扩增按文献[6]的方法操作。
1.5 条带统计
ISSR条带根据琼脂糖凝胶电泳结果某一相同迁移率位置上出现条带的标记为“1”,未出现条带的标记为“0”。利用GeneMarker 2.2软件对毛细管电泳结果的峰值进行扫描及数据收集,再根据无带和有带情况转化为0,1数据矩阵。根据EcoRⅠ/HpaⅡ和EcoRⅠ/MspⅠ双酶切产生的条带差异,参考ZHAO等[11]的方法将甲基化模式分为3种类型:Ⅰ型为非甲基化位点,即EcoRⅠ/HpaⅡ和EcoRⅠ/MspⅠ双酶切组合中均能出现的条带的位点,记作(1,1);Ⅱ型为半甲基化位点,即EcoRⅠ/HpaⅡ组合中有条带,而EcoRⅠ/MspⅠ组合中没有条带的位点,记作(1,0);Ⅲ型为全甲基化位点,即EcoRⅠ/HpaⅡ组合中无条带,而EcoRⅠ/MspⅠ组合中有条带的位点,记作(0,1)。
根据Cervera等[12]的方法,将F-MSAP产生的条带类型分为2个二维矩阵:甲基化非敏感多态性矩阵(methylation insensitive polymorphisms,MISP),将条带类型为(1,1)的标记为“1”,其他类型的均标记为“0”;甲基化敏感多态性矩阵(methylation sensitive polymorphisms,MSP),将条带类型为(1,0)和(0,1)的标记为“1”,其他类型的均标记为“0”。
1.6 数据分析
利用软件NTsys 2.10e对不同的数据矩阵进行UPGMA聚类分析,遗传相似性采用简单匹配系数(simple matching coefficient)法。不同类型相似性矩阵间的相关性采用软件NTsys 2.10e的Mantel检测法(1000次随机排列)。
2. 结果与分析
2.1 20株香菇菌株的ISSR分析
利用8对ISSR引物对20株香菇菌株的基因组DNA多态性分析显示:8对引物共可扩增出98条稳定清晰可辨的条带,其中多态性条带89条,多态性比率为90.82%。各引物扩增的条带数为8~16个,片段大小在250~3 000。样品间的遗传相似系数范围为0.520 4~0.989 7,表明野生香菇菌株与栽培菌株种间亲缘关系较远,栽培菌株间L135与L808间亲缘关系较远,其遗传相似系数为0.581 6。根据ISSR扩增数据构建的20株香菇菌株的UPMGA聚类树状图(图 1)可将其分为3大类。栽培菌株与野生菌株在相似系数约0.61处分属不同分枝。
2.2 20株香菇菌株的F-MSAP分析
2.2.1 DNA甲基化水平
利用15对引物对20个香菇菌株进行甲基化多态性分析,结果见表 1。共扩增产生13 487条DNA片段,平均每个样本每对引物扩增获得约45条片段。在全部检测位点中,半甲基化位点为1 704个,平均半甲基化率12.64%,其中Zhongxiang-68和L2016-5半甲基化率最高为15.32%,Cr66最低为9.21%;全甲基化位点为1 865个,平均全甲基化率13.85%,其中L236全甲基化率最高为36.61%,L939最低为8.26%;L236总甲基化水平最高为48.41%,L26最低为22.13%,平均总甲基化率为26.49%。
表 1 20株香菇DNA甲基化水平分析Table 1. Analysis of methylation polymorphisms on 20 L. edodes strains菌株 带型 半甲基化率/% 全甲基化率/% 总甲基化率/% Ⅰ Ⅱ Ⅲ Cr04 516 101 70 14.70 10.19 24.89 Cr66 538 64 93 9.21 13.38 22.59 L01 502 78 101 11.45 14.83 26.28 L04 484 85 106 12.59 15.70 28.30 L135 490 78 78 12.07 12.07 24.15 L18 510 91 70 13.56 10.43 23.99 L20 537 76 88 10.84 12.55 23.40 L2016-1 449 77 89 12.52 14.47 26.99 L2016-2 478 100 82 15.15 12.42 27.58 L2016-5 503 108 94 15.32 13.33 28.65 L236 341 78 242 11.80 36.61 48.41 L241-4 537 77 84 11.03 12.03 23.07 L258 497 74 91 11.18 13.75 24.92 L26 549 79 77 11.21 10.92 22.13 L808 504 74 88 11.11 13.21 24.32 L9015 500 89 70 13.51 10.62 24.13 L921 479 81 91 12.44 13.98 26.42 L939 503 97 54 14.83 8.26 23.09 Wuxiang-1 498 91 114 12.94 16.22 29.16 Zhongxiang-68 503 106 83 15.32 11.99 27.31 注:总扩增位点= Ⅰ+Ⅱ+Ⅲ;甲基化总位点= Ⅱ+Ⅲ;总甲基化率=(Ⅱ+Ⅲ)/(Ⅰ+Ⅱ+Ⅲ);全甲基化率=Ⅲ/(Ⅰ+Ⅱ+Ⅲ);半甲基化率= Ⅱ/(Ⅰ+Ⅱ+Ⅲ)。 2.2.2 MISP和MSP矩阵聚类分析
进一步将MSAP矩阵拆分为MSP和MISP矩阵。根据MISP矩阵进行聚类分析(图 2),可将野生菌株和栽培菌株分为2大组,而在栽培菌株组中L236单独聚为一枝,其他栽培菌株的聚类分析结果与ISSR类似;根据MSP矩阵进行聚类分析的结果(图 3)与ISSR和MISP矩阵分析的结果差异较大,在相似系数约0.75处,L236、Wuxiang-1和L921首先分别聚为3个不同分枝,其他的栽培菌株和野生菌株则聚为一个大的组,进一步可分为野生菌株组和栽培菌株组。进一步采用Mantel检验(1000次随机排列)分析ISSR与MSP、MISP产生的相似性系数矩阵间的相关性水平,结果表明:ISSR与MSP相似性系数矩阵间的相关系数为0.14,两者间相关性不显著(P=0.143);ISSR与MISP相似性系数矩阵间的相关系数为0.63,且显著相关(P < 0.01)。
3. 讨论与结论
根据ISSR和MSAP的聚类分析结果看出,ISSR分析原先聚为一枝的部分菌株通过MSAP分析进一步从原分枝中区分出来,推测表观遗传多样性相对于序列变异更具有多发性,且可以通过MSAP分析检测出来[13]。本研究发现,MSP与ISSR间的相关系数为0.14,遗传与表观遗传多样性间存在负相关性,甲基化多样性和遗传多样性是分开的,两者间可能通过不同的机制产生或维持[14]。在MSP和MISP分析中,野生香菇菌株和栽培菌株分为明显不同的分支,推测在香菇种间存在物种特异的DNA甲基化多态性,且可以稳定遗传下去,而且还可能被选择促使这物种的遗传和表观遗传分化[14]。
MSAP技术是在AFLP技术基础上建立起来的分子标记技术,是目前常用的表观遗传学研究技术之一,仅需较少的引物组合即可检测出大量的甲基化位点[15]。越来越多的研究表明DNA甲基化可以产生可遗传的变异。目前关于香菇多样性的研究大多采用ISSR、RAPD或SRAP等遗传多样性研究技术[3, 16],但这些标记不能检测由于DNA甲基化或染色质异构等表观遗传学造成的差异。遗传和表观遗传多样性同为生物多样性的重要基础,因此本研究利用ISSR和F-MSAP技术分析了不同香菇菌株基因组甲基化多态性,为香菇种质资源鉴定、分析及遗传育种研究提供参考。
-
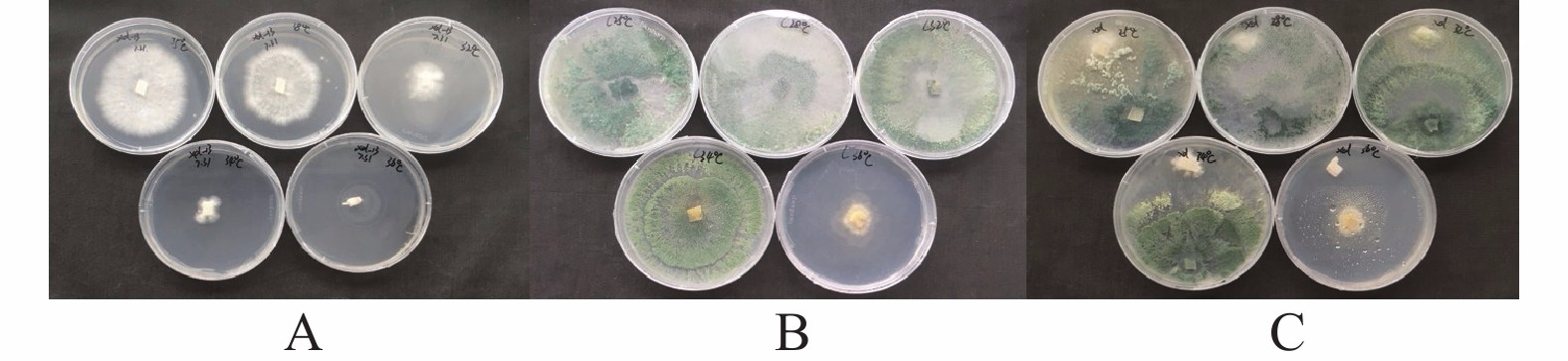
图 1 秀珍菇(XD-13)木霉(T001)菌丝在不同温度条件下生长及共培养情况
注:①A:秀珍菇菌丝;B:木霉菌丝;C:秀珍菇和木霉菌丝共培养;②图中平皿从左到右处理温度依次为25、28、32 ℃(上排),34、36 ℃(下排)。
Figure 1. Mycelial growth of P. pulmonarius (XD-13) and T. harzianum (T001) in cocultivation at different temperatures
Note: ① A: mycelia of P. pulmonarius; B: mycelia of T. harzianum; C: mycelia of P. pulmonarius and T. harzianum. ② Plate temperatures from left to right at 25 ℃, 28 ℃, and 32 ℃ on upper row; 34 ℃ and 36 ℃ on bottom row.
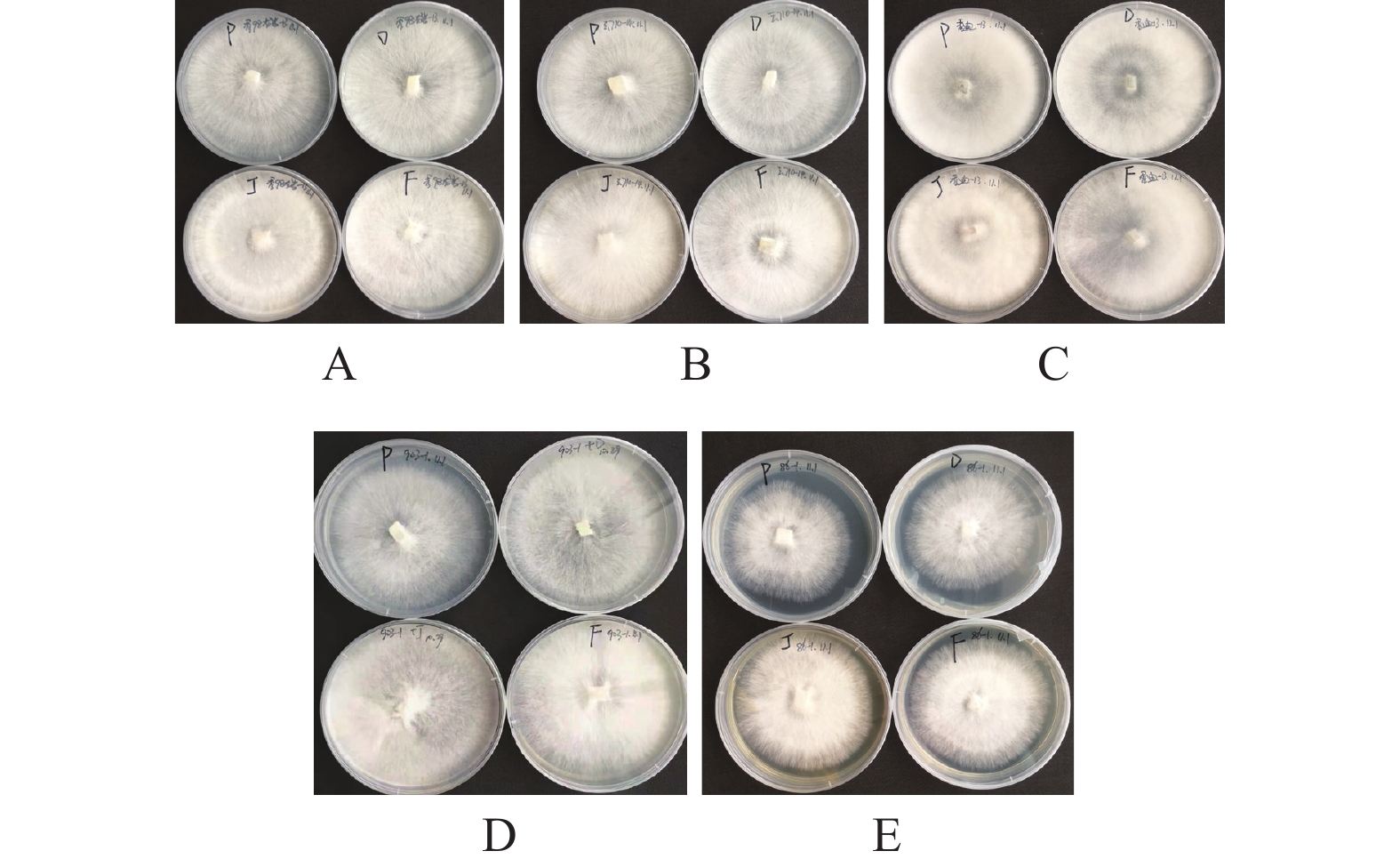
图 2 5个菌株在不同培养基条件下菌丝的生长情况
注:①A:X98ly-13菌株;B:Y710-14菌株;C:XD-13菌株;D:903-1菌株;E:86-1菌株。②平皿从左至右依次为PDA、PDSA、PDYA、PDSYA培养基。
Figure 2. Mycelial growth of 5 strains of P. pulmonarius cultured on different media
Note: ①A:X98ly-13; B: Y710-14; C: XD-13; D: 903-1; E: 86-1. ② Plates from left to right represent culture media PDA, PDSA, PDYA, and PDSYA.
表 1 温度对秀珍菇菌丝生长速度的影响
Table 1 Effects of temperature on mycelial growth of P. pulmonarius
菌株
Strain温度
Temperature/
℃萌发时间
Germination
time/h菌丝生长速度
The growth rate of
mycelia
/(mm·d−1)满皿时间
Full petri
dish time/dX98ly-13 25 24 8.63±0.01 Aa 6 28 24 8.25±0.01 Aab 6 30 24 7.96±0.05 ABbc 6 32 24 7.50±0.01 Bc 6.33 34 72 0.92±0.02 Cd >15 Y710-14 25 24 7.42±0.06 Bc 6.67 28 24 8.00±0.03 Bb 6 30 24 8.83±0.01 Aa 5.33 32 24~48 6.46±0.01 Cd 8.33 34 72 0.83±0.03 De >15 Xd-13 25 24 8.88±0.02 Aa 5 28 24 7.63±0.01 Aa 5 30 24 8.38±0.03 ABb 5.33 32 24~48 7.75±0.03 Bc 6.67 34 72 0.92±0.01 Cd >15 903-1 25 24 7.86±0.08 Aa 6 28 24 7.71±0.01 Aa 6 30 24 7.71±0.02 Aa 6 32 24~48 6.29±0.06 Bb 7.67 34 72 0.67±0.01 Cc >15 86-1 25 24 5.38±0.04 Aa 9 28 24 4.46±0.09 ABa 10 30 24 4.38±0.09 ABa 11.33 32 24~48 3.08±0.05 Bb 20.33 34 72 0.46±0.01 Cc >21 注:表中不同大小写字母表示同一菌株在不同温度条件下菌丝生长速度有极显著差异(P<0.01)和显著差异(P<0.05)。
Note: Data with different uppercase and lowercase letters on same column indicate significant differences at P<0.01 and P<0.05, respectively.表 2 木霉在不同温度条件下菌丝生长情况
Table 2 Mycelial growth of T. harzianum at different temperatures
温度
Temperature/
℃萌发时间
Germination
time/h菌丝生长速度
Growth rate of mycelia/
(mm·d−1)满皿
时间
Full petri
dish time/d覆盖秀珍菇
菌丝时间
Infect mycelia of
Pleurotus
pulmonarius
time/h25 <24 19.33±0.03 Bb 2.21 48 28 <24 20.5±0.05 Aa 2.21 48 30 <24 19.33±0.03 Bb 2.5 48 32 24 18.5±0.05 Bc 3 48~54 34 24~48 14.67±0.03 Cd 3 54~72 36 72 3.17±0.03 De / / 注:表中不同大小写字母表示菌株在不同温度条件下菌丝生长速度有极显著差异(P<0.01)和显著差异(P<0.05)。
Note: Data with different uppercase and lowercase letters on same column indicate significant differences at P<0.01 and P<0.05, respectively.表 3 秀珍菇不同菌株在4种培养基中的菌丝生长情况分析
Table 3 Mycelial growth of 5 strains of P. pulmonarius on 4 different culture media
培养基
Culture
medium菌株
Strain菌丝生长速度
The growth rate
of mycelia/
(mm·d−1)菌丝特征
Mycelia characteristicsPDA X98ly-13 8.42±0.38 Aa 生长速度快、粗壮浓密、洁白 Y710-14 8.05±1.04 Aa 生长速度较快、浓密、洁白 XD-13 8.67±0.90 Aa 生长速度快、气生菌丝多、洁白 903-1 7.72±0.36 Aa 生长速度中等、较密、洁白 86-1 6.06±0.88 Bb 生长速度慢、粗壮浓密、洁白 PDSA X98ly-13 7.78±1.20 Bb 生长速度快、粗壮浓密、乳白 Y710-14 8.44±0.46 ABab 生长速度快、浓密、乳白 XD-13 9.28±0.51 Aa 生长速度快、气生菌丝多、乳白 903-1 7.56±0.58 Bb 生长速度中等、较密、乳白 86-1 6.00±0.56 Cc 生长速度慢、粗壮浓密、乳白 PDYA X98ly-13 8.58±0.66 Aab 生长速度快、粗壮浓密、洁白 Y710-14 8.78±0.75 Aa 生长速度快、浓密、洁白 XD-13 8.89±0.82 Aa 生长速度快、气生菌丝多、洁白 903-1 7.83±0.35 Ab 生长速度正常、较密、洁白 86-1 6.22±0.62 Bc 生长速度慢、粗壮浓密、洁白 PDSYA X98ly-13 8.22±0.71 Aa 生长速度快、粗壮浓密、洁白 Y710-14 8.11±0.49 Aa 生长速度快、浓密、洁白 XD-13 8.75±0.69 Aa 生长速度快、气生菌丝多、洁白 903-1 8.05±0.81 Aa 生长速度正常、较密、洁白 86-1 6.72±0.36 Bb 生长速度慢、粗壮浓密、洁白 注:表中不同大、小写字母表示不同菌株在相同培养基条件下菌丝生长速度有极显著差异(P<0.01)和显著差异(P<0.05)。
Note: Means within a column followed by different uppercase and lowercase letters indicate significant difference at P<0.01 or P<0.05, respectively. -
[1] 闫静, 王伟科, 袁卫东, 等. 温度对秀珍菇生长发育及胞外酶活性的影响 [J]. 浙江大学学报(农业与生命科学版), 2020, 46(2):161−167. YAN J, WANG W K, YUAN W D, et al. Effects of temperature on the growth, development and extracellular enzyme activities of Pleurotus pulmonarius [J]. Journal of Zhejiang University (Agriculture & Life Sciences), 2020, 46(2): 161−167.(in Chinese)
[2] 张金霞, 黄晨阳, 郑素月. 平菇新品种——秀珍菇的特征特性 [J]. 中国食用菌, 2005, 24(4):26,25. ZHANG J X, HUANG C Y, ZHENG S Y. Characteristics of a new variety of Pleurotus ostreatus - Pleurotus pulmonarius [J]. Edibie fungi of China, 2005, 24(4): 26,25.(in Chinese)
[3] LECHNER B E, WRIGHT J E, ALBERTÓ E. The genus Pleurotus in Argentina [J]. Mycologia, 2004, 96(4): 845−858. DOI: 10.2307/3762117
[4] OLIVEIRA S S, DA C S M G, EDMAR C. Chemical composition of Pleurotus pulmonarius (Fr. ) Quél. substrates and residue after cultivation [J]. Braz Arch Biol Techn, 2002, 45(4): 531−535. DOI: 10.1590/S1516-89132002000600018
[5] VELÁZQUEZ-CEDEÑO M A, MATA G, SAVOIE J M. Waste-reducing cultivation of pleurotus ostreatus, and pleurotus pulmonarius, on cofee pulp: changes in the production of some lignocellulolytic enzymes [J]. World J Microb Biot, 2002, 18(3): 201−207. DOI: 10.1023/A:1014999616381
[6] STANLEY H O, UMOLO E A, STANLEY C N. Cultivation of oyster mushroom (Pleurotus pulmonarius) on amended corncob substrate [J]. Agric Biol JN Am, 2011, 2(10): 1336−1339. DOI: 10.5251/abjna.2011.2.10.1336.1339
[7] NGUYEN T K, IM K H, CHOI J, et al. Evaluation of antioxidant, anti-cholinesterase, and anti-inflammatory effects of culinary mushroom Pleurotus pulmonarius [J]. Mycobiology, 2016, 44(4): 291−301. DOI: 10.5941/MYCO.2016.44.4.291
[8] WAHAB N A, ABDULLAH N, AMINUDIN N. Characterisation of potential antidiabetic-related proteins from Pleurotus pulmonarius (Fr.) Quél. (grey oyster mushroom) by MALDI-TOF/TOF mass spectrometry [J]. BioMed Research International, 2014, 2014: 131607.
[9] XU W, HUANG J J, CHEUNG P C. Extract of Pleurotus pulmonarius suppresses liver cancer development and progression through inhibition of VEGF-induced PI3K/AKT signaling pathway [J]. PLoS One, 2012, 7(3): e34406. DOI: 10.1371/journal.pone.0034406
[10] OLUFEMI A E, TERRY A O A, KOLA O J. Anti-leuCultivation of diferent strains of king oyster mushroom (Pleurotus eryngii) on saw dus and rice straw in Bangladeshkemic and immunomodulatory efects of fungal metabolites of Pleurotus pulmonarius and Pleurotus ostreatus on benzene-induced leukemia in Wister rats [J]. Korean J Hematol, 2012, 47(1): 67−73. DOI: 10.5045/kjh.2012.47.1.67
[11] 王增术. 秀珍菇烂袋原因及其预防措施 [J]. 食用菌, 2004, 26(5):43−44. WANG Z S. Reasons and preventive measures for rotten bag of Pleurotus geesteranus [J]. Edible Fungi, 2004, 26(5): 43−44.(in Chinese)
[12] 陈天泰, 马福义. 食用菌绿霉病综合防治技术 [J]. 食用菌, 2004, 26(5):44−45. CHEN T T, MA F Y. Integrated control technology of edible fungus Trichoderma disease [J]. Edible fungi, 2004, 26(5): 44−45.(in Chinese)
[13] 柯斌榕, 卢政辉, 吴小平, 等. 秀珍菇退化菌株生物学特征比较及dsRNA病毒检测 [J]. 南方农业学报, 2018, 49(1):98−103. KE B R, LU Z H, WU X P, et al. Biological characteristics of degenerated strains of Pleurotus pulmonarius and detection of dsRNA virus [J]. Journal of Southern Agriculture, 2018, 49(1): 98−103.(in Chinese)
[14] 卢政辉. 秀珍菇安全高效生产技术要点 [J]. 浙江食用菌, 2009(4):46−48. LU Z H. Safe and efficient production technology of Pleurotus pulmonarius [J]. Edible Fungi of Zhejiang, 2009(4): 46−48.(in Chinese)
[15] 邓文明, 王怡暄, 王爱仙, 等. 五个秀珍菇菌株在水帘设施大棚中栽培的生长表现 [J]. 食药用菌, 2020(5):335−337. DENG W M, WANG Y X, WANG A X, et al. The growth performance of five strains of Pleurotus cultivated in a greenhousewith evaporative cooling pad facilities [J]. Edible and Medicinal Mushrooms, 2020(5): 335−337.(in Chinese)
[16] 黄良水, 蔡为明, 金群力. 我国秀珍菇的发展现状与前景展望 [J]. 食药用菌, 2015(6):340−343. HUANG L S, CAI W M, JIN Q L. The present situation and prospect of the development of the Pleurotus pulmonarius in China [J]. Edible and Medicinal Mushrooms, 2015(6): 340−343.(in Chinese)
[17] 中国食用菌协会. 2019年度全国食用菌统计调查结果分析[J]. 中国食用菌, 2021(6): 104−110. Chinese Edible Fungi Association. Analysis on the results of the national statistical survey of edible fungi in 2019[J]. Edible Fungi of China, 2021(6): 104−110.(in Chinese)
[18] 卢政辉, 廖剑华, 陈美元, 等. 秀珍菇高产优质栽培技术 [J]. 菌物学报, 2007(26):404−407. LU Z H, LIAO J H, CHEN M Y. High yield and high quality cultivation technology of Pleurotus pulmonarius [J]. Journal of fungus, 2007(26): 404−407.(in Chinese)
[19] 杨爱玲. 罗源县秀珍菇规模化高产栽培技术 [J]. 食用菌, 2019, 41(5):51−54,57. YANG A L. Large-scale and high-yield cultivation techniques of Pleurotus pulmonarius in Luoyuan county [J]. Edible Fungi, 2019, 41(5): 51−54,57.(in Chinese)
[20] 王再明, 石堃, 潘玲玲, 等. 温度对8种食用菌菌丝生长的影响 [J]. 林业科技, 2015, 40(3):20−23. WANG Z M, SHI K, PAN L L, et al. The influence of temperature on mycelial growth of eight kinds of food [J]. Forestry Science & Technology, 2015, 40(3): 20−23.(in Chinese)
[21] 翁伯琦, 江枝和, 林勇. 不同培养料对秀珍菇子实体蛋白质营养评价的影响 [J]. 食用菌学报, 2002, 9(2):10−13. WENG B Q, JIANG Z H, LIN Y. Effect of different kinds of composts on the nutritional evaluation of the protein in Pleurotus geesteranus fruitbodies [J]. Acta Edulis Fungi, 2002, 9(2): 10−13.(in Chinese)
[22] 冯志勇, 王志强, 郭力刚, 等. 秀珍菇生物学特性研究 [J]. 食用菌学报, 2003, 10(3):11−16. FENG Z Y, WANG Z Q, GUO L G, et al. Studies on the biological characteristics of Pleurotus geesteranus [J]. Acta Edulis Fungi, 2003, 10(3): 11−16.(in Chinese)
[23] 余松, 李文博, 李冬莲等. 江西省秀珍菇产业发展现状及政策建议 [J]. 农业经济, 2021(4):130−134. YU S, LI W B, LI D L, et al. Development status and policy suggestions of Pleurotus pulmonarius industry in Jiangxi province [J]. Agricultural economy, 2021(4): 130−134.(in Chinese)
[24] 雷潇, 陈定安, 吴胜莲, 等. 秀珍菇高温品种筛选及栽培配方优化 [J]. 贵州农业科学, 2019, 47(9):49−52. LEI X, CHEN D A, WU S L, et al. Screening and optimum cultivation formula of Pleurotus geesteranus strains with tolerance to high temperature [J]. Guizhou Agricultural Sciences, 2019, 47(9): 49−52.(in Chinese)
[25] 吴小平, 吴晓金, 谢宝贵, 等. 食用菌抗木霉菌株的初步筛选[C]//中国菌物学会第四届会员代表大会暨全国第七届菌物学学术讨论会. 2008: 375−382.





 下载:
下载: