Duplex TaqMan qPCR for Detecting Porcine Epidemic Diarrhea and Transmissible Gastroenteritis Viruses and Epidemic Study in Fujian
-
摘要:目的 实现猪流行性腹泻病毒(PEDV)和猪传染性胃肠炎病毒(TGEV)的快速鉴别诊断,并调查分析福建省2019–2021年PEDV和TGEV流行情况。方法 根据PEDV的N 基因和TGEV的S 基因序列分别设计特异性引物和标记FAM、VIC荧光报告基团的探针,建立、优化双重荧光定量PCR反应条件和体系,并检测其敏感性、特异性和重复性。应用该方法对福建省2019–2021年收集的297份疑似腹泻病料进行病原检测。结果 建立的方法对PEDV和TGEV的最低检测限均为10拷贝·μL−1,比普通PCR检测灵敏度提高100倍;对其他常见猪病原不发生非特异性反应;批内、批间变异系数均小于1%。福建省297份临床样本检测结果显示,单PEDV感染率为88.89%,单TGEV感染率为1.01%,PEDV和TGEV混合感染率为3.37%。结论 本研究建立的方法具有敏感性高、特异性强、稳定性好等特点。福建省内2019–2021年以PEDV感染为主,TGEV感染率低,存在PEDV、TGEV混合感染的情况。Abstract:Objective A
TaqMan probe-based duplex real-time PCR for rapid detection of porcine epidemic diarrhea virus (PEDV) and transmissible gastroenteritis virus (TGEV) was developed. A study was conducted using the methodology to analyze the related 2019–2021 epidemic occurred in Fujian. Method Specific primers and probes labeled with FAM and VIC were designed to amplify the N gene of PEDV and the S gene of TGEV, respectively. A reaction system for the assay was established, optimized, and tested for sensitivity, specificity, and repeatability. The assay was used for the viral detection on 297 suspected clinic specimens collected from 2019 to 2021 for an epidemiology study.Result The newly developed duplex qPCR methodology showed a sensitivity of 10 copies·μL−1 on PEDV and TGEV, which was 100 times higher than that of regular PCR. There were no cross reactions with other common viruses. The inter- and intra-assays had variations on Ct values below 1%. On the 297 specimens, the infection rate of PEDV was 88.89%, that of TGEV 1.01%, and that of both PEDV and TGEV 3.37%.Conclusion The established duplex qPCR had high sensitivity, specificity, repeatability, and reproducibility for detecting PEDV and TGEV. The 2019–2021 epidemic involving the viruses appeared to be mostly PEDV with low incidents of mixed TGEV and PEDV/TGEV infection. -
作为食用菌生产的首道工序,菌种生产对食用菌产业的健康发展至关重要[1]。目前,在食用菌制种工艺中,主要采用固体菌种逐级扩繁的方式来生产食用菌母种、原种和栽培种, 双孢蘑菇[2]、香菇[3]、金针菇[4]及杏鲍菇[5]等食用菌的菌种生产都是采用这种制种工艺。近年来,食用菌工厂化生产迅速发展,采用液体菌种进行工厂化生产金针菇、杏鲍菇等食用菌也得到应用[6-7]。2013年,福建省农业科学院食用菌研究所制种研究室对双孢蘑菇菌株W192进行了液体发酵培养的研究[8],优化配方培养的双孢蘑菇W192液体菌种作为原种扩繁生产栽培种取得良好效果,并具有培养时间短、发菌快、菌龄整齐一致、接种方便等优点。廖剑华等[9]选育的双孢蘑菇W192经2次发酵的粪草料栽培,表现出耐肥、耐水和适应性广的特点,但在常规季节性栽培中,培养料投料量不足,含氮量低,扭结密度大时容易出现小菇薄菇,影响鲜销。为了进一步改良品种特性,课题组采用单孢分离方法,从W192后代中优选出双孢蘑菇菌株W38。该菌株经2011-2013年产季的中型生产试验,高产优质性状表现稳定,已进行生产性栽培示范。前期的研究表明,培养基及其培养条件影响双孢蘑菇液体菌种菌丝体生物量和菌种活力[8]。目前,关于双孢蘑菇菌株W38液体菌种培养的报道还未见。本文对双孢蘑菇W38进行摇瓶培养,并采用Plackett-Burmen设计和响应面分析法对其液体培养基及培养条件进行优化,以获得最优液体菌种生物量的培养配方及培养条件,旨在为利用双孢蘑菇液体菌种扩繁栽培种提供参考。
1. 材料与方法
1.1 试验材料
供试菌株:双孢蘑菇菌株W38,摇瓶种子培养基和摇瓶基础培养基配方见参考文献[8]。麦粒培养基配方:小麦98%,石膏粉2%,含水量 (45±1)%,pH 7.5~8.0等。
1.2 试验方法
1.2.1 菌种活化
双孢蘑菇W38菌种活化方法见参考文献[8]。
1.2.2 摇瓶种子培养
将活化的0.5 cm×0.5 cm大小的双孢蘑菇W38试管母种菌块,转接到250 mL三角瓶中100 mL灭菌摇瓶种子培养基上,每瓶三角瓶接4块菌块,静置培养2 d后,在培养温度24℃、摇瓶转数180 r·min-1的培养振荡器上旋转振荡培养10 d,得到双孢蘑菇W38摇瓶种子。
1.2.3 摇瓶发酵培养
在无菌操作条件下,将双孢蘑菇W38摇瓶种子用组织捣碎机匀浆。250 mL三角瓶装入试验摇瓶基础培养基100 mL,灭菌后接入5% (V/V) 摇瓶种子,置于振荡器上旋转振荡培养。培养条件:培养温度24℃、摇瓶转数180 r·min-1、培养时间7 d。
1.2.4 菌丝体生物量测定
菌丝体生物量参照参考文献[8]进行测定。
1.2.5 液体菌种活力检测
将500 g麦粒培养基装入15 cm×30 cm折角聚丙烯菌种袋中,经126℃、2.5 h高温高压灭菌,冷却后在超净工作台接入10 mL优化配方培养的双孢蘑菇W38液体菌种,以基础培养基培养的液体菌种作为对照。接种后,置于培养室25℃培养,观察菌种的萌发、走菌情况,当菌丝生长至袋口端边缘4~5 cm时,画一起始线,当生长最快的菌丝即将长满菌种袋时再画一终止线,记录培养时间,测量菌丝生长长度,计算菌丝生长速度。
1.3 响应面方法的试验设计与数据分析
1.3.1 Plackett-Burman试验设计和结果分析方法
根据前期单因素试验结果和双孢蘑菇W192液体发酵培养的文献报道[8],按照Plackett-Burman试验设计,以双孢蘑菇W38菌丝体生物量为指标,选取发酵培养基组分和培养条件的8个因素作为考察对象,利用Design-Expert 8.0统计软件对试验结果进行各个因素的显著性分析。
1.3.2 Box-Behnken试验设计和结果分析方法
通过Design-Expert 8.0软件对Plackett-Burman试验结果进行分析,得到3个对双孢蘑菇W38菌丝体生物量影响极其显著的因素,然后进行3因素3水平的17组Box-Behnken中心组合设计试验,中心点编码为0,试验的实际浓度选取Plackett-Burman试验中高低水平浓度的中间值,经计算,小米粉为40 g·L-1、黄豆粉为12.5 g·L-1、MgSO4·7H2O为1.0 g·L-1,其余因素浓度取初始配方值。
2. 结果与分析
2.1 Plackett-Burman试验
按照Plackett-Burman筛选试验设计,考察小米粉 (X1)、黄豆粉 (X2)、K2HPO4(X3)、MgSO4·7H2O (X4)、发酵培养温度 (X5)、培养基初始pH (X6)、发酵培养时间 (X7)、摇瓶转数 (X8)8个因素对双孢蘑菇W38菌丝体生物量的影响。试验设计及其结果如表 1,各因素均取高 (1)、低 (-1) 2个水平,按照设计表格的试验号依次进行试验,所得Y值为双孢蘑菇W38菌丝体生物量。
表 1 筛选试验设计及结果Table 1. Plackett-Burman design and results试验号 X1 X2 X3 X4 X5 X6 X7 X8 Y 1 -1 1 -1 1 1 -1 1 1 1.42 2 1 -1 1 1 1 -1 -1 -1 1.81 3 -1 -1 1 -1 1 1 -1 1 1.35 4 -1 1 1 -1 1 1 1 -1 1.31 5 1 -1 -1 -1 1 -1 1 1 1.58 6 -1 -1 -1 -1 -1 -1 -1 -1 1.43 7 -1 1 1 1 -1 -1 -1 1 1.54 8 -1 -1 -1 1 -1 1 1 -1 1.52 9 1 1 -1 1 1 1 -1 -1 1.65 10 1 -1 1 1 -1 1 1 1 1.74 11 1 1 1 -1 -1 -1 1 -1 1.58 12 1 1 -1 -1 -1 1 -1 1 1.52 注:X1~X8为培养因素;Y值为W38菌丝体生物量 (100 mL含有的克重)。下表同。 利用Design-Expert 8.0统计软件对以上结果进行回归分析,结果如表 2所示,对双孢蘑菇W38菌丝体生物量的影响达到极显著水平 (P<0.01) 的因素有小米粉 (X1)、黄豆粉 (X2) 和MgSO4·7H2O (X4),其他5个因素对菌丝体生物量影响不显著 (P>0.05)。由此,选择小米粉、黄豆粉和MgSO4·7H2O这3个重要影响因素进行Box-Behnken中心组合设计试验。
表 2 Plackett-Burman试验回归分析Table 2. Regression analysis of Plackett-Burman编码 因素 水平 效应t 显著性Pt>︱t︱ 低 (-1) 高 (1) X1 小米粉/ % 3.5 4.5 0.1091 0.0003 X2 黄豆粉/ % 1.00 1.25 -0.0341 0.0099 X3 K2HPO4/ % 0.20 0.25 0.0175 0.2900 X4 MgSO4·7H2O/% 0.100 0.125 0.0758 0.0010 X5 t/℃ 25 30 -0.0175 0.0577 X6 初始pH 6.5 7.5 -0.0225 0.0518 X7 t培养/ d 7 9 -0.0125 0.1215 X8 v/ r·min-1 180 220 -0.0125 0.1215 2.2 响应面优化试验
2.2.1 中心组合设计和响应面分析结果
表 3为Box-Behnken中心组合设计的因素及水平,试验结果见表 4。采用Design-Expert 8.0软件对试验结果进行处理,得到二次响应面回归方程:Y=2.04+0.30X1+0.11X2-0.0031X4-0.053X1X2+0.025X1X4+0.050X2X4-0.039X12-0.084X22-0.081X42,参数见表 5,方程中的X1、X2、X1X2、X22、X42对双孢蘑菇W38菌丝体生物量影响极显著 (P<0.01)。在培养基配方的各成分中,小米粉和黄豆粉对菌丝体生物量的影响最大。对所得数据进行回归分析,结果如表 6所示,回归方程P<0.000 1,表明回归模型极显著;回归方程具有较高的决定系数 (R2= 0.993 3) 和不显著的失拟系数 (P=0.239 8),表明模型拟合程度理想, 可以用于双孢蘑菇W38液体菌种菌丝体生物量的理论预测。
表 3 中心组合设计的因素与水平Table 3. Factors and levers on central composite design编码 因素 水平 -1 0 1 X1 小米粉/(g·L-1) 30 40 50 X2 黄豆粉/(g·L-1) 10.0 12.5 15.0 X4 MgSO4·7H2O/(g·L-1) 0.75 1.00 1.25 表 4 响应面试验设计与结果Table 4. Experimental design and result of response surface methodology试验号 因素 Y X1 X2 X4 1 1 1 1 2.28 2 1 0 1 2.23 3 0 0 0 2.01 4 -1 0 -1 1.66 5 0 0 0 2.03 6 0 -1 -1 1.81 7 0 0 0 2.07 8 0 1 1 2.04 9 0 -1 -1 2.03 10 0 0 0 1.96 11 1 0 -1 2.18 12 0 0 0 2.06 13 -1 0 1 1.61 14 -1 1 0 1.75 15 -1 -1 0 1.45 16 1 -1 0 2.19 17 0 -1 1 1.69 表 5 回归方程各项回归系数显著性检验Table 5. Test of significance for regression coefficient参数 参数估计 标准误差 T检验 Pt>︱t︱ X1 0.30 0.013 0.30125 <0.0001 X2 0.11 0.011 0.11125 <0.0001 X4 -0.005 0.011 -0.005 0.6498 X1X2 -0.053 0.011 -0.0525 0.0097 X1X4 0.025 0.015 0.025 0.1375 X2X4 0.050 0.015 0.050 0.0122 X12 -0.039 0.015 -0.03875 0.0322 X22 -0.084 0.015 -0.08375 0.0007 X42 -0.081 0.015 -0.08125 0.0008 表 6 回归模型方差分析Table 6. Analysis of variance of regression equation方差来源 平方和 自由度 均方 F值 P(Pr>F) 模型 0.92 9 0.10 12.22 <0.0001 残差 6.225×10-3 7 8.893×10-4 失拟 3.825×10-3 3 1.275×10-3 2.13 0.2398 纯误差 2.400×10-3 4 6.000×10-4 总值 0.93 16 决定系数R2 0.9933 变异系数CV 1.53% 图 1~3是根据响应面回归分析和回归方程拟合绘出的响应面三维分析图和等高线图形,图 1~3分别将MgSO4·7H2O、小米粉和黄豆粉中的1个因子分别固定在中心点水平,可以直观分析出其他2因素及其交互作用对双孢蘑菇W38液体菌种菌丝体生物量影响效应的大小。图 1和图 2的等高线图呈椭圆形,说明X1(小米粉) 和X2(黄豆粉) 及X4(MgSO4·7H2O) 和X2(黄豆粉) 之间的交互作用显著;而图 3的等高线图呈圆形,说明X1(小米粉) 和X4(MgSO4·7H2O) 之间的交互作用不显著。
2.2.2 液体培养基最优组合
运用Design-Expert 8.0软件计算出最大响应值所对应的X1、X2、X4分别为0.99、0.44、0.27,自变量实际取值X1为49.90 g·L-1,X2为13.60 g·L-1,X4为1.067 5 g·L-1,此时最大响应值为每100 mL菌丝体2.31 g。因此,双孢蘑菇W38液体菌种最优培养基和培养条件为:小米粉49.90 g·L-1,黄豆粉13.60 g·L-1,KH2PO4 2.00 g·L-1,MgSO4·7H2O 1.067 5 g·L-1,初始pH 6.5,发酵时间7 d,发酵温度24℃,摇瓶转速180 r·min-1。
2.2.3 响应面模型的验证
在优化后的培养基和培养条件下进行3次平行验证实验,双孢蘑菇W38液体菌种的平均每100 mL菌丝体干重为2.35 g,与预测值接近,即拟合度良好。比初始培养基 (基础培养基) 液体发酵培养的双孢蘑菇W38菌丝体每100 mL干重为0.58 g,提高了3.05倍。
2.2.4 液体菌种活力检验
向麦粒培养基中接入10mL优化配方培养的双孢蘑菇W38液体菌种,以基础培养基培养的液体菌种为对照,重复3次,每次10袋,共30袋,进行菌种活力测定,测量菌丝生长长度,计算平均菌丝生长速度。由表 7可知,优化配方的液体菌种菌丝萌发时间为36 h,比基础配方的液体菌种萌发时间48 h缩短12 h,而且在麦粒培养基中生长的菌丝密度浓密,颜色浓白;经计算,优化配方的液体菌种在麦粒培养基的平均菌丝生长速度3.27 mm·d-1,较初始配方的液体菌种平均菌丝生长速度2.85 mm·d-1快14.7%,差异极显著 (P<0.01)。
表 7 双孢蘑菇W38液体菌种的活力对比Table 7. Comparative test on the activity of liquid spawn of Agaricus bisporus Strain W38菌种来源 萌发时间/h 平均菌丝生长速度/(mm·d-1) 初始液体菌种 48 2.85±0.05A 优化液体菌种 36 3.27±0.02B 注:同列数据后不同大写字母表示差异达极显著 (P < 0.01) 水平。 3. 讨论与结论
本研究利用Design-Expert软件,采用Plackett-Burman设计和中心组合设计, 建立了二次响应面回归模型,优化了双孢蘑菇W38液体菌种培养基和培养条件。在Plackett-Burman设计中筛选出影响菌丝体生物量的主效因素为小米粉、黄豆粉和MgSO4·7H2O,这与双孢蘑菇W192液体发酵培养基的优化[8]所筛选主因素为玉米淀粉、黄豆粉和摇瓶转数不同。双孢蘑菇菌株W38与菌株W192虽具有较近的亲缘关系,但它们的液体发酵培养所筛选的主因素不同可能是双孢蘑菇菌株的差异性所致。通过液体菌种活力检测,优化配方培养的双孢蘑菇W38液体菌种比基础配方培养的菌种平均菌丝生长速度快14.7%,差异达极显著 (P<0.01) 水平,说明以菌丝生物量为指标,响应面法优化配方可以提高双孢蘑菇W38液体菌种活力。
本研究在实验室条件下,通过摇瓶发酵培养,获得双孢蘑菇W38液体菌种,再作为原种转接麦粒培养基中培养,液体菌种萌发和菌丝生长情况良好,这证实了双孢蘑菇液体菌种作为原种转接固体培养基的可行性。液体菌种的培养基和培养条件的优化只是液体菌种制种工艺初步阶段,还有待完善液体菌种接种量、接种方式以及发酵罐深层发酵培养的技术参数等。通过响应面分析法确定双孢蘑菇W38最佳的培养基和培养条件为:小米粉49.90 g·L-1,黄豆粉13.60 g·L-1,KH2PO4 2.00 g·L-1,MgSO4·7H2O 1.07 g·L-1,初始pH 6.5,发酵时间7 d,发酵温度24℃,摇瓶转速180 r·min-1。在此条件下,双孢蘑菇W38液体菌种的每100 mL菌丝体生物量可达2.35 g,与初始培养条件下的菌丝体生物量相比提高了3.05倍。本研究得到的液体培养基优化配方可以为双孢蘑菇W38在发酵罐中深层发酵培养提供参考。
-
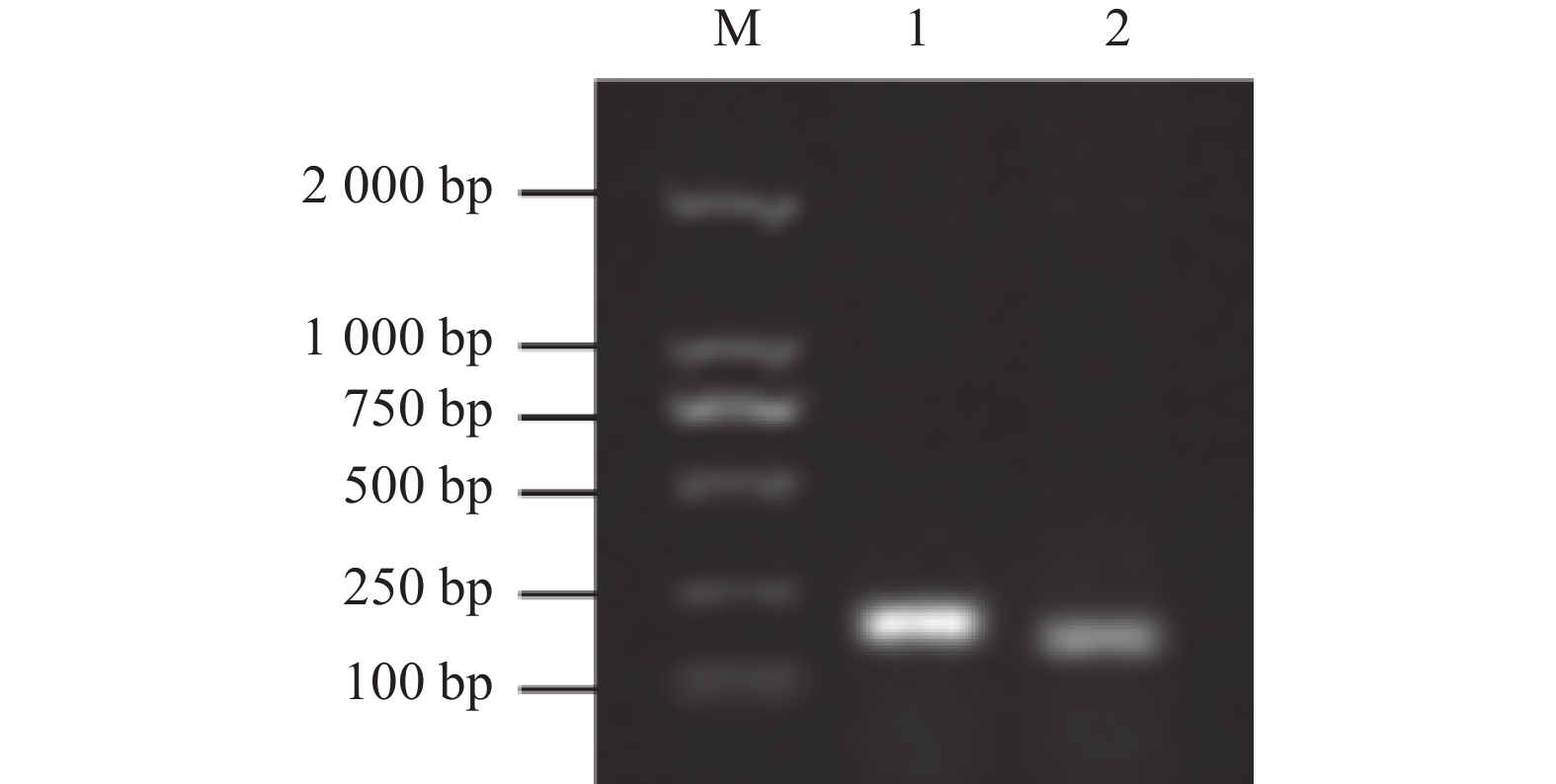
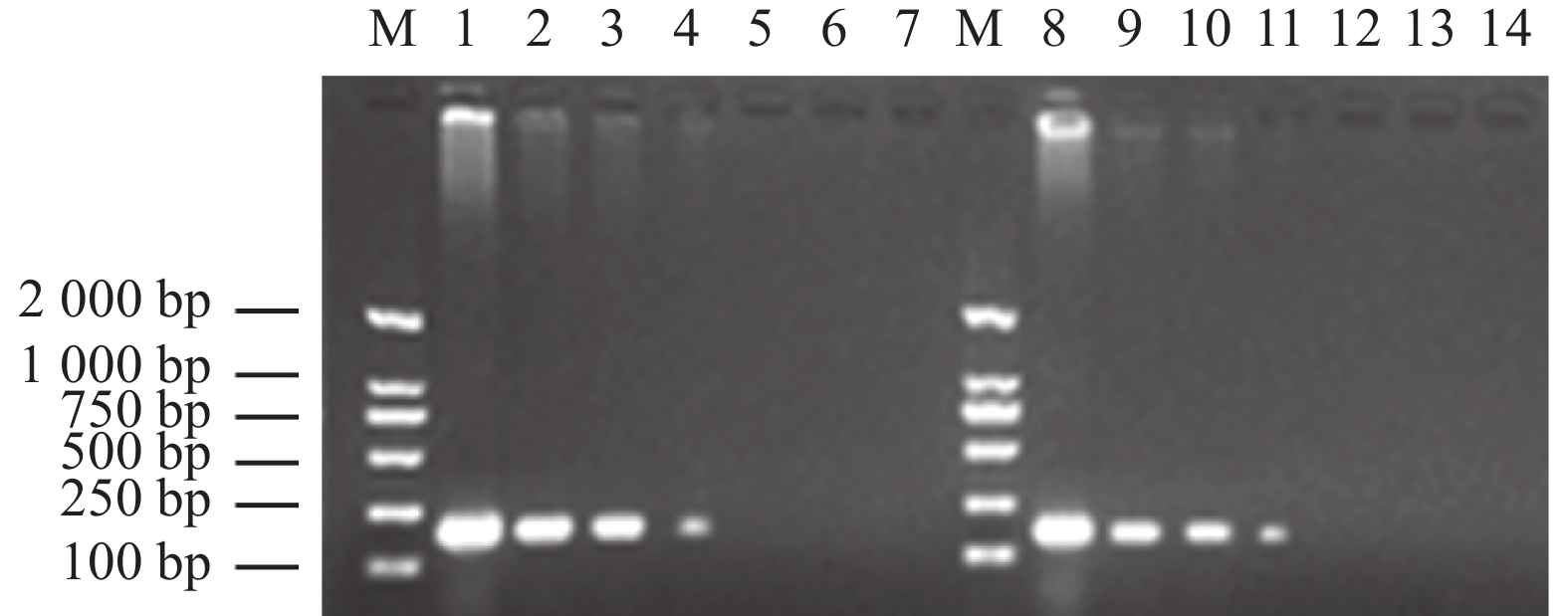
图 5 PEDV和TGEV普通PCR体系敏感性检测
M:Marker DL2000;1–6分别为PEDV质粒浓度1×106 ~ 1×101拷贝·μL−1;8–13分别为TGEV质粒浓度1×106 ~ 1×101拷贝·μL−1,7和14为阴性对照。
Figure 5. Sensitivity of regular PCR for PEDV and TGEV
M: Marker DL2000; PEDV (1-6) and TGEV (8-13) with numbers of copies of 1×106, 1×105, 1×104, 1×103, 1×102, and 1×101; 7 and 14: negative.
表 1 PEDV、TGEV双重荧光定量PCR引物及探针序列
Table 1 Primers and probes of PEDV and TGEV for qPCR
病毒
Virus引物名称
Primer序列(5'- 3')
Sequence (5'- 3')片段大小
Amplified fragment/bp猪流行性腹泻病毒
PEDVPEDV-F CTCCCGAGTGTAGTTGAGATTG 175 PEDV-R CTCCACGACCCTGGTTATTT PEDV-P FAM–CAACCCAACACACCTCCTACTTCACG-BHQ1 传染性胃肠炎病毒
TGEVTGEV-F TGAGGGTGCTGGCTTTGAT 149 TGEV-R CAAGAGTGACACCACCCGTT TGEV-P VIC-CACTGTGGCACCCTTAC
CTGATTGT-BHQ1表 2 疑似腹泻病料收集的来源信息
Table 2 Information on collection of suspected diseased tissues
地区
Region样本数(份)/来源猪场(个)
Samples/ Farms2019年 2020年 2021年 福州 Fuzhou 7/2 25/6 28/19 宁德 Ningde 5/3 15/6 24/13 泉州 Quanzhou 3/2 12/4 21/18 漳州 Zhangzhou 4/3 13/5 18/17 南平 Nanping 7/5 15/7 26/19 三明 Sanming 6/4 11/8 17/12 龙岩 Longyan 3/2 14/12 23/11 合计 Total 35/21 105/48 157/109 表 3 PEDV和TGEV双重荧光定量PCR重复性试验
Table 3 Repeatability and stability of duplex qPCR on PEDV and TGEV detections
质粒 Plasmid 浓度Concentration/
(拷贝·μL−1)组内变异试验 Intra-assay variability 组间变异系数 Inter-assay variability 平均数¯X±SD 变异系数
CV/%平均数¯X±SD 变异系数
CV/%T-PEDV 1.0×102 31.57±0.22 0.69 31.50±0.30 0.93 1.0×103 28.46±0.13 0.45 28.35±0.2 0.71 1.0×104 25.44±0.11 0.45 25.31±0.19 0.75 T-TGEV 1.0×102 32.06±0.28 0.87 31.83±0.33 0.96 1.0×103 28.87±0.11 0.38 28.36±0.19 0.69 1.0×104 25.82±0.16 0.62 25.39±0.23 0.91 表 4 临床样品检测结果
Table 4 Test results on clinical specimens
检测结果 Test results 猪流行性腹泻病毒PEDV 猪传染性胃肠炎病毒TGEV 猪流行性腹泻病毒+猪传染性胃肠炎病毒PEDV+TGEV 样本阳性率 Rate of positive samples/% 88.89 (264/297) 1.01 (3/297) 3.37 (10/297) 病毒拷贝数 Virus copies 1.8×102~6.5×107 3.3×103~7.5×106 1.5×102~7.5×105 阳性猪场比例 Rate of positive farms/% 61.24 (109/178) 1.12 (2/178) 2.81 (5/178) -
[1] ZHANG B, TANG C, YUE H, et al. Viral metagenomics analysis demonstrates the diversity of viral flora in piglet diarrhoeic faeces in China [J]. The Journal of General Virology, 2014, 95(Pt7): 1603−1611.
[2] SUN R Q, CAI R J, CHEN Y Q, et al. Outbreak of porcine epidemic diarrhea in suckling piglets, China [J]. Emerging Infectious Diseases, 2012, 18(1): 161−163. DOI: 10.3201/eid1801.111259
[3] WHITWORTH K M, ROWLAND R R R, PETROVAN V, et al. Resistance to coronavirus infection in amino peptidase N-deficient pigs [J]. Transgenic Research, 2019, 28(1): 21−32. DOI: 10.1007/s11248-018-0100-3
[4] LI W T, LI H, LIU Y B, et al. New variants of porcine epidemic diarrhea virus, China, 2011 [J]. Emerging Infectious Diseases, 2012, 18(8): 1350−1353. DOI: 10.3201/eid1803.120002
[5] YUAN X M, LIN H X, LI B, et al. Efficacy and immunogenicity of recombinant swinepox virus expressing the truncated S protein of a novel isolate of porcine epidemic diarrhea virus [J]. Archives of Virology, 2017, 162(12): 3779−3789. DOI: 10.1007/s00705-017-3548-1
[6] STEVENSON G W, HOANG H, SCHWARTZ K J, et al. Emergence of Porcine epidemic diarrhea virus in the United States: Clinical signs, lesions, and viral genomic sequences [J]. Journal of Veterinary Diagnostic Investigation: Official Publication of the American Association of Veterinary Laboratory Diagnosticians, Inc, 2013, 25(5): 649−654. DOI: 10.1177/1040638713501675
[7] DIEL D G, LAWSON S, OKDA F et al. Porcine epidemic diarrhea virus: An overview of current virological and serological diagnostic methods [J]. Virus Research, 2016, 226: 60−70. DOI: 10.1016/j.virusres.2016.05.013
[8] HIGGINS J A, EZZELL J, HINNEBUSCH B J, et al. 5' nuclease PCR assay to detect Yersinia pestis [J]. Journal of Clinical Microbiology, 1998, 36(8): 2284−2288. DOI: 10.1128/JCM.36.8.2284-2288.1998
[9] WANG J C, WANG J F, CHEN P, et al. Development of a TaqMan-based real-time PCR assay for rapid and specific detection of fowl aviadenovirus serotype 4 [J]. Avian Pathology, 2017, 46(3): 338−343. DOI: 10.1080/03079457.2016.1278428
[10] 李波, 蒋慧娴, 杨瑾, 等. 荧光定量PCR检测技术在动物检疫中的应用进展 [J]. 食品安全导刊, 2021(26):152,154. LI B, JIANG H X, YANG J, et al. Application progress of quantitative PCR detection technology in animal quarantine [J]. China Food Safety Magazine, 2021(26): 152,154.(in Chinese)
[11] 高鑫, 朱武洋, 卢学新. 实时荧光定量PCR在病毒检测中的应用 [J]. 中国人兽共患病学报, 2018, 34(7):660−667. DOI: 10.3969/j.issn.1002-2694.2018.00.105 GAO X, ZHU W Y, LU X X. Real-time polymerase chain reaction in detection of viral pathogen [J]. Chinese Journal of Zoonoses, 2018, 34(7): 660−667.(in Chinese) DOI: 10.3969/j.issn.1002-2694.2018.00.105
[12] 曾宪煜, 陈秋勇, 王隆柏, 等. 2012–2018年福建省猪病毒性腹泻流行情况 [J]. 福建畜牧兽医, 2020, 42(3):11−14. DOI: 10.3969/j.issn.1003-4331.2020.03.005 ZENG X Y, CHEN Q Y, WANG L B, et al. The epidemiological analysis of porcine viral diarrhea in Fujian Province in 2012–2018 [J]. Fujian Journal of Animal Husbandry and Veterinary Medicine, 2020, 42(3): 11−14.(in Chinese) DOI: 10.3969/j.issn.1003-4331.2020.03.005
[13] ZHU Y, LIANG L, LUO Y K, et al. A sensitive duplex nanoparticle-assisted PCR assay for identifying porcine epidemic diarrhea virus and porcine transmissible gastroenteritis virus from clinical specimens [J]. Virus Genes, 2017, 53(1): 71−76. DOI: 10.1007/s11262-016-1405-z
[14] MENG F D, REN Y D, SUO S, et al. Evaluation on the efficacy and immunogenicity of recombinant DNA plasmids expressing spike genes from porcine transmissible gastroenteritis virus and porcine epidemic diarrhea virus [J]. PLoS One, 2013, 8(3): e57468. DOI: 10.1371/journal.pone.0057468
[15] GONZÁLEZ J M, GOMEZ-PUERTAS P, CAVANAGH D, et al. A comparative sequence analysis to revise the current taxonomy of the family Coronaviridae [J]. Archives of Virology, 2003, 148(11): 2207−2235. DOI: 10.1007/s00705-003-0162-1
[16] JUNG K, WANG Q H, SCHEUER K A, et al. Pathology of US porcine epidemic diarrhea virus strain PC21A in gnotobiotic pigs [J]. Emerging Infectious Diseases, 2014, 20(4): 662−665.
[17] KIM S Y, SONG D S, PARK B K. Differential detection of transmissible gastroenteritis virus and porcine epidemic diarrhea virus by duplex RT-PCR [J]. Journal of Veterinary Diagnostic Investigation: Official Publication of the American Association of Veterinary Laboratory Diagnosticians, Inc, 2001, 13(6): 516−520. DOI: 10.1177/104063870101300611
[18] KLEIBOEKER S B, SCHOMMER S K, LEE S M, et al. Simultaneous detection of North American and European porcine reproductive and respiratory syndrome virus using real-time quantitative reverse transcriptase-PCR [J]. Journal of Veterinary Diagnostic Investigation: Official Publication of the American Association of Veterinary Laboratory Diagnosticians, Inc, 2005, 17(2): 165−170. DOI: 10.1177/104063870501700211
[19] 胡鸿惠, 南文金, 黄健强, 等. 猪流行性腹泻病毒和猪传染性胃肠炎病毒一步法双重RT-PCR检测方法的建立与应用 [J]. 中国畜牧兽医, 2016, 43(9):2279−2284. HU H H, NAN W J, HUANG J Q, et al. Establishment and application of a double RT-PCR method for detection of PEDV and TGEV [J]. China Animal Husbandry & Veterinary Medicine, 2016, 43(9): 2279−2284.(in Chinese)
[20] KONG F Z, XU Y R, RAN W, et al. Cold exposure-induced up-regulation of Hsp70 positively regulates PEDV mRNA synthesis and protein expression In vitro [J]. Pathogens (Basel, Switzerland), 2020, 9(4): 246.
[21] ALONSO C, GOEDE D P, MORRISON R B, et al. Evidence of infectivity of airborne porcine epidemic diarrhea virus and detection of airborne viral RNA at long distances from infected herds [J]. Veterinary Research, 2014, 45(1): 73. DOI: 10.1186/s13567-014-0073-z
-
期刊类型引用(7)
1. 陈珣,肇莹,龚娜,刘国丽,马晓颖,张敏,肖军. 基于响应面法优化滑菇液体菌种发酵培养基配方. 南方农业学报. 2024(12): 3625-3635 .  百度学术
百度学术
2. 王焱,王竟夷,黄亮,班立桐,李奕葶,党红慧,王玉. 双孢蘑菇液体菌种固态化工艺的初步研究. 食品与发酵科技. 2021(01): 24-28+74 .  百度学术
百度学术
3. 尹川,杜冰冰,连洁,张弘扬,黄亮,班立桐,王玉. 气升式反应器中通气量和pH对双孢蘑菇液体菌种的影响. 食品与发酵科技. 2021(02): 35-39 .  百度学术
百度学术
4. 曾志恒,曾辉,蔡志欣,郭仲杰,卢园萍,陈美元,廖剑华,戴建清. 双孢蘑菇新型颗粒原种配方的优化. 生物技术通报. 2021(11): 134-141 .  百度学术
百度学术
5. 陈晨伟,丁榕,彭柳城,谢晶,杨福馨,杨新宇,于千惠. 外源营养物对菌丝体生物质材料的生长研究及其性能表征. 农业工程学报. 2021(21): 295-302 .  百度学术
百度学术
6. 曾志恒,曾辉,程翊,杨雷,施肖堃,戴建清. 双孢蘑菇发酵液还原糖和总糖的含量测定. 中国食用菌. 2018(06): 40-43+49 .  百度学术
百度学术
7. 林金盛,蒋宁,李辉平,侯立娟,曲绍轩,张晓华,马林. 工厂化袋栽杏鲍菇液体菌种制作与应用. 山西科技. 2017(06): 143-145 .  百度学术
百度学术
其他类型引用(2)




 下载:
下载: