Effects of Silicon on Growth and Functional Ingredients Accumulation of Anoectochilus roxburghii
-
摘要:目的 探究硅对金线莲营养生长及其主要活性成分累积的影响,为金线莲提质促产提供理论依据。方法 以福建红霞金线莲为材料,采用水培的方式,施加不同浓度硅离子(0、0.175、0.350、0.525、0.700、0.875 mmol·L−1)处理30 d,测定金线莲生长和相关生理生化指标。结果 硅对金线莲生长有促进作用,0.175~0.700 mmol·L−1处理后相对生长率均达对照的7倍以上;随着硅浓度的增加,叶绿素含量、叶绿素指数和氮平衡指数值均呈现明显的先升后降趋势,0.525 mmol·L−1处理时均达到最高值(P<0.01);类黄酮指数则呈先降后升的趋势,在0.875 mmol·L−1处理时达最高值(P<0.01);0.175 mmol·L−1和0.700 mmol·L−1的硅显著提高过氧化物酶的活性,为对照的2~3倍(P<0.01);0.700 mmol·L−1的硅可显著促进金线莲总黄酮和多糖的累积(P<0.01),含量较对照分别高71.45%和116.65%。结论 硅对金线莲的生长有益,0.525 mmol·L−1为营养生长期最佳浓度;提高浓度到0.700 mmol·L−1有益于主要活性成分总黄酮和多糖的累积。Abstract:Objective Effects of silicon on the growth and functional ingredients accumulation of Anoectochilus roxburghii were studied for the herbal crop quality improvement.Method Plants of Hong Xia, A. roxburghii (Wall.) Lindl, were supplied with concentrations of silicon at 0, 0.175, 0.350, 0.525, 0.700, and 0.875 mmol·L−1 in a hydroponic experiment for 30 d. Effects of the treatments on the plant physiology and functional ingredients contents were monitored.Result Silicon addition promoted the growth of A. roxburghii. The relative growth rate under the supplementations of 0.175 to 0.700 mmol·L−1 silicon was more than 7 times that of control. The chlorophyll content, chlorophyll index, and nitrogen balance index (NBI) all rose with increasing silicon to peak at 0.525 mmol·L−1 and followed by a decline (P<0.01), while the flavonoid decreased significantly to its lowest under 0.875 mmol·L−1 (P<0.01) and the peroxidase activity significantly increased more than 2 to 3 times that of control (P<0.01). At high concentration of silicon (i.e., 0.700 mmol·L−1), the accumulation of total flavonoids was 71.45%, and polysaccharides 116.65%, higher than those of control (P<0.01).Conclusion Presence of silicon was beneficial for the growth of A. roxburghii. At an addition rate of 0.525 mmol·L−1 during the vegetative growth period and 0.700 mmol·L−1 in later stage, a maximized accumulation on flavonoids and polysaccharides could be realized.
-
0. 引言
【研究意义】硅(Silicon,Si)在土壤中的含量高达26.4%[1],但主要以不可溶晶态硅存在,植物并不能吸收,只有少量可溶性单硅酸被植物吸收利用,含量在0.1~0.6 mmol·L−1[2]。硅是大多数植物生长发育的准必需元素,对农作物生长有益 [3]。硅能延缓功能叶早衰[4],提高光合色素含量和光合能力[5],促进干物质累积,提高作物产量和品质[6-8]。硅还能改变碳、氮和磷代谢相关基因[9]及激活防卫相关基因的表达,诱导感病作物产生抗毒物质如酚醛类和黄酮类等[10],以及抑制镉[11]和镍[12]等重金属的吸收累积,提高作物对病虫害和逆境的抵抗能力[13-15]。金线莲 Anoectochilus roxburghii(Wall.)Lindl.为兰科多年生草本珍稀草药,素有“药王”的美称,其主要活性药效成分是黄酮类和多糖类[16],具有清除自由基、抗氧化、消炎、增强免疫力等多种药效[17]。因人为过度采挖,加之生长缓慢,金线莲野生资源已十分匮乏,被列为国家二级保护珍稀植物,现已采用组培扩繁、人工大棚或林地仿野生栽植等方式生产金线莲。因生长慢、产量少,金线莲的市场售价高,然而人工生产的栽培期短和品种差异导致有效活性成分差异大、含量低等问题困扰和阻碍了金线莲产业的发展。因此,如何通过改变栽培措施提高金线莲产量和活性成分含量,一直是金线莲研究的热点[18, 19]。【前人研究进展】现有研究发现,硅对盐胁迫下甘草非药用部位茎和叶中总黄酮的积累有明显的促进作用,这种促进效应因硅浓度、胁迫时间和不同部位而异[20]。于涛等研究发现,水稻增施硅钙肥能显著提高各生育时期叶片总酚和类黄酮含量,能明显降低穗颈瘟的病穗率和病情指数[21]。何永美等发现,用UV-B辐射水稻两个品种后,其叶中硅的含量与总酚和类黄酮含量均呈极显著正相关[22],硅素有助于提高叶中酚类化合物合成关键酶PAL的活性和调控叶中的酚类化合物代谢[23]。杨开兴[24]利用沼液施肥可显著增加金线莲的叶绿素、总黄酮和多糖含量。栽培期长短以及不同栽培基质均会影响金线莲多糖和总氨基酸的累积[25],林下仿生种植的总黄酮含量显著高于大棚种植。【本研究切入点】施用硅是否也能提高金线莲的产量和品质,相关研究目前还未见报道。【拟解决的关键问题】本研究以福建红霞金线莲为材料,利用水培的方式,通过在培养液中施加不同浓度的硅,研究其对与营养生长、代谢生理有关的各项生理生化指标的影响,测定其药效成分总黄酮和多糖含量的变化,为名贵中药材金线莲的提质促产提供理论依据和高效栽培措施。
1. 材料与方法
1.1 材料试剂及主要仪器
福建红霞金线莲为福建闽鑫种业有限公司组培的商品瓶苗,硅素供体试剂为国药集团生产的Na2SiO3·9H2O,霍格兰营养液(青岛海博生物),芦丁对照标准品购于中国食品药品检定研究院(批号:100080−201811),葡萄糖等其他药品均为分析纯(国药集团)。
AUW220D十万分之一电子天平(日本岛津),Dualex4植物氮平衡指数测量仪(法国FORCE-A),Lambda35紫外可见分光光度计(PerkinElmer公司),HH-2(双列)电子数显恒温水浴锅(国华电器有限公司),KQ-2200超声波清洗器(上海锦玟仪器设备有限公司)。
1.2 试验方法
1.2.1 硅对金线莲生长的影响
瓶苗开盖驯化3 d,洗净根部用育苗海绵包裹苗根塞入定植篮中,植于增氧水培种植箱中,用10倍稀释霍格兰营养液作为基本培养液(pH 5.8)预培养2 d。每隔1 h用气泵为处理液定时充气15 min,培养温度(23±2) ℃,光照周期为14 h·d−1,光照强度为54 μmol·m−2·s−1。
1.2.2 硅处理
用Na2SiO3·9H2O和基本培养液配制含不同硅浓度的处理液(pH 5.8),选取生长一致的金线莲进行水培处理。试验共设6个浓度处理(0、0.175、0.350、0.525、0.700、0.875 mmol·L−1),每个处理30株,重复3次。处理液每2 d更换一次,培养条件同上。处理30 d后,测定与营养生长、代谢生理有关的相对生长率(R,Relative growth rate)、叶绿素含量、氮平衡指数(Nitrogen balance index,NBI)和过氧化物酶(Peroxidase,POD)活性,以及与其药效相关的总黄酮和多糖含量等各项生理生化指标。
1.2.3 相对生长率的测定
金线莲生长缓慢,为避免单株测量产生的系统误差,采用测定处理前后总鲜重(30株)变化的方法,计算出相对生长率(R),以此作为对比各处理对金线莲生长影响的指标。称量前用吸水纸吸干金线莲样品表面水分,用分析天平测定每处理(30株)的总鲜重。R计算公式如下:R=(m2−m1)/ m1×100%(m1为处理前总鲜重,m2为处理后总鲜重)。
1.2.4 氮素营养参数测定
每个处理每次随机选6株样株,重复3次,测定其+1叶(顶端第一片完全展开叶为+1叶,叶序依次向下递增)叶脉两侧中部两点氮平衡参数,参数包括叶绿素指数(Chl)、类黄酮指数(Flav)、花青素指数(Anth)和氮平衡指数(NBI)。
1.2.5 叶绿素含量测定
每个处理每次随机选6株样株,重复3次,取+1叶,剪碎后称得混合样0.20 g,采用95%乙醇提取叶绿素[26] ,利用分光光度计测定665 nm、649 nm波长下的吸光度A665和A649,根据下列公式分别计算叶绿素a(Chl a)、叶绿素b(Chl b)和总叶绿素(Chl)的含量。
w(Chl a) = 13.95A665 — 6.88A649
w(Chl b) = 24.96wA649 — 7.32A665
w(Chl) = w(Chl a) + w(Chl b) = 6.63A665 + 18.08A649
1.2.6 过氧化物酶(POD)活性测定
每个处理每次随机选6株样株,重复3次,剪取并归集+1、+2、+3叶,各位叶每次取其鲜叶混合样0.1 g,利用愈创木酚-比色法[27] 测定各位叶的POD活性。
1.2.7 总黄酮和多糖提取测定
每个处理每次随机选6株样株,重复3次,全草105 ℃杀青30 min后,80 ℃干燥至恒重,粉碎后过60目筛备用,总黄酮和多糖含量采用张志信等[28]优化后的方法进行测定。
1.2.8 数据处理与分析
数据用Excel 2013整理和制表绘图,用SPSS 22.0 对数据进行统计分析,采用单因素方差分析和Duncan法进行多重比较分析(α=0.05和α=0.01),数据为平均值±标准偏差。
2. 结果与分析
2.1 硅对金线莲生长的影响
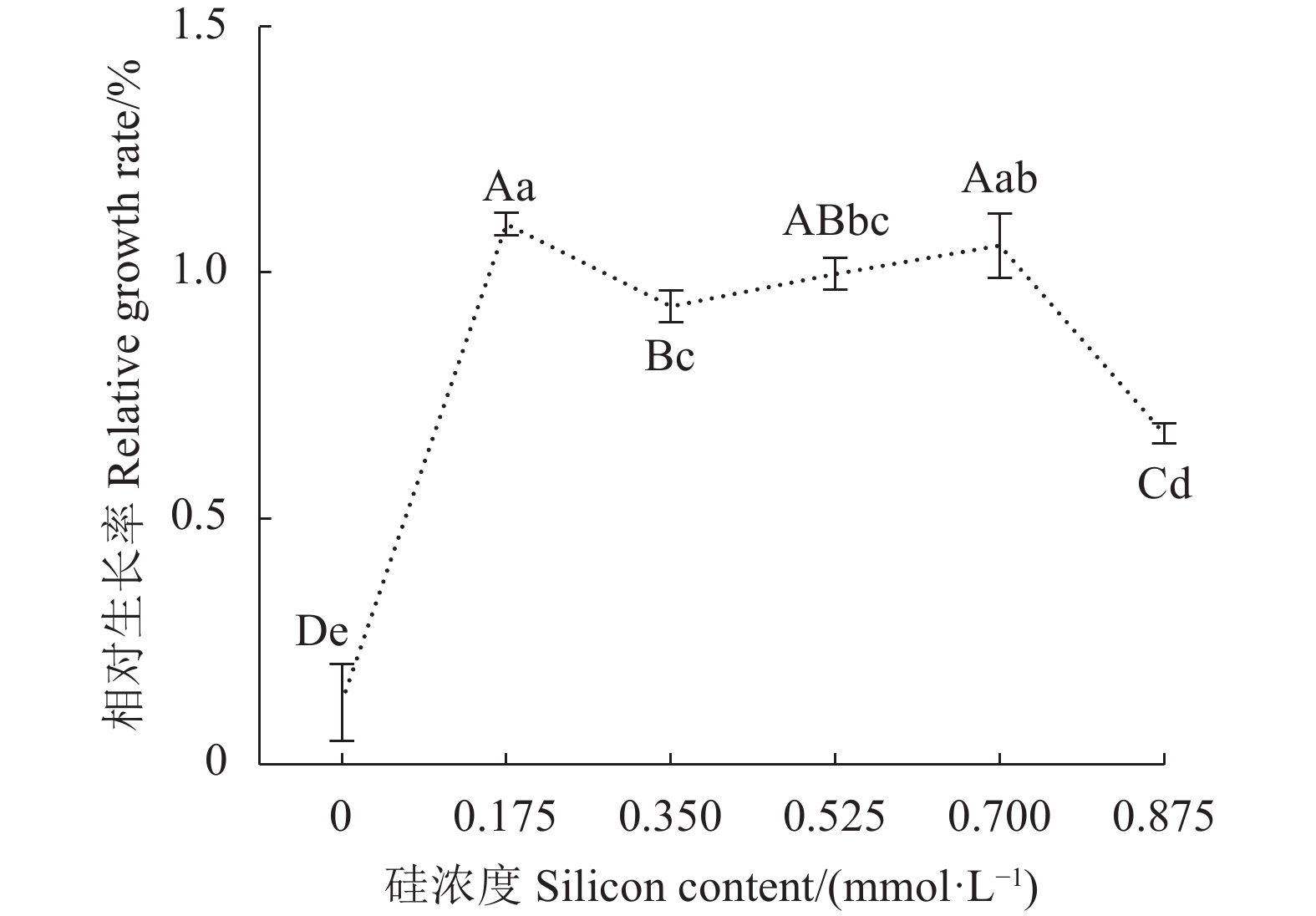
由图1可见,各处理相对生长率均比对照高,相对生长率(R)总体呈先升后降的趋势,各处理均显著高于对照(P<0.01)。0.175和0.700 mmol·L−1的硅处理效果最佳,R值显著高于对照和其他处理(P<0.05),对金线莲的生长促进作用更强;而高浓度0.875 mmol·L−1的硅对金线莲的促生作用最弱,但依然显著好于对照(P<0.01)。
![]() 图 1 不同浓度硅处理对金线莲相对生长率的影响图中不同大、小写字母分别表示处理间的差异达显著水平P<0.01或P<0.05,下图同。Figure 1. Effect of silicon at varied concentrations on relative growth rate of A. roxburghiiData with different capital and lowercase letters mean significant difference at P<0.01 and P<0.05, respectively. Same for following figures.
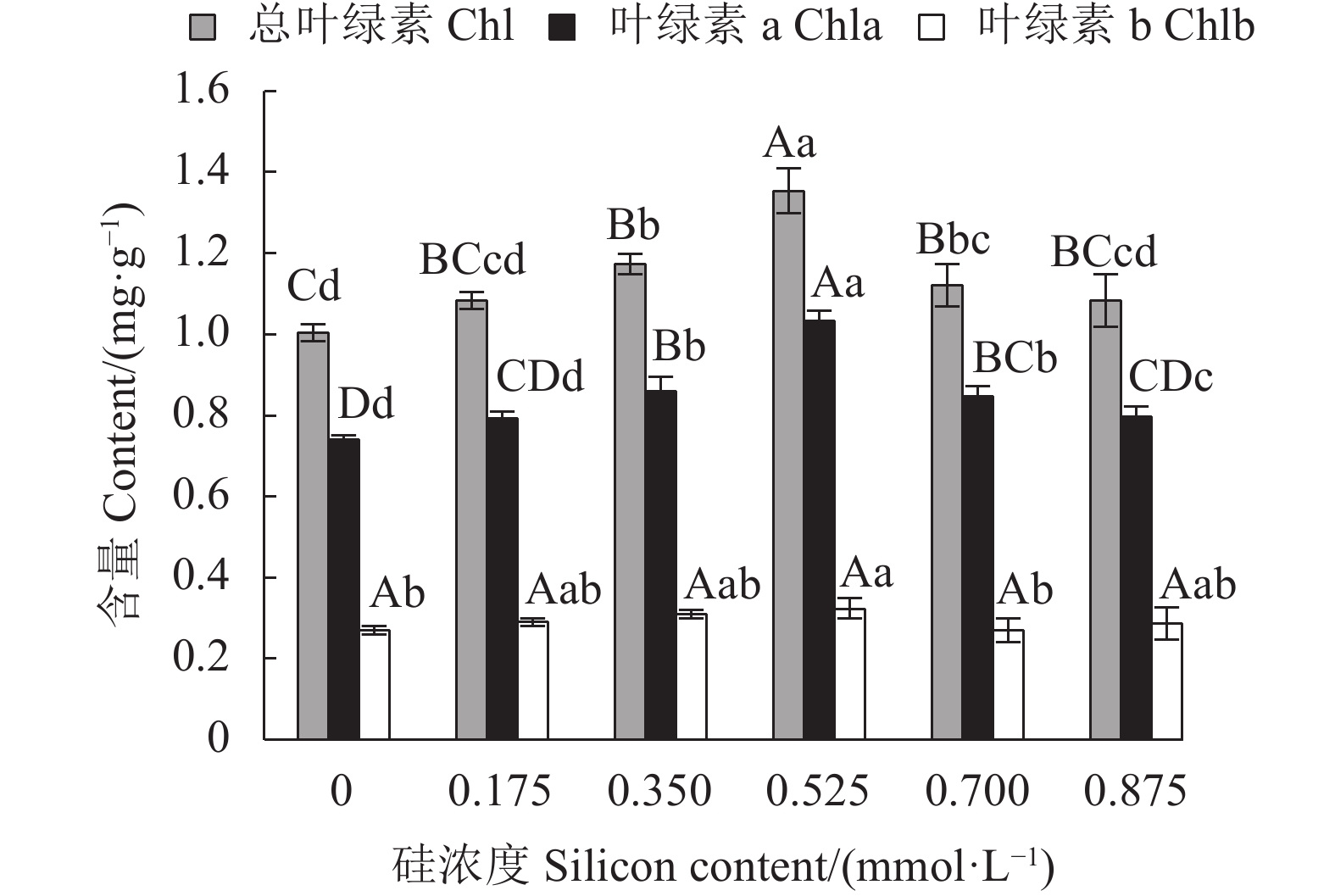
图 1 不同浓度硅处理对金线莲相对生长率的影响图中不同大、小写字母分别表示处理间的差异达显著水平P<0.01或P<0.05,下图同。Figure 1. Effect of silicon at varied concentrations on relative growth rate of A. roxburghiiData with different capital and lowercase letters mean significant difference at P<0.01 and P<0.05, respectively. Same for following figures.2.2 硅对金线莲叶片叶绿素含量的影响
从图2可以看出,处理对叶绿素a含量的影响大,其含量呈现先升后降趋势;对叶绿素b影响不明显;叶绿素总含量的变化趋势和叶绿素a相似,各处理组均高于对照。叶绿素总含量在0.525 mmol·L−1处理时达最大值,较对照高33.66%(P<0.01);处理浓度增大到0.700 mmol·L−1时含量不增反降,但依然高于对照(P<0.01);处理浓度增大到0.875 mmol·L−1时,总含量依然高于对照值,但差异不显著。由此可见,0.525 mmol·L−1的硅对金线莲的光合生长更有益,0.875 mmol·L−1的硅则无明显益处。
2.3 硅对金线莲氮素营养的影响
NBI反映作物早期氮素营养状况和长势,可快速测定并预测其产量。结果表明,硅处理后金线莲+1叶的NBI和Chl指数值均呈先增后减的趋势(见表1),而Flav值的变化则相反。在0.175 mmol·L−1处理后,Chl值较对照高11.71%(P<0.01),NBI值较对照高18.43%(P<0.05),Flav值较对照低,但差异不显著。当处理浓度为0.525 mmol·L−1时,NBI和Chl值最大,分别较对照高66.87%和24.70%,差异均达极显著水平(P<0.01);Flav值较对照低22.73%(P<0.01)。当浓度≥0.700 mmol·L−1时,NBI和Chl值均显著低于对照值(P<0.05);Flav值则显著高于对照(P<0.05)。硅对Anth值无影响。由此可见,金线莲对低浓度(0.175mmol·L−1)硅处理即可快速响应,当处理浓度为0.525 mmol·L−1时,金线莲的氮素营养状况达到最佳,氮素营养吸收利用好,极大地促进叶绿素的合成;但浓度增大后(≥0.700 mmol·L−1),金线莲的氮素营养状况出现异常变化,可能偏向次生代谢物质的累积,促进了总黄酮等其他成分的合成和累积。
表 1 不同浓度硅处理对金线莲氮平衡指数的影响Table 1. Effect of silicon application at varied concentrations on NBI of A. roxburghii硅Si/(mmol·L−1) 叶绿素指数Chl 类黄酮指数Flav 花青素指数Anth 氮平衡指数NBI 0 29.0±1.2 Cc 0.22±0.04 BCb 0.08±0.01 a 133.4±25.1 CDcd 0.175 32.4±5.3 Bb 0.21±0.03 Cbc 0.08±0.01 a 158.0±49.9 BCbc 0.350 34.6±3.2 ABa 0.20±0.03 Cc 0.08±0.01 a 175.2±26.9 Bb 0.525 36.2±4.4 Aa 0.17±0.02 Dd 0.08±0.00 a 222.5±46.9 Aa 0.700 26.3±2.3 CDd 0.25±0.04 ABa 0.08±0.01 a 107.7±10.6 Ee 0.875 24.7±1.6 Dd 0.26±0.05 Aa 0.08±0.01 a 99.8±20.7 Ee 数据以平均值±标准偏差表示(n=3),同列不同大、小写字母分别表示处理间差异达极显著(P<0.01)或显著水平(P<0.05)。表2同。 Data are presented as mean±SD (n = 3); those with different capital and lowercase letters on same column mean significant difference at P<0.01 and P<0.05, respectively. Same for Table 2. 2.4 硅对金线莲叶片POD酶活性的影响
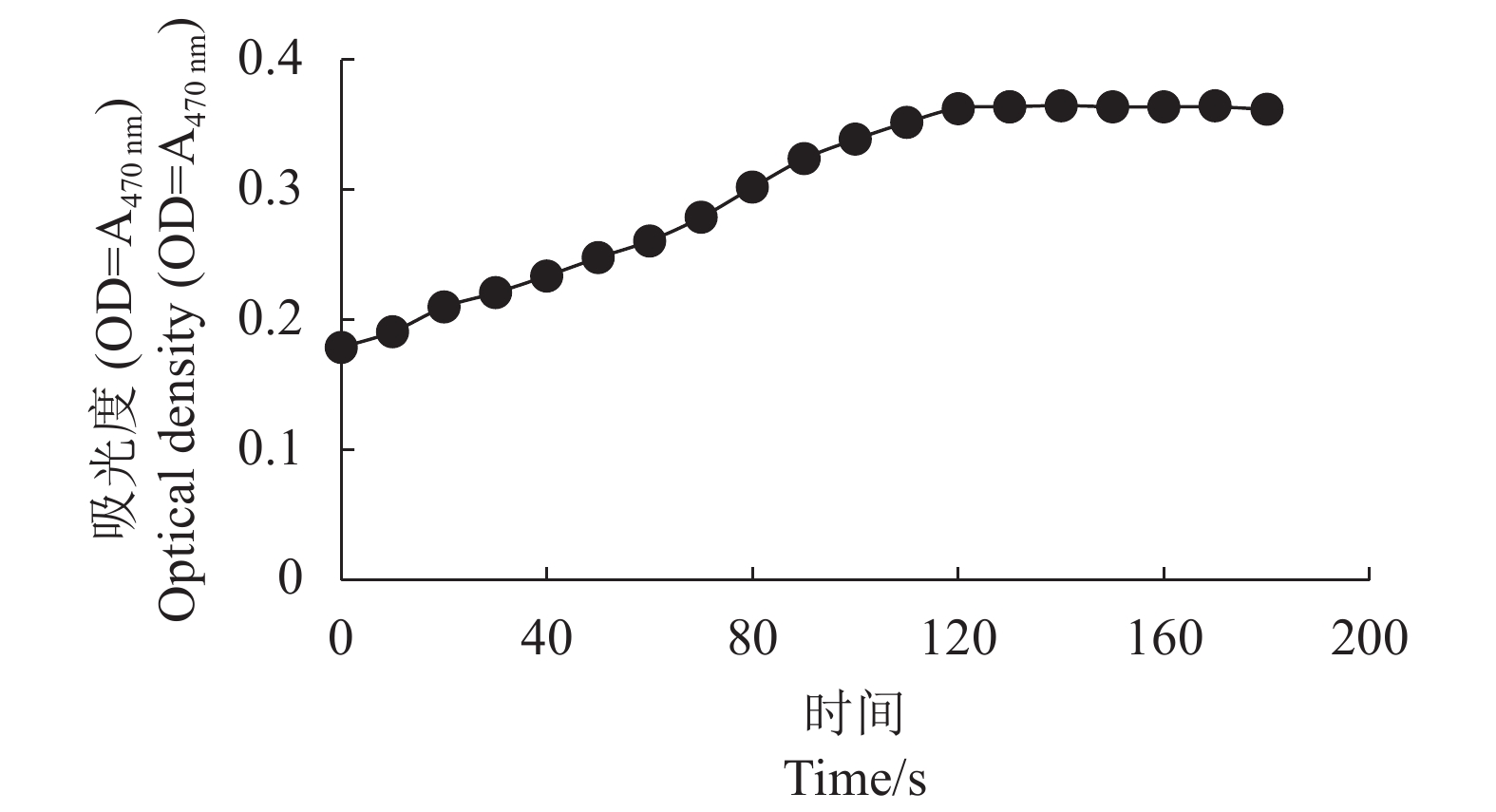
图3可见,测定金线莲POD酶活的最佳反应时段应控制在120 s内。POD酶在植物体内普遍存在且活性较高的一种抗氧化保护酶类,它可以清除植物体内的过氧化氢,对环境因子变化十分敏感,测定其活性可反映植物体内的代谢变化,是研究植物生理变化非常重要的指标。试验结果发现(见表2),对照组+1叶的POD酶活分别较+2叶和+3叶高68.87%和31.78%,表明新叶的抗氧化生理活性高于老叶。各处理组+1、+2和+3叶POD酶活较对照均有提高,表明硅处理增强了金线莲的抗氧化能力。POD酶活随处理浓度的增大呈现出双峰态势,在处理浓度为0.175 mmol·L−1和0.700 mmol·L−1时,各叶酶活均处于较高峰值,均显著高于对照组(P<0.01),各叶值大小均为+1>+3>+2叶。0.175 mmol·L−1处理组+1叶、+2叶和+3叶中POD酶活分别比对照高179.41%、231.13%和191.97%, 对其各叶抗氧化能力影响的大小为+2>+3>+1叶。0.700 mmol·L−1处理组+1、+2和+3叶中POD酶活性分别比对照高179.80%、210.60%和155.30%,抗氧化能力影响大小是+2叶>+1叶>+3叶。可见,硅处理对+2叶的抗氧化能力影响大。
表 2 不同浓度硅处理对金线莲不同叶位叶片POD酶活的影响Table 2. Effect of silicon application at varied concentrations on peroxidase activity in differently located leaves on an A. roxburghii plant硅Si/(mmol·L−1) +1 叶+1 leaf/(U·g−1) +2叶+2 leaf/(U·g−1) +3叶+3 leaf/(U·g−1) 0 510±66 Bc 302±8 Cd 387±68 Bb 0.175 1425±268 Aa 1000±103 Aa 1157±212 Aa 0.350 688±33 Bbc 528±138 BCc 577±53 Bb 0.525 950±233 Bb 745±120 ABbc 622±63 Bb 0.700 1427±189 Aa 938±164 Aab 988±258 Aa 0.875 923±163 Bb 750±140 ABbc 628±25 Bb 2.5 硅对金线莲多糖的影响
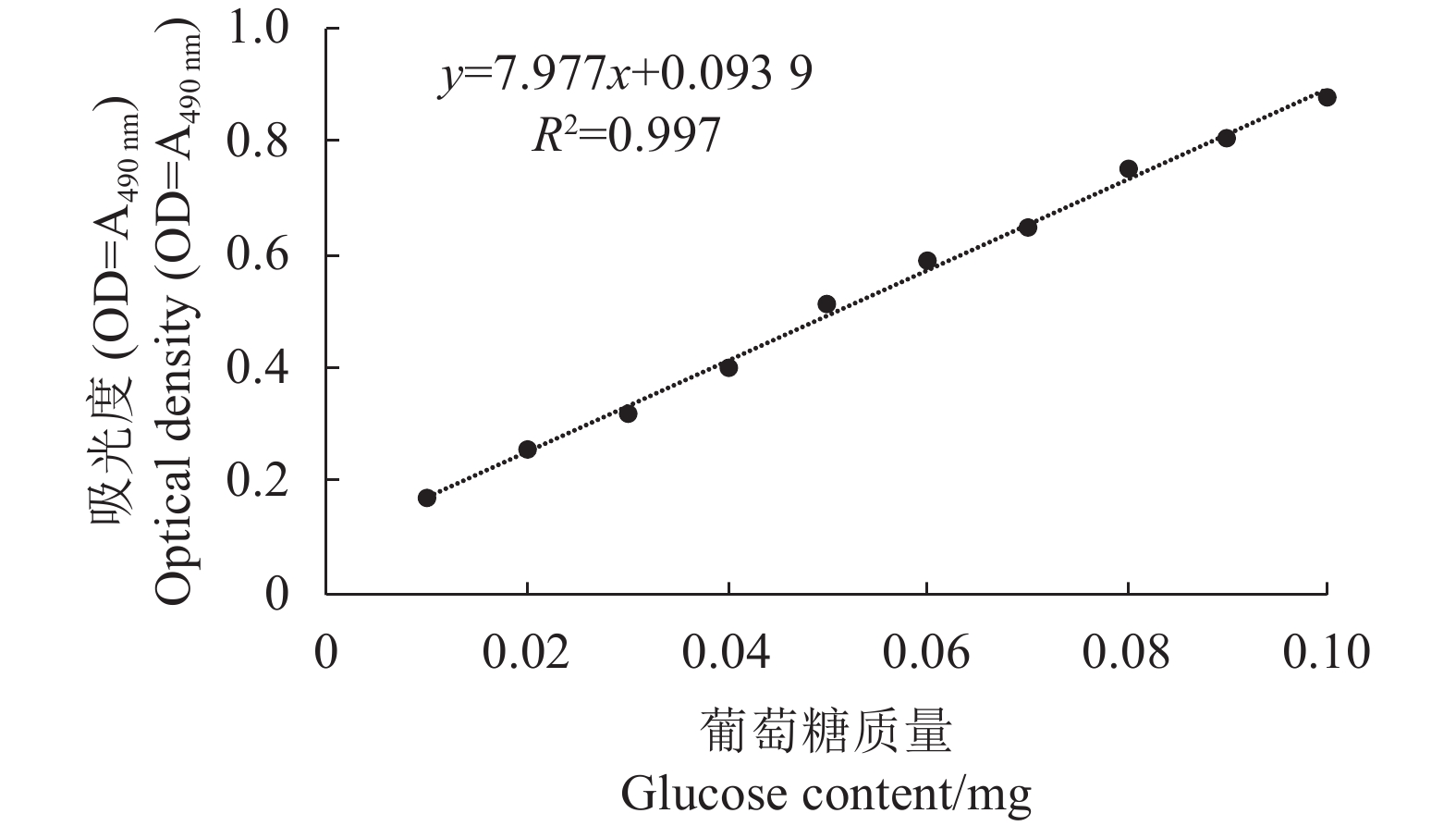
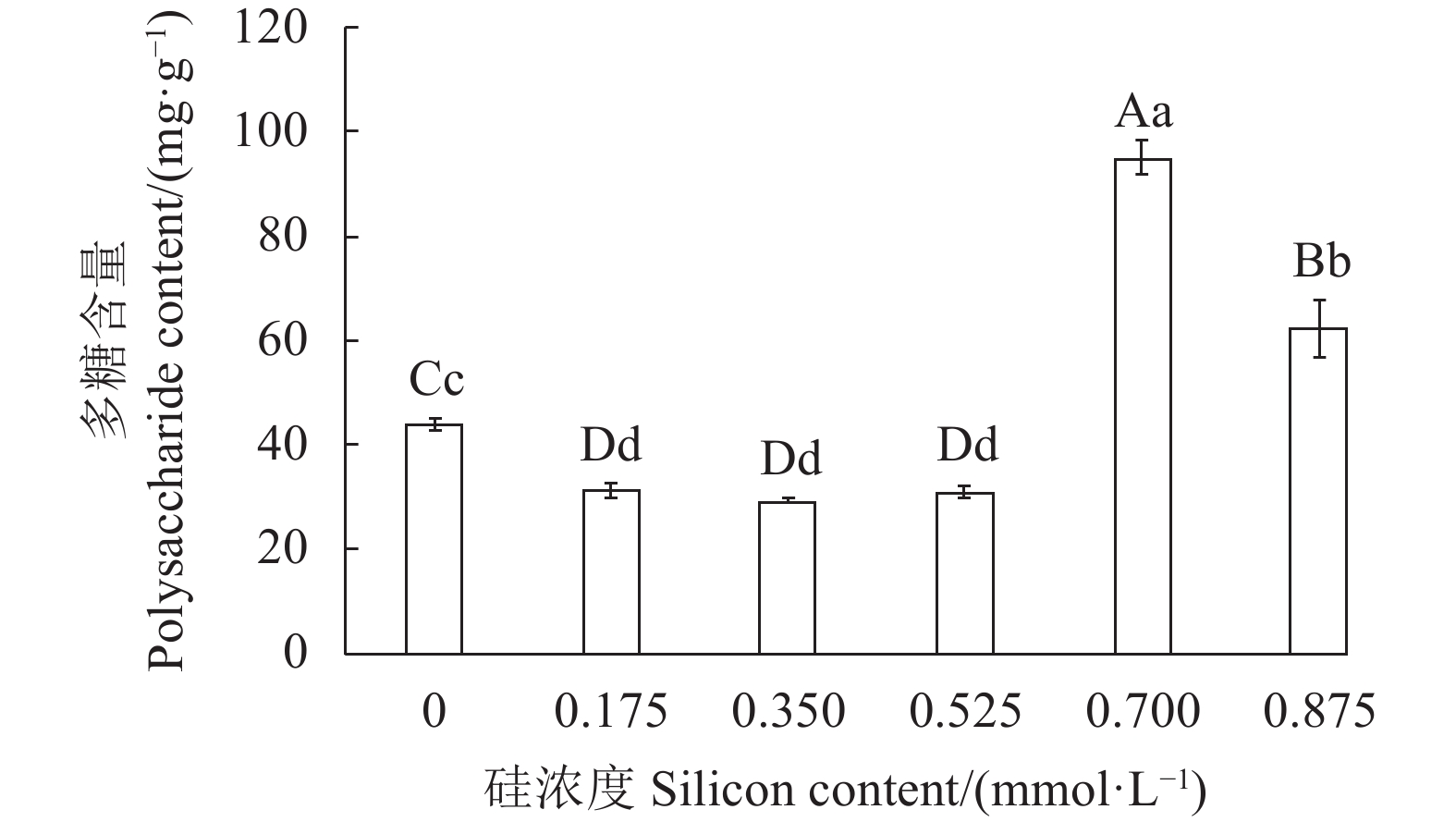
根据葡萄糖标准曲线(见图4)计算各处理样品中的多糖含量(以葡萄糖计)(见图5)。当硅浓度为0.175~0.525 mmol·L−1时,金线莲多糖含量呈下降趋势,显著低于对照值(P<0.05、0.01);当处理浓度增大到0.700 mmol·L−1时,多糖含量达到最高水平,是对照的2倍以上(P<0.05、0.01);继续增大到0.875 mmol·L−1时,多糖含量反而下降,但依然比对照高41.94%,差异显著(P<0.05、0.01)。由此可见,高浓度硅能提高金线莲的多糖含量,0.700 mmol·L−1硅处理对多糖累积效果最佳。
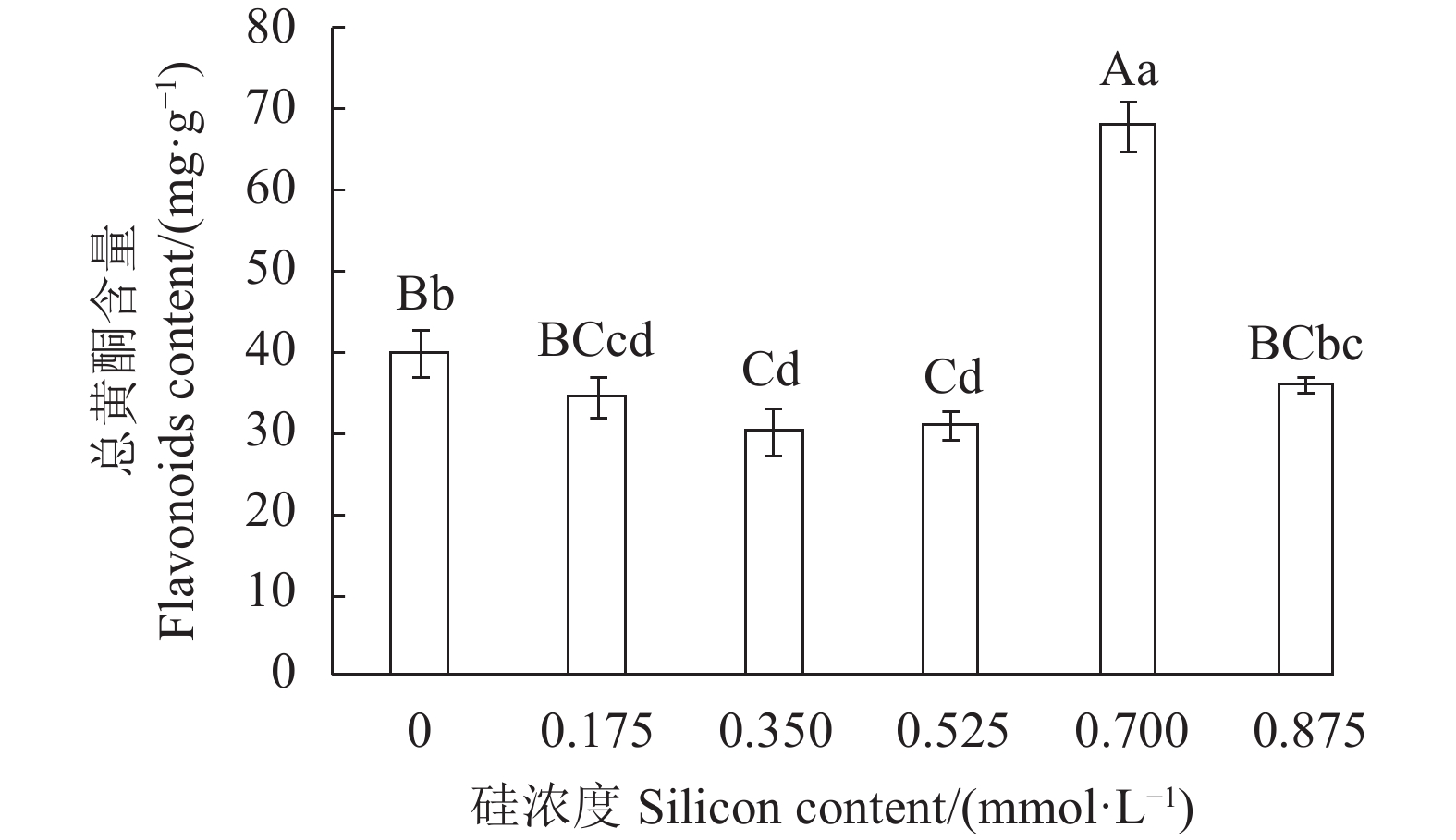
2.6 硅对金线莲总黄酮的影响
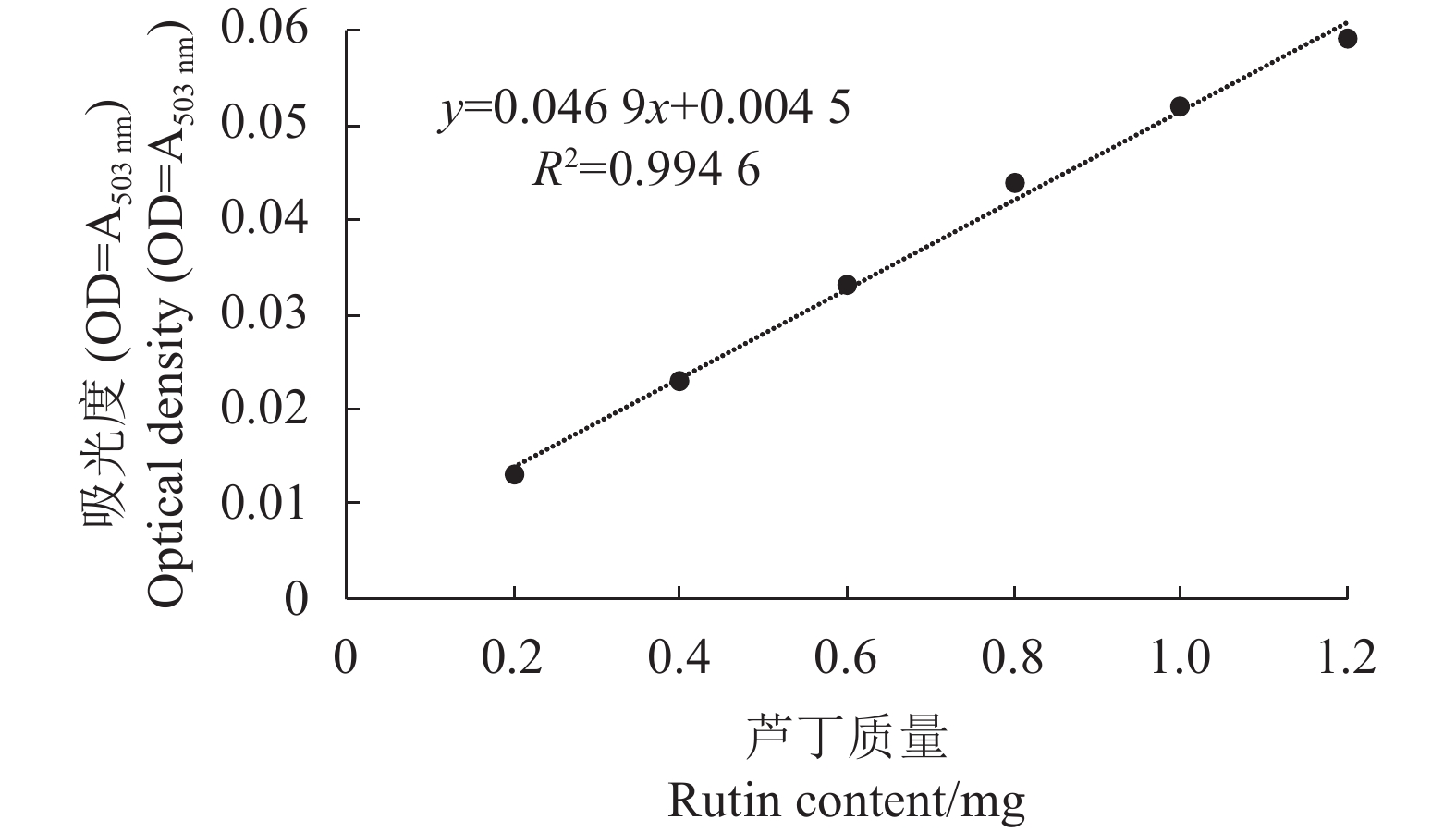
根据芦丁标准曲线(见图6)计算各处理样品中的总黄酮含量(以芦丁计)(见图7)。硅处理对金线莲总黄酮含量的影响变化与多糖较为相似。0.175~0.525 mmol·L−1处理时,金线莲的总黄酮含量也呈下降趋势,显著低于对照(P<0.05);浓度增大到0.700 mmol·L−1时,金线莲的总黄酮含量达到最高,比对照高71.45%(P<0.01);继续增大处理浓度到0.875 mmol·L−1时,总黄酮含量反而大幅下降,且低于对照,但差异不显著。由此可见,0.700 mmol·L−1硅处理最益于提高金线莲总黄酮含量,高浓度(≥0.875 mmol·L−1)处理反而会降低。
3. 讨论
单子叶植物大都属高硅累积植物(喜硅植物),其叶片的硅含量显著高于双子叶植物[29],施硅对其生长有利;金线莲也是单子叶植物,试验表明适宜浓度的硅对金线莲的生长也有益,但金线莲是否也属于高硅累积植物,还需通过测定其体内硅的含量来确定。浓度处理对比发现,0.175~0.700 mmol·L−1处理较0.875 mmol·L−1处理对鲜重增长效果更好,总叶绿素含量呈先升后降趋势,以及氮素营养吸收利用(NBI)也表现出低促高抑现象,硅对这三者的影响表现出一致性,表明低浓度硅较高浓度硅对金线莲生长更有益。已有研究认为低浓度硅会提高植物对N、P、K、Ca、Mg、Fe、Mn、Cu、Zn等元素的吸收利用,而高浓度硅会抑制磷、钙、镁等营养离子的吸收和利用[30]。0.525 mmol·L−1浓度硅处理后,总叶绿素含量、Chl值和NBI值均达最高值,表明该处理的金线莲对氮素营养吸收利用最好,能促进叶绿素合成并提高含量。已有研究发现,适量硅可促进植物氮素营养吸收、氨基酸(如L-谷氨酸)合成和原叶绿素酸酯及叶绿素的形成,能显著提高水稻、甘蔗和番茄的叶绿素总含量[31],还能使叶绿体片层结构和基粒增多,提高光合同化能力和增加物质累积[32]。
试验发现,硅对金线莲叶绿素总含量和NBI指数的影响变化趋势是一致的,符合李振海等[33]关于利用氮平衡指数建模估测叶绿素质量分数,具有较好精度的论断,可通过测定NBI指数实现叶绿素含量的快速及无损监测和估算。棉花叶片NBI值和Chl 值的变化与叶片全氮含量呈极显著正相关关系[34],NBI、Chl可作为作物氮素营养状况变化的快速诊断指标。因此,在金线莲栽培生产中,是否也可通过测定NBI和Chl值早期判断其氮素营养和生长状态值得进一步研究和探讨。
试验中发现,金线莲+1叶中的POD酶活性分别均较+2叶和+3叶的高,这可能与+1叶正处于发育成熟初期有关,因为POD也是木质素单体合成的关键酶,其活性在开始成熟或老化组织中活性较高, POD活性的增强亦可作为植物细胞和组织逐步成熟或衰老的一种生理指示。0.175 mmol·L−1的硅处理时,金线莲氮代谢及营养生长旺盛,增强POD酶活性有利于清除体内过多的自由基;另一个峰值出现在0.700 mmol·L−1处理, POD酶活性提高可能与酚类(类黄酮)和多糖等次生代谢物质的合成有关,因为POD不仅是植物酶促防御系统中的关键酶,作为代谢调节因子还参与酚类(类黄酮)物质及植保素的合成。现有研究发现,硅素营养与水稻叶片酚类化合物代谢存在密切联系;水稻在缺硅条件下,叶中的苯丙氨酸解氨酶(Phenylalanine Ammonia-lyase,PAL)活性和酚类化合物含量均极显著下降[35],而PAL正是连接初级代谢和苯丙烷类代谢、催化苯丙烷类代谢的酶,是酚类化合物代谢的关键酶和限速酶;硅素能在水稻叶上大量沉积,有助于提高叶片酚类化合物合成关键酶PAL的活性,以及调节4一香豆酸辅酶A连接酶(4CL)的活性及其编码基因的表达,促进水稻叶酚类化合物的合成[23]。试验结果也表明,0.700 mmol·L−1浓度处理能显著增加金线莲的总黄酮和多糖含量,且0.700 mmol·L−1的浓度优于0.875 mmol·L−1。
综上所述,施用适量的硅对金线莲水培是有益的。硅浓度为0.525 mmol·L−1时促进金线莲氮素营养吸收利用和光合机能,相对生长率最高,适用于营养生长;0.700 mmol·L−1硅处理使金线莲总黄酮和多糖含量最高,对提高其药用品质有益。今后,可进一步研究在金线莲不同栽培模式下进行硅处理和延长处理时间,对其不同器官中药效成分累积的影响,以及施硅对其抗病抗逆性的影响等方面开展研究,为金线莲的提质促产提供切实有效的栽培技术措施和科学的理论依据。
-
图 1 不同浓度硅处理对金线莲相对生长率的影响
图中不同大、小写字母分别表示处理间的差异达显著水平P<0.01或P<0.05,下图同。
Figure 1. Effect of silicon at varied concentrations on relative growth rate of A. roxburghii
Data with different capital and lowercase letters mean significant difference at P<0.01 and P<0.05, respectively. Same for following figures.
表 1 不同浓度硅处理对金线莲氮平衡指数的影响
Table 1 Effect of silicon application at varied concentrations on NBI of A. roxburghii
硅Si/(mmol·L−1) 叶绿素指数Chl 类黄酮指数Flav 花青素指数Anth 氮平衡指数NBI 0 29.0±1.2 Cc 0.22±0.04 BCb 0.08±0.01 a 133.4±25.1 CDcd 0.175 32.4±5.3 Bb 0.21±0.03 Cbc 0.08±0.01 a 158.0±49.9 BCbc 0.350 34.6±3.2 ABa 0.20±0.03 Cc 0.08±0.01 a 175.2±26.9 Bb 0.525 36.2±4.4 Aa 0.17±0.02 Dd 0.08±0.00 a 222.5±46.9 Aa 0.700 26.3±2.3 CDd 0.25±0.04 ABa 0.08±0.01 a 107.7±10.6 Ee 0.875 24.7±1.6 Dd 0.26±0.05 Aa 0.08±0.01 a 99.8±20.7 Ee 数据以平均值±标准偏差表示(n=3),同列不同大、小写字母分别表示处理间差异达极显著(P<0.01)或显著水平(P<0.05)。表2同。 Data are presented as mean±SD (n = 3); those with different capital and lowercase letters on same column mean significant difference at P<0.01 and P<0.05, respectively. Same for Table 2. 表 2 不同浓度硅处理对金线莲不同叶位叶片POD酶活的影响
Table 2 Effect of silicon application at varied concentrations on peroxidase activity in differently located leaves on an A. roxburghii plant
硅Si/(mmol·L−1) +1 叶+1 leaf/(U·g−1) +2叶+2 leaf/(U·g−1) +3叶+3 leaf/(U·g−1) 0 510±66 Bc 302±8 Cd 387±68 Bb 0.175 1425±268 Aa 1000±103 Aa 1157±212 Aa 0.350 688±33 Bbc 528±138 BCc 577±53 Bb 0.525 950±233 Bb 745±120 ABbc 622±63 Bb 0.700 1427±189 Aa 938±164 Aab 988±258 Aa 0.875 923±163 Bb 750±140 ABbc 628±25 Bb -
[1] 梁永超, 张永春, 马同生. 植物的硅素营养 [J]. 土壤学进展, 1993, 21(3):7−14. LIANG Y C, ZHANG Y C, MA T S. Review of the studies on silicon nutrition of plants [J]. PROGRESS IN SOIL SCIENCE, 1993, 21(3): 7−14.(in Chinese)
[2] EPSTEIN E. The anomaly of silicon in plant biology [J]. PNAS, 1994, 91(1): 11−17. DOI: 10.1073/pnas.91.1.11
[3] ARTHI V, SRIRAMACHANDRASEKHARAN M V, MANIVANNAN R, et al. Effect of silicon fertilization on agro-morphological traits of grand naine banana grown in typic ustifluvent soil [J]. International Journal of Plant & Soil Science, 2020: 38−46.
[4] 董倩, 黄国强, 王艳君, 等. 硅对果蔗组培腋芽苗增殖生长及相关指标的影响 [J]. 热带作物学报, 2018, 39(1):116−120. DOI: 10.3969/j.issn.1000-2561.2018.01.018 DONG Q, HUANG G Q, WANG Y J, et al. Effects of silicon on proliferation, growth and relevant parameters of in vitro cultured fruit sugarcane axillary bud seedlings [J]. Chinese Journal of Tropical Crops, 2018, 39(1): 116−120.(in Chinese) DOI: 10.3969/j.issn.1000-2561.2018.01.018
[5] TRIPATHI P, NA C I, KIM Y. Effect of silicon fertilizer treatment on nodule formation and yield in soybean (Glycine max L. ) [J]. European Journal of Agronomy, 2021, 122: 126172. DOI: 10.1016/j.eja.2020.126172
[6] LIU C G, LU W K, MA Q N, et al. Effect of silicon on the alleviation of boron toxicity in wheat growth, boron accumulation, photosynthesis activities, and oxidative responses [J]. Journal of Plant Nutrition, 2017, 40(17): 2458−2467. DOI: 10.1080/01904167.2017.1380817
[7] HOSSEINI S A, NASERI RAD S, ALI N, et al. The ameliorative effect of silicon on maize plants grown in Mg-deficient conditions [J]. International Journal of Molecular Sciences, 2019, 20(4): 969. DOI: 10.3390/ijms20040969
[8] 李炜蔷, 张逸, 石健, 等. 硅对大葱矿质元素吸收、分配特性及产量和品质的影响 [J]. 植物营养与肥料学报, 2016, 22(2):486−494. DOI: 10.11674/zwyf.14466 LI W Q, ZHANG Y, SHI J, et al. Effects of silicon on mineral element uptake and distribution, yield and quality of Chinese spring onion [J]. Journal of Plant Nutrition and Fertilizer, 2016, 22(2): 486−494.(in Chinese) DOI: 10.11674/zwyf.14466
[9] ZHANG Y, CHEN H T, LIANG Y, et al. Comparative transcriptomic and metabolomic analyses reveal the protective effects of silicon against low phosphorus stress in tomato plants [J]. Plant Physiology and Biochemistry, 2021, 166: 78−87. DOI: 10.1016/j.plaphy.2021.05.043
[10] 宁东峰, 梁永超. 硅调节植物抗病性的机理: 进展与展望 [J]. 植物营养与肥料学报, 2014, 20(5):1280−1287. DOI: 10.11674/zwyf.2014.0525 NING D F, LIANG Y C. Silicon-mediated plant disease resistance: Advance and perspectives [J]. Journal of Plant Nutrition and Fertilizer, 2014, 20(5): 1280−1287.(in Chinese) DOI: 10.11674/zwyf.2014.0525
[11] 陈翠芳, 钟继洪, 李淑仪. 施硅对抑制植物吸收重金属镉的效应研究进展 [J]. 生态学杂志, 2007, 26(4):567−570. DOI: 10.3321/j.issn:1000-4890.2007.04.021 CHEN C F, ZHONG J H, LI S Y. Research progress on inhibitory effects of silicon on cadmium absorption by plants [J]. Chinese Journal of Ecology, 2007, 26(4): 567−570.(in Chinese) DOI: 10.3321/j.issn:1000-4890.2007.04.021
[12] VACULÍK M, KOVÁČ J, FIALOVÁ I, et al. Multiple effects of silicon on alleviation of nickel toxicity in young maize roots [J]. Journal of Hazardous Materials, 2021, 415: 125570. DOI: 10.1016/j.jhazmat.2021.125570
[13] VOLETI S R, PADMAKUMARI A P, RAJU V S, et al. Effect of silicon solubilizers on silica transportation, induced pest and disease resistance in rice (Oryza sativa L. ) [J]. Crop Protection, 2008, 27(10): 1398−1402. DOI: 10.1016/j.cropro.2008.05.009
[14] HAN Y Q, WEN J H, PENG Z P, et al. Effects of silicon amendment on the occurrence of rice insect pests and diseases in a field test [J]. Journal of Integrative Agriculture, 2018, 17(10): 2172−2181. DOI: 10.1016/S2095-3119(18)62035-0
[15] THORNE S J, HARTLEY S E, MAATHUIS F J M. The effect of silicon on osmotic and drought stress tolerance in wheat landraces [J]. Plants, 2021, 10(4): 814. DOI: 10.3390/plants10040814
[16] 沈廷明, 吴仲玉, 黄春情, 等. 金线莲化学成分、药理、组培及栽培研究进展 [J]. 海峡药学, 2016, 28(12):26−30. DOI: 10.3969/j.issn.1006-3765.2016.12.010 SHEN T M, WU Z Y, HUANG C Q, et al. Study on Anoectochilus roxburghii's chemical constituents, pharmacodynamics, tissue culture and cultivation [J]. Strait Pharmaceutical Journal, 2016, 28(12): 26−30.(in Chinese) DOI: 10.3969/j.issn.1006-3765.2016.12.010
[17] 陈育青, 林艺华, 邹毅辉, 等. 金线莲生药鉴定、活性成分影响因素及药理作用研究进展 [J]. 中成药, 2020, 42(8):2141−2144. DOI: 10.3969/j.issn.1001-1528.2020.08.033 CHEN Y Q, LIN Y H, ZOU Y H, et al. Progress in Anoectochilus roxburghii's biochemical drug identification, factors affecting active ingredients and pharmacological effects [J]. Chinese Traditional Patent Medicine, 2020, 42(8): 2141−2144.(in Chinese) DOI: 10.3969/j.issn.1001-1528.2020.08.033
[18] 薛梅花, 卢石孔, 翁文, 等. 不同种植方式对金线莲黄酮类化合物含量的影响 [J]. 福建分析测试, 2021, 30(1):33−36. DOI: 10.3969/j.issn.1009-8143.2021.01.07 XUE M H, LU S K, WENG W, et al. Effects of planting methods on the content of flavonoids in Anoectochilus roxburghii [J]. Fujian Analysis & Testing, 2021, 30(1): 33−36.(in Chinese) DOI: 10.3969/j.issn.1009-8143.2021.01.07
[19] 吴水华, 程伟青. 不同栽培方式对金线莲中多糖含量的影响 [J]. 现代中药研究与实践, 2016, 30(6):8−11. WU S H, CHENG W Q. Effects of different cultivation methods on polysaccharide content of different Anoectochilus roxburghii [J]. Research and Practice on Chinese Medicines, 2016, 30(6): 8−11.(in Chinese)
[20] 王建寰, 张文晋, 郎多勇, 等. 硅对盐胁迫下甘草非药用部位总黄酮、总皂苷积累动态的影响 [J]. 世界科学技术-中医药现代化, 2018, 20(7):1251−1255. WANG J H, ZHANG W J, LANG D Y, et al. Effects of silicon on the accumulation of total flavonoids and total saponins of non-medicinal parts of glvarrhiza uralensis fisch. under salt stress [J]. Modernization of Traditional Chinese Medicine and Materia Medica-World Science and Technology, 2018, 20(7): 1251−1255.(in Chinese)
[21] 于涛, 张海楼, 隽英华, 等. 施肥模式对水稻稻瘟病抗性的影响 [J]. 江苏农业科学, 2014, 42(7):113−116. DOI: 10.3969/j.issn.1002-1302.2014.07.038 YU T, ZHANG H L, JUAN Y H, et al. Effect of fertilization modes on resistance to rice blast [J]. Jiangsu Agricultural Sciences, 2014, 42(7): 113−116.(in Chinese) DOI: 10.3969/j.issn.1002-1302.2014.07.038
[22] 何永美, 湛方栋, 祖艳群, 等. 大田条件下UV-B辐射对元阳梯田2个地方水稻品种硅、类黄酮和总酚含量的影响 [J]. 农业环境科学学报, 2013, 32(8):1500−1506. DOI: 10.11654/jaes.2013.08.002 HE Y M, ZHAN F D, ZU Y Q, et al. Effects of UV-B radiation on the contents of silicon, flavonoids and total phenolic of two local rice varieties in Yuanyang Terrace under field conditions [J]. Journal of Agro-Environment Science, 2013, 32(8): 1500−1506.(in Chinese) DOI: 10.11654/jaes.2013.08.002
[23] CARVER T L W, ROBBINS M P, THOMAS B J, et al. Silicon deprivation enhances localized autofluorescent responses and phenylalanine ammonia-lyase activity in oat attacked by Blumeria graminis [J]. Physiological and Molecular Plant Pathology, 1998, 52(4): 245−257. DOI: 10.1006/pmpp.1998.0149
[24] 杨开兴. 不同施肥模式对金线莲生长及生理特性的影响 [J]. 林业和草原机械, 2020, 1(4):34−38. YANG K X. Effects of different fertilization modes on growth and physiological characteristics of Anoectochilus [J]. Forestry and Grassland Machinery, 2020, 1(4): 34−38.(in Chinese)
[25] 应震, 杨燕萍, 周庄, 等. 不同基质和年份栽培对金线莲药用成分的影响 [J]. 浙江农业科学, 2020, 61(7):1356−1357. YING Z, YANG Y P, ZHOU Z, et al. Effects of different substrates and years on medicinal components of Anoectochilus roxburghii [J]. Journal of Zhejiang Agricultural Sciences, 2020, 61(7): 1356−1357.(in Chinese)
[26] 张文林, 任亚超, 张益文, 等. 不同光质LED光源对转基因杨树叶片Bt毒蛋白含量及叶绿素荧光参数的影响 [J]. 核农学报, 2016, 30(8):1639−1645. DOI: 10.11869/j.issn.100-8551.2016.08.1639 ZHANG W L, REN Y C, ZHANG Y W, et al. Effect of different LED light qualities on bt toxic protein content and chlorophyll fluorescence of transgenic poplar leaves [J]. Journal of Nuclear Agricultural Sciences, 2016, 30(8): 1639−1645.(in Chinese) DOI: 10.11869/j.issn.100-8551.2016.08.1639
[27] 常福辰, 陆长梅, 沙莎. 植物生物学实验[M]. 南京: 南京师范大学出版社, 2007. [28] 张志信, 张铁, 赵保发, 等. 文山野生金线莲总黄酮及多糖含量测定 [J]. 时珍国医国药, 2009, 20(6):1362−1364. DOI: 10.3969/j.issn.1008-0805.2009.06.032 ZHANG Z X, ZHANG T, ZHAO B F, et al. Determination of total flavonoids and polysaccharide of the wild anocetochilus plants in Wenshan prefecture [J]. Lishizhen Medicine and Materia Medica Research, 2009, 20(6): 1362−1364.(in Chinese) DOI: 10.3969/j.issn.1008-0805.2009.06.032
[29] 熊蔚. 湿地草本植物叶硅含量特征及其与环境因子的关系[D]. 杭州: 杭州师范大学, 2016. XIONG W. Characteristics of silicon contents and their relationship to environmental factorsin wetland herbaceous plants[D]. Hangzhou: Hangzhou Normal University, 2016. (in Chinese)
[30] 李晓艳. 不同吸硅型植物硅同位素组成和营养元素分布特征[D]. 杭州: 浙江大学, 2013. LI X Y. Silicon isotope compositions and distribution patterns of Si and others nutritional elements in the different absorbing-silicon plants[D]. Hangzhou: Zhejiang University, 2013. (in Chinese)
[31] 曹逼力, 徐坤, 石健, 等. 硅对番茄生长及光合作用与蒸腾作用的影响 [J]. 植物营养与肥料学报, 2013, 19(2):354−360. DOI: 10.11674/zwyf.2013.0211 CAO B L, XU K, SHI J, et al. Effects of silicon on growth, photosynthesis and transpiration of tomato [J]. Plant Nutrition and Fertilizer Science, 2013, 19(2): 354−360.(in Chinese) DOI: 10.11674/zwyf.2013.0211
[32] 高臣, 刘俊渤, 常海波, 等. 硅对水稻叶片光合特性和超微结构的影响 [J]. 吉林农业大学学报, 2011, 33(1):1−4. GAO C, LIU J B, CHANG H B, et al. Effects of silicon on rice leaf photosynthesis and ultrastructure [J]. Journal of Jilin Agricultural University, 2011, 33(1): 1−4.(in Chinese)
[33] 李振海, 王纪华, 贺鹏, 等. 基于Dualex氮平衡指数测量仪的作物叶绿素含量估算模型 [J]. 农业工程学报, 2015, 31(21):191−197. DOI: 10.11975/j.issn.1002-6819.2015.21.025 LI Z H, WANG J H, HE P, et al. Modelling of crop chlorophyll content based on Dualex [J]. Transactions of the Chinese Society of Agricultural Engineering, 2015, 31(21): 191−197.(in Chinese) DOI: 10.11975/j.issn.1002-6819.2015.21.025
[34] 殷星, 侯振安, 冶军, 等. 应用多酚–叶绿素仪监测棉花氮素营养状况研究 [J]. 植物营养与肥料学报, 2021, 27(7):1198−1212. DOI: 10.11674/zwyf.20617 YIN X, HOU Z N, YE J, et al. Application of polyphenol-chlorophyll meter to monitor cotton N nutrition status [J]. Journal of Plant Nutrition and Fertilizers, 2021, 27(7): 1198−1212.(in Chinese) DOI: 10.11674/zwyf.20617
[35] 吴杏春, 陈裕坤, 李奇松, 等. 硅营养对UV-B辐射条件下水稻酚类代谢的影响 [J]. 中国农学通报, 2009, 25(24):225−230. WU X C, CHEN Y K, LI Q S, et al. Effects of silicon nutrition on phenolics metabolization of rice (Oryza sativa L. ) exposed to enhanced ultraviolet-B [J]. Chinese Agricultural Science Bulletin, 2009, 25(24): 225−230.(in Chinese)
-
期刊类型引用(3)
1. 陈玮,甘志凯,谌希. 硒与AM真菌对金线莲微量元素吸收及相关药用品质的影响. 山东农业科学. 2025(01): 87-95 .  百度学术
百度学术
2. 张闻婷,梅瑜,王继华. 珍稀药用植物金线莲研究现状与展望. 中国农学通报. 2024(05): 16-26 .  百度学术
百度学术
3. 危青泉. 林下仿野生栽培密度和采收期对金线莲种植的影响. 绿色科技. 2023(05): 79-82 .  百度学术
百度学术
其他类型引用(1)




 下载:
下载: