SSR Markers Associated with Sex-difference of Populus yunnanensis Dode
-
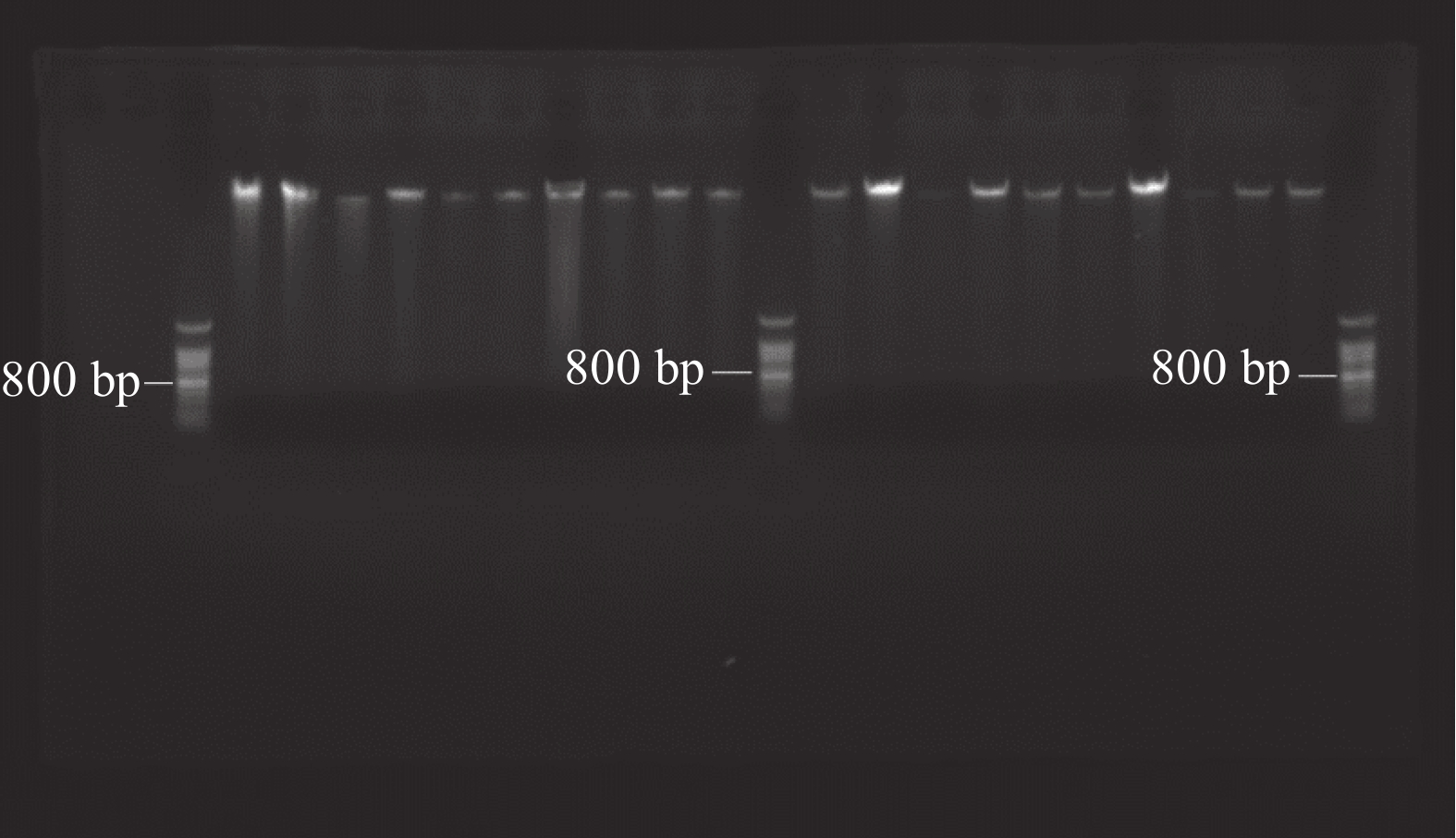
摘要:目的 在滇杨幼苗时期和开花前利用形态差异对雌雄株进行性别鉴定极为困难,因此亟需探明对其性别进行快速鉴定的分子标记方法。方法 以滇杨雌雄各30株为材料,利用简单重复序列(SSR)筛选与滇杨性别相关的分子标记,并利用所获得的SSR标记对未知性别滇杨幼苗进行鉴定,分析滇杨苗期的性别分化情况。结果 从已报道的相关文献中选出15对与植物性别连锁的SSR引物,经试验筛选出1对(BPCA90)在琼脂糖凝胶检测中显现清晰条带且反应稳定的SSR引物,并将这对引物经聚丙烯酰胺凝胶电泳进行复筛,经PCR扩增后在滇杨雄株中出现1条特异性条带,大小在680 bp左右。利用这对SSR引物对30株滇杨幼苗进行性别鉴定,结果表明雄株明显多于雌株,且比例为13∶2。结论 试验筛选所得到的SSR引物可以用于滇杨早期进行性别鉴定。研究结果可作为滇杨早期性别鉴定的遗传标记,为今后滇杨在生产中的分性别利用提供技术支持。Abstract:Objective Means utilizing molecular markers to differentiate rapidly and accurately male and female Populus yunnanensis plants at young stages was investigated.Method Using simple sequence repeats (SSR), molecular markers were screened for those might associate with the sex of P. yunnanensis at seedling stages and before flowering.Result Fifteen pairs of SSR primers were selected from the reported literatures. One of them, coded BPCA90, showed clear bands and stable reaction in agarose gel detection. After rescreening the primer by polyacrylamide gel electrophoresis, a specific band of approximately 680 bp appeared in the PCR amplification of male P. yunnanensis. Subsequent testing on 30 plants using these SSR primers showed significantly more males than females in a ratio of 13 to 2.Conclusion Short of a visible morphological sign for the determination, the SSR primers screened by this study appeared to suffice the general purpose of differentiating the sex of P. yunnanensis at early growth stage.
-
Keywords:
- Populus yunnanensis Dode /
- SSR /
- primer screening /
- gender identification
-
0. 引言
【研究意义】枇杷[Eriobotrya japonica Lindl.]是原产于我国的常绿特色果树,果实春末夏初上市,甜酸适口,深受消费者喜好。福建是我国枇杷主产区,20世纪90年代以来,推广早钟6号、解放钟等枇杷品种,配套集约化栽培技术,有效推动了枇杷产业快速发展。随着生活水平的提高,消费者对枇杷品质的要求也在逐步提高,亟需推广品质更优良的鲜食品种。高接换种技术可利用原有树体的生长基础实现品种快速更新的目的,较新植小苗见效更快、产量损失更少,已成为福建枇杷产区品种更新的主要措施。研究高接换种后幼龄枇杷丰产树冠的快速形成以及枝梢的数量和质量是枇杷高效树形培养的关键。【前人研究进展】果树冠层结构[1,2]、光合特性[3,4]、枝梢类型、比例与分布[5,6]影响冠层内的光照、温度等微域环境[3],进而影响果实品质和产量[2,7],高效树形的培养是苹果(Malus pumila Mill)[8]、桃 [Prunus persica (L.) Batsch][9,10]、梨(Prunus spp)[11,12]等树种的丰产栽培关键技术。枇杷的树形有自然圆头形(主干分层形)、开心形(单层杯状形、双层杯状形)、变则主干形、桌面形等[13],在基本树形的基础上,又延伸出多主枝自然圆头形[14]、疏枝圆头形[15]、双层圆头形[16]、矮化开心形[17]、双层开心形[18]、低干矮冠形[16]等树形,近年来多头高接换种树以多主枝自然圆头形和多主枝开心形为主。枇杷的枝梢数量与单株产量密切相关[19],枝梢生长质量显著影响果实品质和产量,3种不同矮化树体生长型的枇杷品种资源的枝梢生长量和枝梢空间分布特点也不同,随树冠高度增加,枝梢长度、粗度、叶片数等呈增大趋势[20],外围的枝、叶生长影响下部和内膛枝、叶的生长,适宜的枝梢密度是提高整体枝梢质量的重要影响因子,是枇杷高效树形培养的关键技术。【本研究切入点】前人的研究主要侧重于枇杷不同树形培养的技术总结与推广,但不同树形的主要结果部位、树冠不同部位的枝梢分布特点、质量差异等对枇杷生长与结果的具体影响因子尚不明确。【拟解决的关键问题】本研究拟结合枇杷品种结构调整优化过程中高接换种技术的推广,探讨高接换种后多主枝自然圆头形和多主枝矮化开心形两种树形,冠层内不同部位、不同层次的枝梢分布特点及质量差异,为高接换种后丰产树形的培养提供参考。
1. 材料与方法
1.1 试验材料
试验在福建省莆田市城厢区常太镇宏耕农业有限公司枇杷基地(东经118.879°,北纬25.543°)进行,基地位于东圳水库上游,海拔200 m左右,坡向东南,梯台宽度2~4 m。该地属南亚热带海洋性季风气候,年平均气温18~20 ℃,平均日照时数1996 h,无霜期330~350 d,年降雨量1400~1900 mm。试验树株距4.0 m,原定植品种为解放钟,树龄10 a,干高40~80 cm,第一级主枝2~4个。多头高接品种为贵妃,高接在一级主枝上,嫁接口高度100.0 cm左右,每株高接2~6个接穗。试验调查2种树形:(1)多主枝自然圆头形:高接成活后,树冠内选留2~4个不同方位的健壮新梢培养为主枝,主枝不摘心、不短截修剪,每个主枝上间隔60.0~100.0 cm分层培养1~3个副主枝,定型后的树高控制在350.0 cm左右;(2)多主枝矮化开心形:待高接新梢老熟后,树冠不同方位选留2~4个生长健壮的新梢培养为主枝,用编织绳向树冠外围不同方位拉枝,枝角70~90°,主枝上间隔30~50 cm留1~2个健壮枝梢培养为副主枝,新梢老熟后采用拉枝措施矮化树形,定型后的树高控制在250.0 cm左右。两种树形定型后(图1-A、B),均采用1个中心枝+1个侧枝方式留梢,其余肥水、花果管理一致,树体长势均健壮。
1.2 调查方法
2017年11月枇杷抽穗期,分别从两种树形中选择树体长势、生长量较一致的高接换种5年生试验树各6株,2株1个小区,3次重复。因该基地枇杷树体的枝梢量总体偏少,试验参考邓朝军等[20]的方法加以调整对树冠进行分格定位,以主干为中心,用长度100.0 cm定制铝塑管将树冠分割成长宽高100.0 cm×100.0 cm×100.0 cm的立方体小格,并对每个立方体进行定位、编号。调查树高、冠幅、叶幕层厚及各个立方体内的枝梢数、花穗数,计算枝梢抽穗率(枝梢抽穗率/%=花穗数/总枝梢数×100),将每个立方体内的枝梢数和花穗数定义为枝梢密度和花穗密度,单位为个·m−3;测量每个立方体内有代表性的枝梢长度、粗度和枝角,统计每个枝梢上的叶片数,计算节间长度。用卷尺测量树高、冠幅、叶幕层厚、枝梢长度,用游标卡尺(0.01 mm)测量枝梢粗度,用数显量角器(精度0.1°)测量枝角。
为了更好定位和表述,垂直方向上,根据离地高度将树冠分为F1层(树高0.0~100.0 cm)、F2层(树高100.1~200.0 cm)、F3层(树高200.1~300.0 cm)、F4层(树高>300.0 cm);水平方向上,根据与主干距离分为P1区(内部,距离中心干0.0~100.0 cm)、P2区(中部,距离中心干100.1~200.0 cm)、P3区(外围,距离中心干>200. 0 cm)(图1-C)。因两种处理的嫁接口高度100.0 cm左右,F1层内均无枝梢,分析时以叶幕层所在范围为主。
1.3 数据处理与分析
用Excel 2007、DPS7.0分析数据,Origin 2018绘图。
2. 结果与分析
2.1 枇杷两种树形的树体生长量差异
由表1可知,高接后5年生贵妃枇杷多主枝自然圆头形的树高、叶幕层厚、冠幅、枝梢数、花穗数、枝梢抽穗率、枝角、节间长度均显著或极显著大于多主枝矮化开心形,其中多主枝自然圆头形的树高和叶幕层厚分别比多主枝矮化开心形增大40.6%和61.8%,枝梢数和花穗数分别增多37.4%和50.5%,枝梢抽穗率提高7.1%,节间长度增高13.3%,枝梢更直立,枝角增大9.9°,粗长比增加0.02,但枝梢长度、粗度和叶片数分别比多主枝矮化开心形减少14.0%、9.1%和20.7%。由此可知,多主枝自然圆头形的树体生长量较多主枝矮化开心形显著增大,尤其是枝梢数和花穗数明显增加,但枝梢长势总体上弱于多主枝矮化开心形。
表 1 贵妃枇杷两种树形的树体生长量比较Table 1. Growth of two types of loquat tree项目Item 多主枝自然圆头形
Naturally round head tree
with multiple main branches多主枝矮化开心形
Dwarf, open heart-shaped
tree with multiple main branches树高 Tree height/cm 355.67±25.11aA 253.07±2.65bB 冠幅 Crown diameter Canopy/cm 500.67±47.16×447.67±61.17aA 427.67±33.56×356.33±31.82bB 树况 Tree condition 叶幕层厚 Thickness of canopy layers/cm 303.21±19.97aA 187.39±12.50bB 枝梢数 Number of branches 191.26±26.51aA 139.38±24.54bB 花穗数 Number of flower spikes 146.27±8.33aA 97.06±11.71bB 枝梢抽穗率 Flowering branch rate/% 76.65±14.57aA 69.60±9.54bA 长度 Length/cm 38.89±3.93bA 45.24±3.29aA 粗度 Diameter/mm 10.95±0.82bB 12.04±0.94aA 枝梢 Branch tip 叶片数 leave number 23.44±3.06bB 29.29±2.32aA 枝角 Branch/° 40.46±6.03aA 30.58±3.68bB 节间长度 Internode length/cm 1.79±0.17aA 1.58±0.14bA 粗长比 Shoot length/diameter ratio 0.28±0.01aA 0.26±0.01bA 同一列中大写字母表示0.01显著水平差异、小写字母表示0.05显著水平差异。下同。
In the same column, majuscule indicate a significant level difference of 0.01 and lowercase letters indicate a significant level difference of 0.05. The same below.2.2 枇杷两种树形冠层内枝梢和花穗的分布特点
2.2.1 两种树形冠层内枝梢和花穗的水平分布特点
从贵妃枇杷冠层枝梢数和花穗数的水平分布来看,多主枝自然圆头形冠层的单位投影面积内枝梢数为9个·m−2、花穗数7个·m−2(图2-A);P1区分布23.16%的枝梢、22.67%的花穗,单位投影面积内枝梢数9~13个·m−2、平均11个·m−2,花穗数2~15个·m−2、平均7个·m−2,平均枝梢抽穗率76.57%;P2区占总枝梢数的63.68%、占总花穗数的64.67%,单位投影面积内枝梢数6~15个·m−2、平均10个·m−2,花穗数4~15个·m−2、平均8个·m−2,平均枝梢抽穗率80.29%;P3区占枝梢数13.16%、占花穗数12.67%,单位投影面积内枝梢数2~8个·m−2、平均4个·m−2,单位投影面积内花穗数2~5个·m−2、平均3个·m−2,平均枝梢抽穗率82.64%。
![]() 图 2 两种树形冠层内枝梢和花穗的水平分布A、B为多主枝自然圆头形;C、D为多主枝矮化开心形;X、Y轴数值为与主干距离。Figure 2. Horizontal distribution of branches (left) and panicles (right) on canopies of two types of loquat treeA、B: Naturally round head tree with multiple main branches;C、D: dwarf, open heart-shaped tree with multiple main branches;The X-axis and Y-axis value is the distance from the trunk.
图 2 两种树形冠层内枝梢和花穗的水平分布A、B为多主枝自然圆头形;C、D为多主枝矮化开心形;X、Y轴数值为与主干距离。Figure 2. Horizontal distribution of branches (left) and panicles (right) on canopies of two types of loquat treeA、B: Naturally round head tree with multiple main branches;C、D: dwarf, open heart-shaped tree with multiple main branches;The X-axis and Y-axis value is the distance from the trunk.多主枝矮化开心形冠层内单位投影面积的枝梢数8个·m−2、花穗数6个·m−2(图2-B);37.76%的枝梢、28.43%的花穗分布在P1区,该区的枝梢密度较大且分布均匀,单位投影面积的枝梢数13~14个·m−2、平均13个·m−2,花穗数6~10个·m−2、平均7个·m−2,平均枝梢抽穗率53.87%;60.84%的枝梢数、69.61%花穗数分布在P2区,该区的枝梢、花穗分布差异较大,单位投影面积的枝梢数1~14个·m−2、平均7个·m−2,花穗1~12个·m−2、平均6个·m−2,平均枝梢抽穗率83.80%;P3区仅个别区有枝梢和花穗。
从水平分布来看,两种树形的枝梢数、花穗数均主要分布在P2区,其次是P1区,但P1区的单位投影面积的枝梢数、花穗数均较P2区多;多主枝矮化开心形与多主枝自然圆头形相比,P1区的枝梢数增多3个·m−2、枝梢抽穗率降低22.70个百分点、花穗分布更均匀,P2区的枝梢数减少3个·m−2、花穗数减少2个·m−2、枝梢抽穗率差异不显著,P3区无枝梢和花穗。
2.2.2 两种树形冠层内枝梢和花穗的垂直分布特点
由图3可知,多主枝自然圆头形的枝梢和花穗主要分布在F2层(40.96%、36.05%)和F3层(44.15%、46.26%),F4层仅占15.43%、17.69%,枝梢数和花穗数均表现为F3层>F2层>F4层,枝梢抽穗率为F4层(95.13%)>F3层(82.23%)>F2层(69.03%);多主枝矮化开心形冠层内66.43%的枝梢、69.31%的花穗分布在F2层,其余枝梢与花穗分布在F3层,单位面积内的枝梢数和花穗数表现为F2层>F3层,但两层间的枝梢抽穗率差异小(F2层74.95%、F3层70.66%)。
2.2.3 两种树形冠层内不同部位枝梢和花穗的分布特点
由图4-A可知,多主枝自然圆头形冠层可分割成4层84个体积1 m3的立方体小格,扣除F1层24个后,叶幕层分成60个体积1 m3的小格;叶幕层内无枝梢的小格10个,占16.67%,其中F2层3个、F3层5个、F4层2个;格内枝梢数1~9个·m−3、花穗数1~8个·m−3,其中1~4个·m−3枝梢、花穗的小格数分别有34个和40个,占56.67%、66.67%;≥5个·m−3枝梢和花穗的小格分别有16个、9个,占26.67%、15.00%。28.57%、30.69%的枝梢分布在F2、F3层的P2区,10.05%、10.58%分布在F3、F4层P1区,P3区仅F2、F3层有9.52%、3.17%,F3、F4层P1区和F3层P2区平均枝梢数5个·m−3,其次是F2层P2区4个·m−3,其余区域仅1~2个·m−3,花穗数也有相同趋势。
![]() 图 4 两种树形冠层内不同部位枝梢(左图)和花穗(右图)分布情况A、B为多主枝自然圆头形;C、D多主枝矮化开心形;X、Y轴数值为与主干距离。Figure 4. Distribution of branches (left) and panicles (right) in parts of canopies of two types of loquat treeA、B: Naturally round head tree with multiple main branches;C、D: Dwarf, open heart-shaped tree with multiple main branches;The X-axis and Y-axis value is the distance from the trunk.
图 4 两种树形冠层内不同部位枝梢(左图)和花穗(右图)分布情况A、B为多主枝自然圆头形;C、D多主枝矮化开心形;X、Y轴数值为与主干距离。Figure 4. Distribution of branches (left) and panicles (right) in parts of canopies of two types of loquat treeA、B: Naturally round head tree with multiple main branches;C、D: Dwarf, open heart-shaped tree with multiple main branches;The X-axis and Y-axis value is the distance from the trunk.多主枝矮化开心形有3层48个立方体小格,扣除F1层16个后,叶幕层可分成32个体积1 m3的小格(图4-B);叶幕层内无枝梢的小格2个,均在F3层,占6.25%;各小格内枝梢数1~11个·m−3、花穗数1~9个·m−3,其中1~4个·m−3枝梢、花穗的分别有15个和22个,占46.88%、68.75%,≥5个·m−3枝梢、花穗的有15个和7个,占46.88%、21.88%。49.65%、12.06%的枝梢分布在F2、F3层的P2区,16.31%、21.99%分布在F2、F3层的P1区,除F3层P2区平均枝梢数1个·m−3,F2层P1、P2区及F3层P1区分别达6、8个·m−3。
可见,两种树形均表现冠层外围的枝梢、花穗更多;冠层上层枝梢、花穗较多的,其对应下层的枝梢、花穗数较少,说明了冠层上层的枝梢、花穗数量会影响下层的枝梢、花穗数量,多主枝矮化开心形与多主枝自然圆头形相比,冠层内枝梢、花穗的分布更均匀。
2.3 枇杷两种树形冠层内不同部位枝梢质量差异
2.3.1 两种树形冠层内枝梢质量的水平分布差异
由表2可知,多主枝自然圆头形P1区的枝梢长度、枝梢粗度、叶片数的值最大,P3区最小,分别相差8.88 cm、0.92 mm、3片;多主枝矮化开心形P1区的枝梢长度、叶片数的值最大,P2区的枝梢粗度最大、枝梢长度最小。多主枝矮化开心形P1、P2区的枝梢长度、粗度、叶片数均分别较多主枝自然圆头形P1、P2、P3区的大,两种树形P1、P2、P3区间的枝角、节间长度差异不显著。两种树形均表现与主干水平距离越小,枝梢的生长量越大。
表 2 两种树形枝梢性状的水平分布特点Table 2. Horizontal distribution of branch traits on two types of loquat tree树形
Tree shape水平分区
Horizontal partitioning枝梢长度
Shoot length/cm枝梢粗度
Shoot thickness/ mm叶片数
Number of blades/leaf节间长度
Internode length/cm枝角
Branch/°多主枝自然圆头形
Naturally round head tree
with multiple main branchesP1 39.70±3.96bc 11.78±0.95ab 24.00±2.00bc 1.64±0.14a 30.24±1.53a P2 36.74±3.12c 11.22±0.85ab 21.58±1.98c 1.70±0.14a 38.88±3.65a P3 30.82±6.43d 10.86±0.86b 20.83±2.64c 1.53±0.11a 46.08±2.90a 多主枝矮化开心形
Dwarf, open heart-shaped
tree with multiple main branchesP1 47.78± 1.30a 12.38±0.63a 30.50±1.29a 1.58±0.03a 31.35±2.95a P2 42.60±5.35ab 12.51±0.92a 28.33±1.87ab 1.50±0.15a 38.21±5.92a 多主枝矮化开心形P3区无枝梢。
Multi-main branch dwarfing open-center P3 area without branch tip.2.3.2 两种树形冠层内枝梢质量的垂直分布质量
由表3可知,多主枝自然圆头形F4层的枝梢长度、枝梢粗度、叶片数的值均显著大于F3层,F2层最小,F4层分别较F2层大16.43 cm、2.43 mm、7片,节间长度以F4层最大、F3层最小,F2层枝角较F3、F4层增加21.98%、37.00%;多主枝矮化开心形以F3层的枝梢长度、枝梢粗度及叶片数的值最大,分别较F2层大5.74 cm、1.5 mm、3片,F2层的枝角较F3层大38.14%,两层间的节间长度无显著差异。两种树形均表现随冠层的高度增加,枝梢生长量显著增大,多主枝自然圆头形的最上层与最下层的枝梢长度、粗度、叶片数等的差异大于多主枝矮化开心形上下层的差异,两种树形顶层除节间长度有显著差异外,其余性状差异均不显著,而多主枝矮化开心形底层(F2)的枝梢长度、粗度、叶片数均大于多主枝自然圆头形的底层。
表 3 两种树形枝梢质量的垂直分布特点Table 3. Vertical distribution of branch traits on two types of loquat tree树形
Tree shape层级
Vertical hierarchy枝梢长度
Shoot length/cm枝梢粗度
Shoot thickness/mm叶片数
Number of blades/leaf节间长度
Internode length/cm枝角
Branch/°多主枝自然圆头形
Naturally round head tree
with multiple main branchesF4 48.49±5.03a 12.88±0.28a 26.3±1.32a 1.85±0.09a 31.27±3.96ab F3 33.13±3.51c 11.38±0.44b 21.68±2.27b 1.54±0.10b 35.12±3.85ab F2 32.06±3.69c 10.45±0.47c 19.96±1.15b 1.69±0.10ab 42.84±5.02a 多主枝矮化开心形
Dwarf, open heart-shaped tree
with multiple main branchesF3 46.44±6.74a 12.80±1.03a 30.20±2.83a 1.53±0.14b 28.97±4.02b F2 40.70±3.57b 11.36±0.27b 26.87±0.92a 1.51±0.12b 40.02±7.14ab 多主枝矮化开心形F4层无枝梢。
Multi-main branch dwarfed open-center F4 layer without branch tip.3. 讨论
3.1 不同树形对贵妃枇杷冠层内枝梢分布的影响
已有研究表明,奥林达夏橙自然圆头形枝梢多分布在树冠上层和外部,开心形抽生春梢总量最多,且可改善光照、扩大结果面积、改良枝组结构、提高果实品质[21];库尔勒香梨疏散分层形与开心形的骨干枝数量差异不明显,主要分布在树冠下层与中部,一年生枝总数差异明显,主要分布在冠层中层与外围[22];苹果开心形的枝量和叶面积指数小于小冠疏层形、疏散分层形、纺锤形,但4种树形的叶片在冠层内的主要分布区域不同[23],苹果三主枝疏散分层形郁闭大树改造成树冠成高干开心形,通过降低树高、增大干高,减少枝、叶量,可改善了树体的通风透光条件,实现产量增加和品质提高[24],但若枝梢量偏少,透光率偏高,冠层的光利用效率将降低[25]。本研究表明多主枝自然圆头形和多主枝矮化开心形均表现60%~70%的枝梢分布在与中心干水平距离100.1~200.0 cm区域,其次是0.0~100.0 cm区域,但0.0~100.0 cm区域多主枝矮化开心形的枝梢数较多主枝自然圆头形多,而100.1~200.0 cm区域以多主枝自然圆头形的枝梢数更多;垂直分布上,多主枝自然圆头形85.11%集中在树高100.1~300.0 cm,多主枝矮化开心形66.43%的枝梢集中分布在树高100.1~200.0 cm范围。枝梢数量对枇杷的单株产量影响密切[19],足够数量的枝梢是实现高产的保证,将冠层内单位体积的枝梢数<1个·m−3当作无效区,1~4个·m−3为低效区,≥5个·m−3为正常区,多主枝矮化开心形冠层内无效区和低效区的占比均少于多主枝自然圆头形,因此,仅就枝梢数量而言,多主枝矮化开心形的生产效率高于多主枝自然圆头形。
3.2 不同树形对贵妃枇杷枝梢生长质量的影响
苹果分层纺锤形冠层结构的主枝长、粗和产量随冠层高度的增加而减小[2],叶幕层厚度超过2m会影响苹果产量和品质[26];燕红桃树四挺身形树形冠内相对光照强度在20%以上,光照分布均匀,果实品质较优,是更适宜树形[26][27]。枇杷枝梢粗度、长度、叶片数等性状与开花结果的关系密切,适当长势的枝梢可实现大果、优质、丰产,但成年枇杷树要求有较高的光照条件[28],自然生长树冠的上部或外围枝梢的长势多数更粗壮[20],外围过多的枝梢易造成内膛或下部的荫蔽,枝叶质量 下降,且易落叶,造成树势衰弱甚至死亡[28]。本研究中,两种树形均表现树冠垂直高度上的枝梢质量的差异大于水平方向的差异,两种树形顶层间的枝梢长度、粗度、叶片数、枝角的差异均不显著,而多主枝自然圆头形的顶层与底层间的差异大于多主枝矮化开心形,多主枝矮化开心形的底层枝梢长度、粗度、叶片数均显著大于多主枝自然圆头形底层,说明上层枝梢对下层枝梢生长的遏制作用更明显,树冠的层次数越多,下层枝梢生长受到的影响越大。
3.3 贵妃枇杷适宜的枝梢密度
不同的树种均有适宜的高光效树形和留梢量,太行山区大果型板粟品种黑燕青、燕魁留枝量4~6个·m−2,中小型品种燕山早丰、紫珀留枝量6~8个·m−2,产量高,树势稳,质量好[29];燕红桃树每株留918个枝的果实品质及单株产量最高[30]。枇杷是常绿果树,叶片大且相互间遮蔽严重,所以自然圆头形的树冠内膛枝普遍因外围枝叶的遮挡而长势细弱。贵妃枇杷的新梢抽发能力较强[31],若不加控制,易造成枝梢数量偏多,影响枝梢的质量。本试验中,多主枝自然圆头形和多主枝矮化开心形外层枝梢数5~6个·m−3,次高层和次外层枝梢数也能达到4~6个·m−3,但多主枝自然圆头形F2层枝梢数量明显减少、质量降低、花穗数少或无。由此认为,要培养高光效的枇杷树形,贵妃枇杷外围和次外围枝梢数5~6个·m−3为宜,单位投影面积枝梢数10~12个·m−2,叶幕层厚度宜小于2 m,冠幅小于5 m。
此外,在枇杷生产上,疏花疏果套袋、枝梢管理等人工成本等占总成本的60%以上,近年来随人工工资的增长,成本占比有增大趋势。田间操作时,枝梢、花穗着生高度超过2 m,人工无法直接操作,需要借助钩子或爬树操作,管理效率显著降低,攀爬等操作还增大了安全风险。试验中,多主枝自然圆头形的树冠生长量、枝梢数、花穗数均较多主枝矮化开心形显著增多,属单株产量更高的树形,但有60%左右的枝梢和花穗分布在树高2~4 m的位置,而多主枝矮化开心形的60%多的枝梢和花穗分布在树高1~2 m的位置,更方便管理操作。
4. 结论
多主枝自然圆头形较多主枝矮化开心形冠层的树体生长量更大、枝梢数量和花穗数更多,两种树形的枝梢主要分布在次高层和次外层,多主枝矮化开心形冠层内的枝梢分布更均匀,且树冠内膛无枝梢或枝梢量少的低效或无效空间占比更少,为更高效树形。
-
表 1 滇杨样品采集信息
Table 1 Specimen collection of P. yunnanensis
编号
Code性别
Sex of the individual采集地
Location1-10 雄性(♂) 香格里拉 11-20 雄性(♂) 大理 21-25 雄性(♂) 禄劝 25-30 雄性(♂) 昆明 1-15 雌性(♀) 香格里拉 16-28 雌性(♀) 大理 29-30 雌性(♀) 禄劝 表 2 SSR扩增引物信息
Table 2 Primers for SSR amplification
引物名称
Locus name引物序列
Primer sequence(5′-3′)退火温度
Ta(annealing temperature)/℃参考文献
ReferenceBmsat95 F:ATTGTAACCGATTTGAGAGA
R:ATTCGCACAATAAGTTCACT54.0 NAGARAJA[19] Bmsat153 F:TGCTGTCGTCTGCTTCCTAA
R:CACGGTGCTGACTGTTGTTT60.0 NAGARAJA[19] Bmsat155 F:AGGGATGATGGGTAAAGAGC
R:GCAGTAGGCATTTGGAAGGAG60.0 NAGARAJA [19] Bmsat156 F:CTCCTTATCCATCCGTTT
R:CTCTCGGATCATAGATACG56.0 NAGARAJA[19] Bmsat159 F:ATCTGGTGCTCAAAAACGGA
R:CGGAACCAAACAAGAACGAT58.0 NAGARAJA[19] Bmsat208 F:ACATGAAATGGGCAAACGACG
R:GCTCATATTTGCTTGCCGGTT55.8 NAGARAJA[19] SSR-8 F:TGCATATCGTCCAGGGTGTTTTC
R:CCCAGCCAGGGTCTTGTTTC64.0 SHAN[20] BPCA90 F:CCTAGCCTTCATTCTCATTCAGC
R:GGTTGCTAGTCAGCTTCTTACC58.4 PAKULL B[21] BPTTG60 F:CAAGAACTCAGACATGATCAGATC
R:CTTTGCACGTTAATAAGGAGACTG56.9 PAKULL B[21] BPTGG82 F:CTTGAAGAGCGAAAACTCAGCAG
R:CTCTAAATCCAAGGTTGGTTACC58.4 PAKULL B[21] BPTG50 F:CTAGCTGTCGAACGTAATTGGCAC
R:CTTGCACGAGCCTCCATCACTC61.8 PAKULL B[21] BPTC66 F:GGCCGTGATTCTCATCATGATG
R:CTTCTTCATCAACAACTGCGTCC58.4 PAKULL B[21] CADEx2/Intr2 F:CAAGGTTATCAGCTGTGG
R:ATATTGTGTGCGTGTTCG54.0 PAKULL B[22] HIAGA7 F:ACAAGCAGTAATGATGAGGA
R:TCCAAGTCTCTCAATTAGGAA56.0 JAKSE[23] 35 F:GAGGCCGACAGGATCGTAC
R:TACGACGTACTCCGGTGGTTTT62.0 CHEN[24] -
[1] 王德新, 张晏, 段安安, 等. 滇杨优树无性系物候期观测 [J]. 西南林学院学报, 2009, 29(6):20−23,27. WANG D X, ZHANG Y, DUAN A A, et al. Observation on phenological phase of Populus yunnanensis plus tree clones [J]. Journal of Southwest Forestry University, 2009, 29(6): 20−23,27.(in Chinese)
[2] CHEN L H, ZHANG S, ZHAO H X, et al. Sex-related adaptive responses to interaction of drought and salinity in Populus yunnanensis [J]. Plant, Cell & Environment, 2010, 33(10): 1767−1778.
[3] LI L, ZHANG Y B, LUO J X, et al. Sex-specific responses of Populus yunnanensis exposed to elevated CO2 and salinity [J]. Physiologia Plantarum, 2013, 147(4): 477−488. DOI: 10.1111/j.1399-3054.2012.01676.x
[4] LI X, YANG Y Q, SUN X D, et al. Comparative physiological and proteomic analyses of poplar (Populus yunnanensis) plantlets exposed to high temperature and drought [J]. PLoS One, 2014, 9(9): e107605. DOI: 10.1371/journal.pone.0107605
[5] LIAO L Q, LIU J, DAI Y X, et al. Development and application of SCAR markers for sex identification in the dioecious species Ginkgo biloba L. [J]. Euphytica, 2009, 169(1): 49−55. DOI: 10.1007/s10681-009-9913-8
[6] 李仕金, 辛培尧, 郭鸿彦, 等. 大麻雄性相关RAPD和SCAR标记的研究 [J]. 广东农业科学, 2012, 39(24):151−154. DOI: 10.3969/j.issn.1004-874X.2012.24.047 LI S J, XIN P Y, GUO H Y, et al. Study of male-specific RAPD and SCAR marker in Cannabis sativa L [J]. Guangdong Agricultural Sciences, 2012, 39(24): 151−154.(in Chinese) DOI: 10.3969/j.issn.1004-874X.2012.24.047
[7] JIANG C X, SINK K C. RAPD and SCAR markers linked to the sex expression locus M in asparagus [J]. Euphytica, 1997, 94(3): 329−333. DOI: 10.1023/A:1002958007407
[8] MIDGLEY J J. Causes of secondary sexual differences in plants—Evidence from extreme leaf dimorphism in Leucadendron (Proteaceae) [J]. South African Journal of Botany, 2010, 76(3): 588−592. DOI: 10.1016/j.sajb.2010.05.001
[9] ZIETKIEWICZ E, RAFALSKI A, LABUDA D. Genome fingerprinting by simple sequence repeat (SSR)-anchored polymerase chain reaction amplification [J]. Genomics, 1994, 20(2): 176−183. DOI: 10.1006/geno.1994.1151
[10] SALIH KAFKAS S K, SELIM CETINER G D, PERL-TREVES R, et al. Development of sex-associated RAPD markers in wildPistaciaspecies [J]. The Journal of Horticultural Science and Biotechnology, 2001, 76(2): 242−246. DOI: 10.1080/14620316.2001.11511358
[11] XU W J, WANG B W, CUI K M. RAPD and SCAR markers linked to sex determination in Eucommia ulmoides Oliv. [J]. Euphytica, 2004, 136(3): 233−238. DOI: 10.1023/B:EUPH.0000032741.99885.c4
[12] GAO W J, LI R L, LI S F, et al. Identification of two markers linked to the sex locus in dioecious Asparagus officinalis plants [J]. Russian Journal of Plant Physiology, 2007, 54(6): 816−821. DOI: 10.1134/S1021443707060143
[13] 刘嘉艺, 岳俊阳, 刘永胜. 基于毛花猕猴桃基因组的性别相关SSR分子标记的开发 [J]. 合肥工业大学学报(自然科学版), 2022, 45(8):1135−1138,1146. LIU J Y, YUE J Y, LIU Y S. Development of sex-related SSR molecular markers based on the genome of Actinidia eriantha [J]. Journal of Hefei University of Technology (Natural Science), 2022, 45(8): 1135−1138,1146.(in Chinese)
[14] 黄海燕, 杜红岩, 乌云塔娜, 等. 基于杜仲转录组序列的SSR分子标记的开发 [J]. 林业科学, 2013, 49(5):176−181. DOI: 10.11707/j.1001-7488.20130523 HUANG H Y, DU H Y, WU Y, et al. Development of SSR molecular markers based on transcriptome sequencing of Eucommia ulmoides [J]. Scientia Silvae Sinicae, 2013, 49(5): 176−181.(in Chinese) DOI: 10.11707/j.1001-7488.20130523
[15] 马霞霞. 基于BSA分析的山葡萄性别位点定位研究[D]. 沈阳: 沈阳农业大学, 2018. MA X X. Mapping of sex locus based on BSA analysis in Vitis amurensis[D]. Shenyang: Shenyang Agricultural University, 2018. (in Chinese)
[16] 王洪梅, 李春明, 白卉, 等. 一种鉴定山杨性别的SSR分子标记的筛选 [J]. 东北林业大学学报, 2017, 45(10):17−19,29. DOI: 10.3969/j.issn.1000-5382.2017.10.005 WANG H M, LI C M, BAI H, et al. Screening SSR markers for sex identification in Populus davidiana dode [J]. Journal of Northeast Forestry University, 2017, 45(10): 17−19,29.(in Chinese) DOI: 10.3969/j.issn.1000-5382.2017.10.005
[17] 雷瀚, 刘成, 唐军荣, 等. 滇杨性别相关的SRAP分子标记 [J]. 中南林业科技大学学报, 2020, 40(8):139−146. LEI H, LIU C, TANG J R, et al. SRAP molecular markers related to sexuality of Populus yunnanensis Dode [J]. Journal of Central South University of Forestry & Technology, 2020, 40(8): 139−146.(in Chinese)
[18] 陈学军, 周坤华, 宗洪霞, 等. 中国灌木辣椒种质遗传多样性的SRAP和SSR分析 [J]. 西北植物学报, 2012, 32(11):2201−2205. DOI: 10.3969/j.issn.1000-4025.2012.11.009 CHEN X J, ZHOU K H, ZONG H X, et al. Genetic diversity of Capsicum frutescens in China as revealed by SRAP and SSR markers [J]. Acta Botanica Boreali-Occidentalia Sinica, 2012, 32(11): 2201−2205.(in Chinese) DOI: 10.3969/j.issn.1000-4025.2012.11.009
[19] NAGARAJA G M, MAHESH G, SATISH V, et al. Genetic mapping of Z chromosome and identification of W chromosome-specific markers in the silkworm, Bombyx mori [J]. Heredity, 2005, 95(2): 148−157. DOI: 10.1038/sj.hdy.6800700
[20] SHAN T F, PANG S J. Sex-linked microsatellite marker detected in the female gametophytes of Undaria pinnatifida (Phaeophyta) [J]. Phycological Research, 2010, 58(3): 171−176. DOI: 10.1111/j.1440-1835.2010.00575.x
[21] PAKULL B, GROPPE K, MECUCCI F, et al. Genetic mapping of linkage group XIX and identification of sex-linked SSR markers in a Populus tremula × Populus tremuloides cross [J]. Canadian Journal of Forest Research, 2011, 41(2): 245−253. DOI: 10.1139/X10-206
[22] PAKULL B, GROPPE K, MEYER M, et al. Genetic linkage mapping in aspen (Populus tremula L. and Populus tremuloides Michx. ) [J]. Tree Genetics & Genomes, 2009, 5(3): 505−515.
[23] JAKSE J, STAJNER N, KOZJAK P, et al. Trinucleotide microsatellite repeat is tightly linked to male sex in hop (Humulus lupulus L. ) [J]. Molecular Breeding, 2008, 21(2): 139−148. DOI: 10.1007/s11032-007-9114-x
[24] CHEN S L, JI X S, SHAO C W, et al. Induction of mitogynogenetic diploids and identification of WW super-female using sex-specific SSR markers in half-smooth tongue sole (Cynoglossus semilaevis) [J]. Marine Biotechnology, 2012, 14(1): 120−128. DOI: 10.1007/s10126-011-9395-2
[25] CHARLESWORTH D. Plant sex chromosome evolution [J]. Journal of Experimental Botany, 2013, 64(2): 405−420. DOI: 10.1093/jxb/ers322
[26] BOUALEM A, TROADEC C, CAMPS C, et al. A cucurbit androecy gene reveals how unisexual flowers develop and dioecy emerges [J]. Science, 2015, 350(6261): 688−691. DOI: 10.1126/science.aac8370
[27] RENNER S S. Pathways for making unisexual flowers and unisexual plants: Moving beyond the “two mutations linked on one chromosome” model [J]. American Journal of Botany, 2016, 103(4): 587−589. DOI: 10.3732/ajb.1600029
[28] CHARLESWORTH D. Plant sex determination and sex chromosomes [J]. Heredity, 2002, 88(2): 94−101. DOI: 10.1038/sj.hdy.6800016
[29] 董莉娜, 苏雪, 孙坤, 等. DNA分子标记在雌雄异株植物性别鉴定中的应用 [J]. 广西植物, 2006, 26(1):63−68. DOI: 10.3969/j.issn.1000-3142.2006.01.015 DONG L N, SU X, SUN K, et al. Applications of DNA molecular markers on sex identification of dioecious plants [J]. Guihaia, 2006, 26(1): 63−68.(in Chinese) DOI: 10.3969/j.issn.1000-3142.2006.01.015
[30] PAKULL B, KERSTEN B, LÜNEBURG J, et al. A simple PCR-based marker to determine sex in aspen [J]. Plant Biology, 2015, 17(1): 256−261. DOI: 10.1111/plb.12217
[31] 任朝兴, 黄建昌, 肖艳, 等. 番木瓜雄性性别的RAPD和SCAR标记 [J]. 果树学报, 2007, 24(1):72−75. REN C X, HUANG J C, XIAO Y, et al. RAPD and SCAR molecular markers for male trait in Caric papaya [J]. Journal of Fruit Science, 2007, 24(1): 72−75.(in Chinese)
[32] 唐美玲, 孔瑾, 许雪峰, 等. 山葡萄性别相关AFLP标记筛选及SCAR标记转化 [J]. 园艺学报, 2008, 35(2):195−200. DOI: 10.3321/j.issn:0513-353X.2008.02.007 TANG M L, KONG J, XU X F, et al. Screening of the AFLP markers associated to the sex locus of Vitis amurensis rupr. and its conversion to SCAR marker [J]. Acta Horticulturae Sinica, 2008, 35(2): 195−200.(in Chinese) DOI: 10.3321/j.issn:0513-353X.2008.02.007
[33] 董娜, 唐晓姗, 唐琳. 毛叶山桐子性别相关ISSR分子标记的筛选与分析 [J]. 四川大学学报(自然科学版), 2016, 53(2):465−470. DONG N, TANG X S, TANG L. Screening and analysis of sex-related ISSR molecular marker in Idesia polycarpa Maxim. var. vestita Diels [J]. Journal of Sichuan University (Natural Science Edition), 2016, 53(2): 465−470.(in Chinese)
[34] 邓传良, 任映雪, 张卫丽, 等. 葎草性别相关SRAP分子标记的鉴定 [J]. 植物研究, 2014, 34(6):798−802. DENG C L, REN Y X, ZHANG W L, et al. Identification of sex related SRAP molecular marker in Humulus scandens [J]. Bulletin of Botanical Research, 2014, 34(6): 798−802.(in Chinese)
[35] 齐凤慧, 孙宏冉, 詹亚光. EST-SSR标记在水曲柳雌雄鉴定中的应用 [J]. 西北植物学报, 2015, 35(3):472−479. DOI: 10.7606/j.issn.1000-4025.2015.03.0472 QI F H, SUN H R, ZHAN Y G. Application of EST-SSR markers in the sex identification of Fraxinus mandshurica rupr [J]. Acta Botanica Boreali-Occidentalia Sinica, 2015, 35(3): 472−479.(in Chinese) DOI: 10.7606/j.issn.1000-4025.2015.03.0472
[36] HOU W W, FAN J F, ZHOU F M, et al. RAPD markers related to sex locus in Populus tomentosa [J]. Frontiers of Forestry in China, 2009, 4(2): 223−226. DOI: 10.1007/s11461-009-0037-z
[37] 张洪福. 对PCR引物设计问题的研究[D]. 济南: 山东大学, 2005. ZHANG H F. Study on PCR Primer Design[D]. Jinan: Shandong University, 2005. (in Chinese)
[38] 许玉兰, 康向阳, 张瑞丽, 等. 木本植物中EST-SSR的通用性及其多态性研究 [J]. 西南林业大学学报, 2012, 32(4):94−99. DOI: 10.3969/j.issn.2095-1914.2012.04.020 XU Y L, KANG X Y, ZHANG R L, et al. Study on versatility and polymorphism of EST-SSR application to woody plants [J]. Journal of Southwest Forestry University, 2012, 32(4): 94−99.(in Chinese) DOI: 10.3969/j.issn.2095-1914.2012.04.020
[39] 徐杨, 邓丽丽, 周丽, 等. 云南松EST-SSR引物在其近缘种中通用性的研究 [J]. 西南林业大学学报, 2016, 36(1):16−20. XU Y, DENG L L, ZHOU L, et al. The transferability analysis of microsatellite markers from expressed sequence tags of Pinus yunnanensis to its close related species [J]. Journal of Southwest Forestry University, 2016, 36(1): 16−20.(in Chinese)
[40] 杨彦伶, 张亚东, 张新叶. 杨树SSR标记在柳树中的通用性分析 [J]. 分子植物育种, 2008, 6(6):1134−1138. DOI: 10.3969/j.issn.1672-416X.2008.06.018 YANG Y L, ZHANG Y D, ZHANG X Y. Transferability analysis of Populus SSR markers in Salix [J]. Molecular Plant Breeding, 2008, 6(6): 1134−1138.(in Chinese) DOI: 10.3969/j.issn.1672-416X.2008.06.018
[41] 盛文涛. 芦笋性别决定基因分子标记的筛选与开发[D]. 南昌: 南昌大学, 2010 SHENG W T. Identification and development of molecular makers associated with sex determining gene in Asparagus[D]. Nanchang: Nanchang University, 2010. (in Chinese)





 下载:
下载: