Somatic Incompatibility and Genetic Differences among Strains of Ganoderma sinense
-
摘要:目的 评价不同紫芝(Ganoderma sinense)菌株间体细胞不亲和反应与遗传差异的关系,为应用体细胞不亲和性评价紫芝菌株间的遗传差异提供依据。方法 以7个不同交配基因型的紫芝单核体为亲本,应用单向或者双向核迁移技术构建双核体菌株;通过在PDA培养基配对检测双核体菌株间的体细胞不亲和性,并采用ISSR、RAPD和SRAP 3种分子标记综合分析双核体菌株间的遗传差异。结果 构建了5类遗传背景清晰的不同双核体菌株11个,它们之间的体细胞不亲性反应分为亲和、不亲和,其中不亲和反应出现隔离区、隔离区带线状和类似墙式结构的3种类型;3种分子标记综合分析显示,11个菌株间的遗传相似系数0.29~0.97,UPMGA聚类树状图能很好地展示11个双核体菌株间的遗传差异,并与亲本来源相一致。结论 紫芝菌株间的体细胞不亲性反应主要受细胞核的影响,而细胞质的影响极小,并且紫芝菌株间的体细胞不亲性反应类型与菌株间的遗传差异相对应,在以后的紫芝种质资源遗传差异评价中,可应用操作简便的体细胞不亲和性进行初步分析。Abstract:Objective Somatic incompatibility (SI) and genetic differences among Ganoderma sinense strains were studied.Method DikaryonG. sinense strains were generated from 7 monokaryon parents by uni- or bi-directional nuclear migration. On a PDA medium, SI between the dikaryon strains was tested, and genetic differentiations examined using ISSR, RAPD, and SRAP molecular markers.Result Eleven dikaron strains of 5 distinctive genetic types showing a gap, a gap with line, or a wall-like SI were obtained. The combined genetic similarity coefficients of the ISSR, RAPD, and SRAP molecular markers on the strains ranged from 0.29 to 0.97. The UPMGA clustering of the strains corresponded to that of the parents.Conclusion The SI among the G. sinense strains were mainly associated with the nucleus rather than the cytoplasm. Since the SI types largely paralleled the genetic differences of the dikaron strains, SI determination could be conveniently applied to preliminarily study the genetics of a G. sinense strain.
-
Keywords:
- antagonism /
- genetic relationship /
- molecular marker
-
0. 引言
【研究意义】紫芝(Ganoderma sinense Zhao,Xu et Zhang)是我国著名的药用菌,具有抗肿瘤、提高免疫力等功效,已被收录《中国药典》中,作为法定的中药材[1]。紫芝在我国分布较广,其遗传资源较丰富[2],然而众多学者对紫芝的研究主要集中在其活性物质[3−5]、药用功能[6−8]方面,对其遗传多样性的研究甚少。目前生产栽培的紫芝品种较为单一,菌种主要通过引种或者对本地品种进行改良等方式获得,这导致了生产所用菌种的生物学性状不突出以及遗传背景混乱等问题。通过体细胞亲和性试验与分子标记技术相结合,从传统和现代两方面进行分析,可进一步揭示其遗传差异的规律所在,为选育更高品质的新菌株提供有力的理论支持。【前人研究进展】体细胞不亲和性(Somatic incompatibility, SI)是丝状真菌同一物种内识别异己、保持独立个体的一种系统,它可以使营养菌丝体在遗传、生理和生态等各方面保持自己的个性[9],因此可应用于研究个体差异和群体结构[10]。在高等担子菌中,SI主要出现在双核菌丝阶段,遗传差异背景较大的个体在菌丝交界区会形成明显的分界线,这一现象被称之为拮抗反应,拮抗反应是体细胞非亲和性的具体表现[11]。人们利用这一现象可以简单快速地初步判别菌株的亲缘关系,因此SI在鉴别同种异名菌株以及揭示遗传多样性方面也具有重要意义及地位。在真菌中,拮抗反应具有丰富的多态性,在木耳菌株中,拮抗反应出现隆起型、沟型及隔离型等3种类型,在这几种类型中又会出现不亲和程度和色素有无的差异[12],香菇(Lentinula edodes)[13]及其他的担子菌也会出现类似的拮抗反应。随着分子生物学的发展,DNA分子标记技术给食用菌遗传科学提供了新的可能。简单序列重复区间(Inter simple sequence repeats, ISSR)、 随机扩增多态性DNA(random amplified polymorphic DNA, RAPD)和相关序列扩增多态性(sequence related amplified polymorphism, SRAP)已广泛应用于真菌的亲缘关系分析,3种分子标记的设计原理不同,各有优缺点,将3种分子标记综合起来分析,可利用不同分子标记间的优势互补,获得更为可靠的菌株遗传多样性分析结果。刘靖宇等[14]利用ISSR、RAPD和SRAP 等3种分子标记综合分析26个香菇菌株,其结果显示,3种分子标记综合分析的结果比单一分子标记分析的结果可以更准确地反映供试菌株间的亲缘关系。【本研究切入点】在真菌中,拮抗是SI的具体体现,目前作为我国食用菌DUS测试指南必测的指标之一[15]。虽然拮抗试验可以快速鉴定菌株的遗传差异,但对其观察的结果也受到主观因素的影响。利用分子生物学手段,将传统方法与分子标记相结合,更有利于提升结果的准确性。同时这些拮抗类型与菌株的亲缘关系如何还较为模糊,如出现隆起型和出现隔离型的,其遗传差异哪个更大,受何种因素影响等等问题,还有待进一步研究。阐明SI反应类型和强度与菌株间遗传差异的关系,才能更好地应用SI测试快速评价个体间的遗传差异。【拟解决的关键问题】本研究利用紫芝的单核体菌株,通过配对与核迁移技术,构建遗传背景清晰的紫芝双核菌株,从SI和分子标记两方面分析紫芝的遗传差异,阐明SI反应类型与遗传差异的关系,有利于全面揭示紫芝的遗传多样性,并为其评价提供技术依据。
1. 材料与方法
1.1 供试菌株
在前期对紫芝交配型研究的基础上[2],选择G.s0004-11、G.s0007-31、G.s0011-3、G.s0011-16、G.s0012-26、G.s0012-28和G.s0014-36等7个单核体菌株为材料。
1.2 异核体构建
选用不同交配型的单核体在含PDA培养基的90 mm平皿上进行配对,两菌块相距1 cm,置于25 ℃下培养,参照刘靖宇等[16]的方法,运用单向与双向核迁移技术,在远离两菌块接触的一边取样,获得不同类型的双核体。
1.3 体细胞不亲和性测试
以构建的双核体为研究对象,同种类型内的双核体之间进行测试,每一种类型选择3组进行测试。测试菌株在PDA培养基活化2次后,取0.5 cm2大小的菌块,接种于含PDA培养基的90 mm平皿,两菌块之间相距1 cm,置于25 ℃下培养20 d,观察菌丝接触区域与菌落特征,每组测试重复3次。
1.4 菌丝培养与DNA提取
在无菌操作条件下,将测试菌株分别接种于贴有玻璃纸的PDA培养基平皿,25 ℃培养,待菌丝长满平皿,刮下菌丝置−20 ℃冰箱保存备用,采用CTAB法提取菌丝DNA。
1.5 ISSR、RAPD和SRAP分子检测
应用ISSR、RAPD和SRAP分子标记对紫芝双核菌株进行检测,在引物筛选的基础上,选择稳定性好、具有较大差异的3个ISSR引物、3个RAPD引物和4组SRAP引物进行PCR扩增,使用引物见表1,PCR反应体系与扩增程序参考刘靖宇等[14]的方法。
表 1 引物序列Table 1. Sequences of primers for molecular markers分子标记
Molecular marker引物
Primer序列(5′-3′)
Sequences分子标记
Molecular marker引物
Primer序列(5′-3′)
SequencesISSR ISSR6 DHB (CGA)5 SRAP ME4 TGAGTCCAAACCGGACC ISSR ISSR17 (TG)8RC SRAP ME5 TGAGTCCAAACCGGAAG ISSR ISSR18 VHV (GT)8 SRAP ME6 TGAGTCCAAACCGGTAG RAPD S17 AGGGAACGAG SRAP EM8 GACTGCGTACGAATTAGC RAPD S18 CCACAGCAGT SRAP EM13 GACTGCGTACGAATTGGT RAPD S367 AGCGAGCAAG SRAP EM14 GACTGCGTACGAATTCAG SRAP ME3 TGAGTCCAAACCGGAAT SRAP EM17 GACTGCGTACGAATTCCA ISSR引物中的单字母简写代表多碱基混合位点。位置:D= (A, G, T), H= (A, C, T), B= (C, G, T),R= (A, G),V= (A, C, G)。
Single letter abbreviations of ISSR primers for mixed base. Positions: D= (A, G, T), H= (A, C, T), B= (C, G, T), R= (A, G), V= (A, C, G).1.6 数据分析
将ISSR、RAPD和SRAP扩增获得的图谱用Bio-RAD凝胶成像系统进行照相,对条带进行分析,无ISSR、RAPD及SRAP带谱计为0,有ISSR、RAPD及SRAP带谱计为1,构建相应的初始数据矩阵,用NTSYSpc2.1 专业版软件计算遗传相关系数,采用平均连锁法UPGMA 进行聚类分析,得出聚类图谱。
2. 结果与分析
2.1 体细胞不亲和性测试菌株构建
根据紫芝单核体的交配型,选择7个单核体菌株作为构建双核体的亲本,其中G.s0011-3与G.s0011-16来自同一亲本G.s0011,G.s0012-26与G.s0012-28来自同一亲本G.s0012,使用不同交配型的单核体进行配对,成功构建了5类不同的双核菌株11个(表2),Ⅰ类为细胞核相同而细胞质不同,即同核异质体,如Sh3与Sh4;Ⅱ类是细胞质相同,含一个相同的核,另一个核不同,如以G.s0007-31为受体构建的双核体有Sh2、Sh12和Sh14;Ⅲ类为细胞质相同,细胞核均不同,如Sh3与Sh13;Ⅳ类是细胞质不同,一个核相同,另一个核不同,如含相同核G.s0011-16,另一个核与细胞质不同的双核体有Sh2、Sh3和Sh10;Ⅴ类为细胞核与细胞质均不同,如Sh2与Sh21。这些双核菌株的构建,可使我们很好地掌握其遗传背景,为后续的研究分析提供可靠的依据。
表 2 测试菌株信息Table 2. Information on tested strains菌株
Strain亲本和交配型
Parents and mating types菌株
Strain亲本和交配型
Parent and mating typeSh2 G.s0007-31FP A1B7、G.s0011-16 A3B3 Sh13 G.s0007-31 A1B7、G.s0011-3 FP A2B2 Sh3 G.s0011-16 FP A3B3、G.s0012-28 A5B5 Sh14 G.s0007-31 FP A1B7、G.s0012-26 A4B4 Sh4 G.s0011-16 A3B3、G.s0012-28 FP A5B5 Sh15 G.s0007-31 A1B7、G.s0012-26 FP A4B4 Sh9 G.s0004-11 A1B1、G.s0011-16 FP A3B3 Sh21 G.s0011-3 A2B2、G.s0012-28 FP A5B5 Sh10 G.s0004-11 FP A1B1、G.s0011-16 A3B3 Sh24 G.s0004-11 A1B1、G.s0014-36 FP A7B7 Sh12 G.s0007-31 FP A1B7、G.s0011-3 A2B2 FP代表母本。
FP:female parent.2.2 体细胞不亲和性分析
对构建的5类双核体进行SI测试,以同一双核体的两个菌块接种于同一平皿,其菌丝交接处的特征为参照,来判别其他双核体之间SI反应的依据。菌块之间的配对反应见图1。从图中可以看出,自身两菌块配对的菌丝在交接处相互融合,其菌落特征或分泌的色素完全一致,但一些在两菌块相对位置的菌丝较难融合,出现小隔离区(如Sh3与Sh3)。Ⅰ类双核体中,随机选择Sh3与Sh4、Sh12与Sh13、Sh14与Sh15进行配对,除Sh3与Sh4分泌的色素量存在差异外,这3组同核异质体的菌落显差较小,在离两菌块较远的菌丝之间可以相互交融,即不产生拮抗。
![]() 图 1 紫芝双核体在PDA培养基上的SI反应F:正面;B:背面。异核体的配对类别分为,Ⅰ:同核异质体;Ⅱ:细胞质和一个核相同,另一个核不同;Ⅲ:细胞质相同,细胞核不同;Ⅳ:一个核相同,另一个核与细胞质都不同;Ⅴ:细胞质和细胞核均不同。CK代表对照组。Figure 1. SI reactions of heterokaryotic G. sinense colonies on PDAF: front; B: back. The five pairing types of heterokaryons, Ⅰ: same dikaryon in different FP; Ⅱ: one same monokaryon with one different monokaryon in the same FP; Ⅲ: different dikaryon in the same FP; Ⅳ: one same monokaryon with one different monokaryon in different FP; Ⅴ: different dikaryon in different FP. Control check(CK).
图 1 紫芝双核体在PDA培养基上的SI反应F:正面;B:背面。异核体的配对类别分为,Ⅰ:同核异质体;Ⅱ:细胞质和一个核相同,另一个核不同;Ⅲ:细胞质相同,细胞核不同;Ⅳ:一个核相同,另一个核与细胞质都不同;Ⅴ:细胞质和细胞核均不同。CK代表对照组。Figure 1. SI reactions of heterokaryotic G. sinense colonies on PDAF: front; B: back. The five pairing types of heterokaryons, Ⅰ: same dikaryon in different FP; Ⅱ: one same monokaryon with one different monokaryon in the same FP; Ⅲ: different dikaryon in the same FP; Ⅳ: one same monokaryon with one different monokaryon in different FP; Ⅴ: different dikaryon in different FP. Control check(CK).在Ⅱ、Ⅲ、Ⅳ和Ⅴ的配对中,两菌块之间至少含有一个不同的核,其菌落形态存在明显差异,大部分配对的两菌丝交接处出现明显的拮抗反应,拮抗反应类型主要为两类,一类是隔离型,大部分配对反应属于这一类,除Sh4与Sh15配对在隔离处出现少量色素外,其他配对未观察到;另一类是在菌丝相对处除有隔离现象外还出现线型,如Sh3与Sh9的配对(图1的Sh3×Sh9)、Sh3与Sh10的配对。此外,Sh3与Sh2的配对虽然未出现隔离,但两者的菌落差异大,在Sh3一侧的菌丝形成一道类似墙结构(图1的Sh3×Sh2)。
根据菌丝交接处隔离的宽度,特别是离两菌块相对位置2 cm,两菌丝明显分界的区域大小,将拮抗反应强度分为4个等级(表3),第1级是菌丝交接处中间有明显隔离,但边缘隔离较弱,如Sh2与Sh12的配对(图1中Sh2×Sh12),第2至第4级在菌丝交接处均出现隔离,第4级是最强的拮抗反应类型,如Sh14与Sh24的配对(图1中Sh14×Sh24)。
表 3 测试菌株的体细胞不和性与遗传关系Table 3. Relationships between SI and genetic differences among strains异核体类别
Type of heterokaryon配对
Pairing拮抗信息
Information of antagonism遗传相似系数
Genetic similarity coefficientⅠ 同核异质体
Same dikaryon in different FPSh3×Sh4 - 0.97 Sh12×Sh13 - 0.97 Sh14×Sh15 - 0.95 Ⅱ 细胞质和一个核相同,另一个核不同
one same monokaryon with one different monokaryon in the same FPSh2×Sh14 G+ 0.66 Sh2×Sh12 G+ 0.74 Sh3×Sh9 GL++ 0.66 Ⅲ 细胞质相同,细胞核不同
Different dikaryon in the same FPSh4×Sh15 G+++ 0.46 Sh3×Sh13 G+++ 0.63 Sh9×Sh13 G++ 0.57 Ⅳ 一个核相同,另一个核与细胞质都不同
one same monokaryon with one different monokaryon in different FPSh3×Sh10 GL++ 0.69 Sh2×Sh15 G+ 0.66 Sh3×Sh2 W-l S 0.54 Ⅴ 细胞质和细胞核均不同
Different dikaryon in different FPSh2×Sh21 G++ 0.66 Sh3×Sh14 G+++ 0.49 Sh14×Sh24 G++++ 0.29 FP代表母本;SI反应分为(1)无拮抗-,(2)隔离型G,和(3)隔离型带线状GL和(4)菌丝墙式结构W-l S;“+”表示弱拮抗,“++”中等拮抗,“+++”强拮抗,“++++”非常强拮抗。
FP: female parent; 4 types of SI including(1)-: no antagonism; (2)G: gap; (3)GL: gap with line; and(4) W-1 S: hyphal wall-like structure; +: slight reaction; ++: moderate reaction; +++: strong reaction;++++: extremely strong reaction.2.3 测试菌株ISSR、RAPD和SRAP综合分析
在引物筛选的基础上,选择3个ISSR引物ISSR6、ISSR17和ISSR18,3个RAPD引物S17、S18和S367,4组SRAP引物Me5/Em13、Me3/Em17、Me4/Em8和Me6/Em14对构建的11个双核体进行PCR扩增。3个ISSR引物共扩增出25个条带,多态性条带13个,平均多态性比例为52.0%;3个RAPD引物共扩增出21个条带,多态性条带11个,平均多态性比例为52.4%;4组SRAP引物共扩增出23个条带,多态性条带11个,平均多态性比例为47.8%。
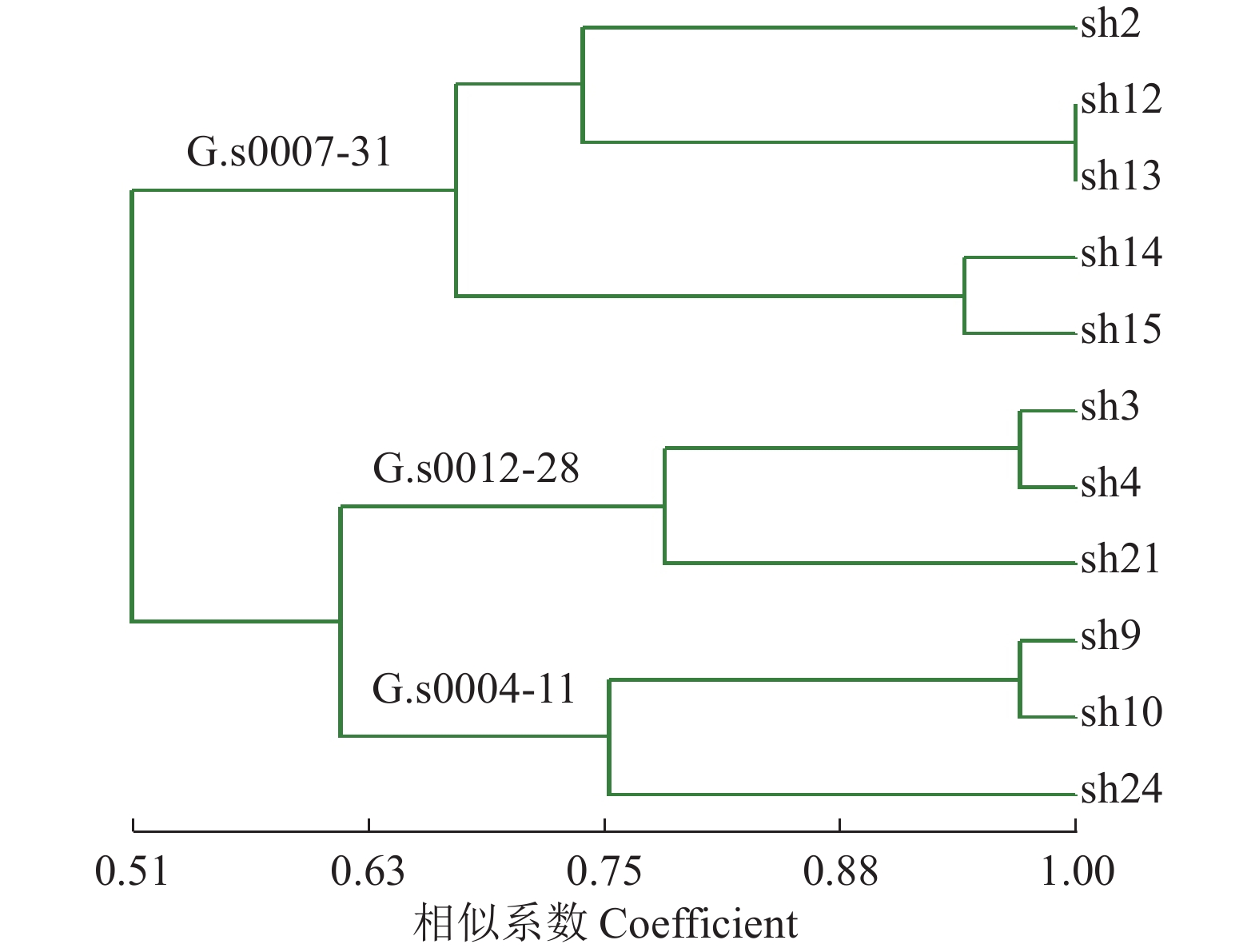
将3种分子标记引物扩增的多态性数据合并,构建11个测试菌株的UPMGA聚类树状图(图2),聚类结果显示,11个菌株间的遗传相似系数范围为0.29~0.97,差异分枝明显,在相似系数为0.63时,可将11个菌株划分为3类,其中以含一个G.s0007-31相同核的5个双核体聚为一类,同样含G.s0012-28相同核的3个双核体和含G.s0004-11相同核的3个双核体各自聚为一类。聚类分析结果很好地反映了测试菌株之间的遗传关系。
2.4 体细胞不亲和性与遗传差异分析
根据SI检测(图1和表3)和11个测试菌株的遗传背景(表2),可知Ⅰ类的3对双核体的菌丝间无拮抗,其遗传背景为细胞核一样而细胞质不一样(细胞质数据未公开),表明亲缘关系很近,分子聚类结果显示其遗传相似系数接近“1”,即说明其差异非常小。构建的Ⅱ、Ⅲ、Ⅳ和Ⅴ双核体,其SI检测为不亲和,菌丝间存在拮抗,其中Ⅱ和Ⅳ配对的双核体表现为较弱拮抗和中等强度的拮抗,而Ⅲ和Ⅴ配对的双核体表现为中等、强和很强的拮抗;Ⅱ和Ⅳ配对双核体间的细胞核遗传背景为含有一个相同的细胞核,另一个细胞核不同,平均遗传相似系数为0.66,而Ⅲ和Ⅴ配对双核体间的细胞核均不同,平均遗传相似系数为0.52,这表明紫芝菌株间的拮抗强度越强,其遗传差异越大。
在构建的Ⅱ和Ⅳ双核体中,如Sh2与Sh14、Sh2与Sh15的配对,Sh3与Sh9、Sh3与Sh10的配对,它们的拮抗反应强度表现为一致,遗传相似系数也没有差异,在遗传背景上,它们只是细胞质存在差异而细胞核一样(Sh14与Sh15、Sh9与Sh10为同核异质体)。此外,在Ⅲ和Ⅴ双核体中,如Sh3与Sh13、Sh2与Sh21的配对,虽然每一组配对均含G.s0007-31、G.s0011-3、G.s0011-16和G.s0012-28这4个核(表2),但是Sh3与Sh13的拮抗强度强于Sh2与Sh21(图1),然而Sh3与Sh13的细胞质相同、Sh2与Sh21的细胞质不同,Sh3与Sh13的遗传相似系数为0.63,Sh2与Sh21的遗传相似系数为0.66(表3),在遗传上这两对组合的关系很近。这些结果表明细胞质并未影响紫芝双核体间的体细胞不亲和。
3. 讨论与结论
真菌的SI是由其遗传关系决定的,是由一套独立的系统控制,与SI位点有关。一般情况下,只有当个体间所有的SI位点相同时,才表现为体细胞亲和,而只要任何一个SI位点不同,则可能表现出不亲和性,SI位点差异越大,不亲和性反应的强度如色素产生量和气生菌丝的数量就越多[17]。虽然SI由SI位点控制,但已有研究表明个体间亲缘关系越远,遗传距离越大,拮抗现象越明显,则SI越强烈,反之亦然[18−19]。本研究构建的紫芝测试菌株中,Ⅰ类的菌株之间遗传关系最近,其SI表现为无拮抗。而亲缘关系较远的双核体之间则出现明显拮抗,如Sh14与Sh24遗传差异大,其配对的拮抗反应在所有测试菌株中最强。虽然Sh9与Sh13、Sh2与Sh21均由不同的细胞核组合,但构成的双核体中均含有来自亲本G.s0011的一对交配可亲和的单核体G.s0011-3和G.s0011-16,在遗传背景上,它们的亲缘关系较近,从分子标记聚类的结果也印证了Sh9与Sh13、Sh2与Sh21的遗传差异,同时其配对的拮抗反应表现为中等拮抗。这表明紫芝的SI反应与其遗传差异相关。此外,构成Sh3与Sh13、Sh2与Sh21配对的4个核都一样,在遗传关系上很近,只是4个核两两组合存在差异,而表现出的拮抗强度却不一样,Sh3与Sh13为强拮抗,Sh2与Sh21为中等强度拮抗,提示SI的反应强度与SI位点之间的相互作用有关。
细胞质对SI反应的影响很小。May [20]在研究灰盖鬼伞的SI发现,2个配对的双核菌丝,其细胞核相同而细胞质不同,虽有一些出现拮抗反应,但大部分的这类配对,其菌丝是相互交织在一起的。本研究构建的紫芝Ⅰ类菌株中,不同细胞质在含相同细胞核的菌株间除菌落表现出差异外,一些其配对的边缘菌丝交接触处虽然可以融合,但中间的菌丝融合受到一定的影响,而在Sh2与Sh14、Sh2与Sh15的配对中,Sh14和 Sh15为同核异质体,2个组合的配对其SI反应强度一样,受细胞质的影响不明显。这些结果说明,影响紫芝SI反应主要由细胞核的SI位点控制,细胞质的某些因子可能对其有影响,但对SI反应的影响也很小,这与Hansen等 [21]指出不同的细胞质可能会影响SI反应,但它不可能作为一个单独的控制因子去影响SI反应的观点相吻合。
本研究利用3种分子标记综合分析11个紫芝测试菌株的遗传关系,其聚类结果显示有G.s0007-31相同核的5个菌株聚为一大类,同时分别含有G.s0011-3和G.s0011-16核的Sh2与Sh12/ Sh13、Sh3/ Sh4与Sh21又各自聚为一小类,以上结果与这11个测试菌株的遗传背景完全吻合,这说明分子标记的结果具有更高的准确性及客观性。虽然SI试验是较为传统的分类鉴别方法,但其简单便捷且不受实验设备的限制,同时具有重要的现实意义。本研究揭示了两者之间遗传差异的联系,结果表明紫芝的SI反应强度与遗传差异大小相吻合,这可为应用拮抗反应判别紫芝菌株间的差异性提供参考,同时SI和分子标记也可应用于紫芝种质资源遗传关系的评价,为其后期杂交育种亲本的选择等研究提供遗传标记。
-
图 1 紫芝双核体在PDA培养基上的SI反应
F:正面;B:背面。异核体的配对类别分为,Ⅰ:同核异质体;Ⅱ:细胞质和一个核相同,另一个核不同;Ⅲ:细胞质相同,细胞核不同;Ⅳ:一个核相同,另一个核与细胞质都不同;Ⅴ:细胞质和细胞核均不同。CK代表对照组。
Figure 1. SI reactions of heterokaryotic G. sinense colonies on PDA
F: front; B: back. The five pairing types of heterokaryons, Ⅰ: same dikaryon in different FP; Ⅱ: one same monokaryon with one different monokaryon in the same FP; Ⅲ: different dikaryon in the same FP; Ⅳ: one same monokaryon with one different monokaryon in different FP; Ⅴ: different dikaryon in different FP. Control check(CK).
表 1 引物序列
Table 1 Sequences of primers for molecular markers
分子标记
Molecular marker引物
Primer序列(5′-3′)
Sequences分子标记
Molecular marker引物
Primer序列(5′-3′)
SequencesISSR ISSR6 DHB (CGA)5 SRAP ME4 TGAGTCCAAACCGGACC ISSR ISSR17 (TG)8RC SRAP ME5 TGAGTCCAAACCGGAAG ISSR ISSR18 VHV (GT)8 SRAP ME6 TGAGTCCAAACCGGTAG RAPD S17 AGGGAACGAG SRAP EM8 GACTGCGTACGAATTAGC RAPD S18 CCACAGCAGT SRAP EM13 GACTGCGTACGAATTGGT RAPD S367 AGCGAGCAAG SRAP EM14 GACTGCGTACGAATTCAG SRAP ME3 TGAGTCCAAACCGGAAT SRAP EM17 GACTGCGTACGAATTCCA ISSR引物中的单字母简写代表多碱基混合位点。位置:D= (A, G, T), H= (A, C, T), B= (C, G, T),R= (A, G),V= (A, C, G)。
Single letter abbreviations of ISSR primers for mixed base. Positions: D= (A, G, T), H= (A, C, T), B= (C, G, T), R= (A, G), V= (A, C, G).表 2 测试菌株信息
Table 2 Information on tested strains
菌株
Strain亲本和交配型
Parents and mating types菌株
Strain亲本和交配型
Parent and mating typeSh2 G.s0007-31FP A1B7、G.s0011-16 A3B3 Sh13 G.s0007-31 A1B7、G.s0011-3 FP A2B2 Sh3 G.s0011-16 FP A3B3、G.s0012-28 A5B5 Sh14 G.s0007-31 FP A1B7、G.s0012-26 A4B4 Sh4 G.s0011-16 A3B3、G.s0012-28 FP A5B5 Sh15 G.s0007-31 A1B7、G.s0012-26 FP A4B4 Sh9 G.s0004-11 A1B1、G.s0011-16 FP A3B3 Sh21 G.s0011-3 A2B2、G.s0012-28 FP A5B5 Sh10 G.s0004-11 FP A1B1、G.s0011-16 A3B3 Sh24 G.s0004-11 A1B1、G.s0014-36 FP A7B7 Sh12 G.s0007-31 FP A1B7、G.s0011-3 A2B2 FP代表母本。
FP:female parent.表 3 测试菌株的体细胞不和性与遗传关系
Table 3 Relationships between SI and genetic differences among strains
异核体类别
Type of heterokaryon配对
Pairing拮抗信息
Information of antagonism遗传相似系数
Genetic similarity coefficientⅠ 同核异质体
Same dikaryon in different FPSh3×Sh4 - 0.97 Sh12×Sh13 - 0.97 Sh14×Sh15 - 0.95 Ⅱ 细胞质和一个核相同,另一个核不同
one same monokaryon with one different monokaryon in the same FPSh2×Sh14 G+ 0.66 Sh2×Sh12 G+ 0.74 Sh3×Sh9 GL++ 0.66 Ⅲ 细胞质相同,细胞核不同
Different dikaryon in the same FPSh4×Sh15 G+++ 0.46 Sh3×Sh13 G+++ 0.63 Sh9×Sh13 G++ 0.57 Ⅳ 一个核相同,另一个核与细胞质都不同
one same monokaryon with one different monokaryon in different FPSh3×Sh10 GL++ 0.69 Sh2×Sh15 G+ 0.66 Sh3×Sh2 W-l S 0.54 Ⅴ 细胞质和细胞核均不同
Different dikaryon in different FPSh2×Sh21 G++ 0.66 Sh3×Sh14 G+++ 0.49 Sh14×Sh24 G++++ 0.29 FP代表母本;SI反应分为(1)无拮抗-,(2)隔离型G,和(3)隔离型带线状GL和(4)菌丝墙式结构W-l S;“+”表示弱拮抗,“++”中等拮抗,“+++”强拮抗,“++++”非常强拮抗。
FP: female parent; 4 types of SI including(1)-: no antagonism; (2)G: gap; (3)GL: gap with line; and(4) W-1 S: hyphal wall-like structure; +: slight reaction; ++: moderate reaction; +++: strong reaction;++++: extremely strong reaction. -
[1] 黄年来, 林志彬, 陈国良, 等. 中国食药用菌学[M]. 上海: 上海科学技术文献出版社, 2010. [2] 刘新锐, 王圣铕, 谢宝贵, 等. 紫芝不亲和性因子分析[J]. 菌物学报, 2014, 33(2): 464-468. LIU X R, WANG S Y, XIE B G, et al. Incompatibility factors of Ganoderma sinense[J]. Mycosystema, 2014, 33(2): 464-468. (in Chinese)
[3] TENG L M, WANG C, CUI B K, et al. Lanostane triterpenoids from mycelia-associated Ganoderma sinense and their anti-inflammatory activity [J]. Phytochemistry, 2023, 215: 113870. DOI: 10.1016/j.phytochem.2023.113870
[4] GAO S Y, ZHANG P, ZHANG C Y, et al. Meroterpenoids from Ganoderma sinense protect hepatocytes and cardiomyocytes from oxidative stress induced injuries [J]. Fitoterapia, 2018, 131: 73−79. DOI: 10.1016/j.fitote.2018.10.009
[5] WU N, PENG B, LI T, et al. Rapid simultaneous determination of four ganoderic acids in Ganoderma (chinese Name: Lingzhi) by direct infusion–multiple reaction monitoring cubed [J]. Journal of Analysis and Testing, 2024, 8(1): 52−62. DOI: 10.1007/s41664-023-00271-1
[6] MEI R Q, ZUO F J, DUAN X Y, et al. Ergosterols from Ganoderma sinense and their anti-inflammatory activities by inhibiting NO production [J]. Phytochemistry Letters, 2019, 32: 177−180. DOI: 10.1016/j.phytol.2019.06.006
[7] JIANG Y F, CHANG Y J, LIU Y, et al. Overview of Ganoderma sinense polysaccharide-an adjunctive drug used during concurrent Chemo/Radiation therapy for cancer treatment in China [J]. Biomedicine & Pharmacotherapy, 2017, 96: 865−870.
[8] HAN W, CHEN H J, ZHOU L, et al. Polysaccharides from Ganoderma Sinense - rice bran fermentation products and their anti-tumor activities on non-small-cell lung cancer [J]. BMC Complementary Medicine and Therapies, 2021, 21(1): 169. DOI: 10.1186/s12906-021-03346-7
[9] LIND M, STENLID J, OLSON A. Genetics and QTL mapping of somatic incompatibility and intraspecific interactions in the basidiomycete Heterobasidion annosum s. l[J]. Fungal Genetics and Biology: FG & B, 2007, 44(12): 1242−1251.
[10] MARCAIS B, CAËL O, DELATOUR C. Genetics of somatic incompatibility in Collybia fusipes [J]. Mycological Research, 2000, 104(3): 304−310. DOI: 10.1017/S0953756299001069
[11] 唐传红, 张劲松, 陈明杰, 等. 利用拮抗试验和RAPD对灵芝属菌株进行分类研究 [J]. 微生物学通报, 2005, 32(5):72−76. DOI: 10.3969/j.issn.0253-2654.2005.05.015 TANG C H, ZHANG J S, CHEN M J, et al. Study on classification of strains of Ganoderma by anatagonistic effect and rapd [J]. Microbiology, 2005, 32(5): 72−76. (in Chinese) DOI: 10.3969/j.issn.0253-2654.2005.05.015
[12] 李黎. 中国木耳栽培种质资源的遗传多样性研究[D]. 武汉: 华中农业大学, 2011. LI L. Studies on Genetic Diversity of Auricularia Auricula-judae Cultivated Germplasm Resources in China[D]. Wuhan: Huazhong Agricultural University, 2011. (in Chinese)
[13] 张瑞颖. 香菇菌株多相鉴定鉴别技术研究[D]. 北京: 中国农业大学, 2004. ZHANG R Y. Study on Polyphasic Strain-typing Technique of Lentinula Edodes[D]. Beijing: China Agricultural University, 2004. (in Chinese)
[14] 刘靖宇, 宋秀高, 叶夏, 等. 香菇菌株遗传多样性ISSR、RAPD和SRAP综合分析 [J]. 食用菌学报, 2011, 18(3):1−8. DOI: 10.3969/j.issn.1005-9873.2011.03.001 LIU J Y, SONG X G, YE X, et al. Differentiation of Lentinula edodes Strains Using ISSR, RAPD and SRAP markers [J]. Acta Edulis Fungi, 2011, 18(3): 1−8. (in Chinese) DOI: 10.3969/j.issn.1005-9873.2011.03.001
[15] 徐珍, 章炉军, 尚晓冬, 等. 金针菇品种DUS测试性状的分级与评价 [J]. 菌物学报, 2019, 38(5):658−668. XU Z, ZHANG L J, SHANG X D, et al. Gradation and evaluation for Flammulina filiformis DUS testing traits [J]. Mycosystema, 2019, 38(5): 658−668. (in Chinese)
[16] 刘靖宇, 刘新锐, 邓优锦, 等. 双向核迁移在香菇遗传和育种中的应用研究 [J]. 菌物学报, 2011, 30(5):774−781. LIU J Y, LIU X R, DENG Y J, et al. The application of the ‘bidirectional haploid nuclei migration’ in breeding and genetics of Lentinula edodes [J]. Mycosystema, 2011, 30(5): 774−781. (in Chinese)
[17] CATEN C E. Vegetative incompatibility and cytoplasmic infection in fungi [J]. Journal of General Microbiology, 1972, 72(2): 221−229. DOI: 10.1099/00221287-72-2-221
[18] WORRALL J J. Somatic incompatibility in basidiomycetes [J]. Mycologia, 1997, 89(1): 24−36. DOI: 10.1080/00275514.1997.12026751
[19] GIOVANNETTI M, SBRANA C, STRANI P, et al. Genetic diversity of isolates of Glomus mosseae from different geographic areas detected by vegetative compatibility testing and biochemical and molecular analysis [J]. Applied and Environmental Microbiology, 2003, 69(1): 616−624. DOI: 10.1128/AEM.69.1.616-624.2003
[20] MAY G. Somatic incompatibility and individualism in the coprophilous Basidiomycete, Coprinus cinereus [J]. Transactions of the British Mycological Society, 1988, 91(3): 443−451. DOI: 10.1016/S0007-1536(88)80121-9
[21] HANSEN E M, STENLID J, JOHANSSON M. Genetic control of somatic incompatibility in the root-rotting basidiomycete Heterobasidion annosum [J]. Mycological Research, 1993, 97(10): 1229−1233. DOI: 10.1016/S0953-7562(09)81290-2




 下载:
下载: