Risk Assessment on Resistance to Pyraclostrobin of Colletotrichum gloeosporioides
-
摘要:目的
探明福建省大豆胶孢炭疽菌群体对吡唑醚菌酯的敏感程度及其与其他杀菌剂的交互抗性。
方法采用菌丝生长速率法对2023年分离自福建省5个地区的112株大豆胶孢炭疽菌进行敏感性分析,以药剂驯化法获得抗性突变体,测定抗性突变体的遗传稳定性、适合度及对4种不同杀菌剂之间的交互抗性。
结果吡唑醚菌酯对112个菌株的EC50值介于
0.0682 ~1.0309 µg·mL−1,变异系数为15.12,敏感性频率分布为连续性单峰曲线,符合偏正态分布,EC50平均值(0.2036 ±0.1215) µg·mL−1,可作为大豆胶孢炭疽菌对吡唑醚菌酯的敏感性基线;从2株大豆胶孢炭疽菌野生菌株中诱导获得4株中抗吡唑醚菌酯的突变体,1株低抗吡唑醚菌酯的突变体,突变频率为8.3×10−4,其抗药性性状能稳定遗传,抗性突变体与其亲本菌株相比,对温度的敏感性存在差异,抗性突变体菌丝的生长速率、产孢能力及致病力略低于其亲本菌株的生存适应度,抗性突变体在田间可能存在一定适合度代价,但抗性突变体具有一定的自然竞争优势;吡唑醚菌酯与不同类杀菌剂多菌灵、苯醚甲环唑、咪鲜胺之间不存在交互抗性,与同属一类的杀菌剂啶氧菌酯存在明显的交互抗性。结论福建省大豆胶孢炭疽菌对吡唑醚菌酯具有较高的敏感性,但存在中等抗性风险,生产中可将吡唑醚菌酯与不同类杀菌剂多菌灵、苯醚甲环唑、咪鲜胺混合或交替使用,以延缓大豆胶孢炭疽菌抗药性的产生。
Abstract:ObjectiveDrug sensitivity to and cross-resistance of pyraclostrobin with other fungicides of Colletotrichum gloeosporioides that caused anthracnose in soybeans in Fujian Province were investigated.
MethodsSensitivity to pyraclostrobin of 112 strains of C. gloeosporioides isolated from 5 regions in the province in 2023 was determined using the mycelial production rate method. Resistant mutants of the pathogen were obtained by fungicide domestication to determine their genetic stability, fitness, and possible cross-resistance to 4 fungicides.
ResultsThe EC50 of pyraclostrobin for the 112 C. gloeosporioides strains ranged 0.0682 µg·mL−1 to 1.0309 µg·mL−1 with a coefficient of variation of 15.12 and averaged (0.203 6±0.121 5) µg·mL−1 as the sensitivity baseline. The distribution of the sensitivity frequency was in a continuous unimodal function consistent with the continuous skewed normal distribution. Induced from two wild C. gloeosporioides, 4 moderate resistant strains and one low resistant strain were secured at a frequency of 8.3×10−4. The mutants stably inherited the drug resistance traits but differed from their parents in temperature sensitivity and were slightly lower on mycelial growth rate, sporulation ability, and pathogenicity. In the field, they might sacrifice other natural competitive advantages as a fitness cost in exchange for the drug resistance. Pyraclostrobin showed no cross-resistance with carbendazim, difenoconazole, and prochloraz but did with the same type of fungicide, picoxystrobin.
ConclusionAlthough the C. gloeosporioides isolated in Fujian were relatively high in sensitivity to pyraclostrobin, they represented merely a moderate drug resistance risk. Nonetheless, in practice, it was plausible to blend pyraclostrobin or apply alternatively with fungicides such as carbendazim, difenoconazole, and prochloraz to delay such potential drawback.
-
0. 引言
【研究意义】由炭疽菌属(Colletotrichum spp.)真菌侵染引起的大豆炭疽病(soybean anthracnose),普遍存在于全球大豆主产区,包括中国、美国南部、巴西、印度、东南亚及南亚,已成为大豆十大重要病害之一[1]。影响炭疽病发生的主要环境因子为温度和降雨量,南方高温多雨的气候环境适宜该病的发生和流行,大豆炭疽病对南方鲜食大豆的生产造成严重影响,近年有明显加重的趋势[2−4]。目前,大豆炭疽病的防治除了采用抗病品种外,主要依靠化学药剂种子处理和喷施杀菌剂[5]。但随着药剂的常年使用和剂量的提高,导致病原菌对防治药剂的敏感性降低,产生抗药性[6]。因此,监测大豆炭疽病菌对防治药剂的敏感性具有重要意义。【前人研究进展】大豆炭疽病是一种种传病害,可侵染大豆的任何生长发育阶段,造成死苗、植株早衰、豆荚坏死,严重影响大豆的产量和外观品质,造成的产量损失达16%~50%,部分地块甚至绝收。1996—2007年,大豆炭疽病造成我国大豆产量损失累计达
1660 万t[7−8]。大豆炭疽病的病原菌种类繁多,包括平头炭疽菌、毁灭炭疽菌、胶胞炭疽菌以及禾谷炭疽菌等,福建省大豆炭疽病的病原菌主要为胶孢炭疽菌和平头炭疽菌2种[9−10]。我国登记注册用于防治炭疽病登记的杀菌剂主要有三唑类、咪唑类、甲氧基丙烯酸酯类和取代苯类等[11]。吡唑醚菌酯(德国巴斯夫公司)是一种甲氧基丙烯酸酯类杀菌剂,其通过阻断真菌线粒体中的电子传递链,有效抑制ATP合成,从而干扰真菌呼吸,抑制线粒体内能量产生,导致细胞死亡。吡唑醚菌酯不仅具有高活性、广谱杀菌、长效保护、低毒性和对环境生物安全的特点,还具有作物保健功能,诱导作物生理变化,增强作物的光合作用,促进蛋白质和干物质的积累,降低乙烯的生物合成,延缓衰老,增强作物抗逆性,提高作物产量和品质[12]。吡唑醚菌酯因其良好的防效和保健增产作用,被广泛用于不同作物的炭疽病防治。田间试验表明,吡唑醚菌酯对大豆炭疽病的防效达85.7%,且显著提高了大豆的产量和品质[13]。然而,甲氧基丙烯酸酯类杀菌剂由于其作用位点单一,抗药性问题也频繁出现。1996年,德国报道小麦白粉病对其产生了抗性,此后,陆续发现了葡萄霜霉病菌(Plasmopara viticola)、梨黑斑病菌(Alternaria alternata)、玉米大斑病菌(Exserohilum turcicum)、桃炭疽病菌(Colletotrichum siamense)的抗性菌株[14−15]。【本研究切入点】吡唑醚菌酯在用于防治大豆胶孢炭疽病中,长期大量使用是否引起病菌抗药性的产生有待深入研究。【拟解决的关键问题】测定分离自福建省不同地区大豆胶孢炭疽菌对吡唑醚菌酯的敏感性,建立其敏感基线,采用药剂驯化法筛选抗性突变体,测定抗性突变体的生物学特性及对其他杀菌剂的交互抗性情况,旨在为吡唑醚菌酯在防治大豆胶孢炭疽病中的科学用药策略制订、预防抗性产生等提供理论依据。1. 材料和方法
1.1 材料
1.1.1 供试菌株和品种
2022—2023年从福建省闽东(福州市、宁德市)、闽西(龙岩市)、闽南(漳州市)、闽北(南平市)、闽中(莆田市、三明市)等大豆主产区采集大豆炭疽病标本,分离并纯化获得单孢菌株,经鉴定和致病性测定,获得112株大豆胶孢炭疽菌,其中闽东地区24株、闽南地区31株、闽西地区27株、闽北地区15株、闽中地区15株。菌株保存在4 ℃的PDA斜面中,备用。供试大豆品种为毛豆3号,由福建省农业科学院作物研究所提供。
1.1.2 供试培养基
马铃薯葡萄糖培养基(PDA):马铃薯200 g、葡萄糖20 g、琼脂粉15 g、蒸馏水
1000 mL。1.1.3 供试药剂
供试药剂:98%吡唑醚菌酯和96%多菌灵(江苏辉丰生物农业股份有限公司),96.1%苯醚甲环唑(江苏耕耘化学有限公司),97%咪鲜胺(江苏辉丰农化股份有限公司),98%啶氧菌酯(山东潍坊润丰化工股份有限公司),99%水杨羟肟酸(Salicylohydroxamic, SHAM)[西格玛奥德里奇(上海)贸易有限公司]。母液配置:多菌灵用0.1 mol·L−1盐酸溶液配置,其他药剂用二甲基亚砜(dimethyl sulfoxide, DMSO)配置,SHAM配成质量浓度为1×105 µg·mL−1母液,非特定原药的其他药剂配制成1×104 µg·mL−1母液,置于4 ℃冰箱中备用。
1.2 方法
1.2.1 大豆胶孢炭疽菌对吡唑醚菌酯的敏感性测定
采用菌丝生长速率法[16],测定112株大豆胶孢炭疽菌对吡唑醚菌酯的敏感性。供试菌株在PDA平板上活化培养后,使用直径为5 mm的打孔器,从菌落边缘截取菌饼,将其菌丝面朝下接种至含有不同质量浓度吡唑醚菌酯(0.03~0.48 µg·mL−1)的PDA平板上。为减少旁路氧化途径的干扰,在含药平板中额外添加了质量浓度为50 µg·mL−1的SHAM。以加入等体积二甲基亚砜和SHAM的PDA平板作为对照。接种后的平板置于28 ℃黑暗培养7 d后,采用十字交叉法测量菌落直径,每处理3次重复。
参照周明国等[17] 的方法,计算各浓度处理下药剂对菌丝生长的抑制率,并进行回归分析,求出吡唑醚菌酯对各供试菌株的抑制中浓度EC50值、相关系数r、回归方程以及95%置信限。比较分析福建省5个地区大豆胶孢炭疽菌群体对吡唑醚菌酯的敏感性差异,计算不同地区菌株个体间的变异系数[18−19]。变异系数=EC50最大值/EC50最小值。对菌株的EC50值进行排序,并划分为7个不同的区间,然后统计每个区间内菌株的数量和频率。利用Shapiro-Wilk检验确认数据正态性后,绘制112株胶孢炭疽菌对吡唑醚菌酯的敏感性分布图。若呈正态分布,则以EC50均值作为福建省大豆胶孢炭疽菌的敏感基准[20]。随后,根据FRAC标准,进一步将菌株的EC50值与敏感基线进行比较,从而判断菌株的敏感性水平。当EC50值与基线的比值≤5时为敏感菌株;当比值在5~10时,为低抗菌株;在10~40时,为中抗菌株;而当比值>40时,则视为高抗菌株[21]。
1.2.2 室内抗性突变体诱导及筛选
参考乐默怡等[22] 的方法,药剂驯化诱导获得大豆胶孢炭疽菌抗吡唑醚菌酯突变体。选取大豆胶孢炭疽菌敏感菌株CG23017和CG23052作为野生敏感菌株,在PDA平板上活化培养5 d后,打取直径5 mm菌饼,转移至含1 µg·mL−1吡唑醚菌酯的PDA平板上,于28 ℃黑暗培养,待长出扇形突变后,转接至下个浓度含吡唑醚菌的PDA平板上,质量浓度梯度分别为2、5、10 µg·mL−1,PDA含药平板中加入质量浓度为50 µg·mL−1的SHAM。选取在含10 µg·mL−1吡唑醚菌酯的PDA平板上生长良好的菌株,转至无药平板复壮培养,标记为F1代。为评估菌株的抗性水平,进行抗性突变体EC50值的测定,并据此计算得到抗性倍数。同时,通过统计接种的菌饼中抗性菌株的数量,进一步得出抗性突变频率。根据计算所得的抗性倍数,菌株被划分为不同的抗性等级[23]:敏感(抗性倍数≤3)、低度抗性(抗性倍数在3~10)、中度抗性(抗性倍数在10~100)以及高度抗性(抗性倍数>100)。
1.2.3 抗药突变体的生物学性状研究
(1)抗性突变体抗药稳定性。参考范昆等[24] 的方法,将抗性突变体在无药PDA平板上连续转接至F7代,28 ℃黑暗培养7 d,每处理3次重复,利用菌丝生长速率法分别测定F1、F3、F5、F7代的EC50值。为分析抗性突变体在连续转接过程中的抗药稳定性,采用以下公式计算抗性倍数(RM):RM = 突变体的EC50 / 亲本菌株的EC50。
(2)抗性突变体对温度的敏感性。根据孙东晗等[25] 的方法,测定抗性突变体及其亲本菌株对不同温度(16 ℃、20 ℃、25 ℃、28 ℃、35 ℃)的敏感性。接种PDA平板后,菌饼在黑暗中培养7 d,每处理3次重复,以评估其在不同温度下的生长情况。
(3)抗性突变体的菌丝生长速率测定。按照乐默怡等[22] 的方法,将直径5 mm的菌饼接种在PDA平板上,于28 ℃黑暗条件下培养7 d。之后,用十字交叉法测量菌落直径,每处理3次重复,以计算并得出菌丝生长速率,菌丝生长速率/%=(菌落直径/菌丝生长天数)×100。
(4)抗性突变体的产孢能力测定。参考乐默怡等[22] 的方法,将活化的抗性突变体和亲本菌株制成直径5 mm的菌饼,接种在直径90 mm的PDA平板中央,28 ℃黑暗培养,10 d后用50 mL ddH2O,分数次加入培养皿中,用涂布棒将所有菌丝刮下,配置成分生孢子悬浮液,用血球计数板计算孢子浓度,计算单位面积内菌株产孢量,每处理3次重复。菌株产孢量=孢子浓度×50 mL/(3.14×菌落半径2)。
(5)抗性突变体的致病力测定。将活化的抗性突变体及其亲本菌株直径5 mm的菌饼接种于PDA平板中央(平板直径90 mm),28 ℃黑暗培养,10 d后用含0.1%吐温80 ddH2O,洗下分生孢子,配置成1×105 个·mL−1的孢子悬浮液,备用。毛豆3号,种植于埔垱基地,行距30 cm,株距15 cm,每处理种植4株,于大豆始荚期,傍晚喷施孢子悬浮液于大豆豆荚上,每处理100 mL,3次重复,以只喷施含0.1%吐温80 ddH2O为空白对照。14 d后,每个处理调查100个豆荚,依据以下分级标准计算病情指数。
大豆炭疽病病情分级标准如下[26]。0级:无病斑;1级:豆荚上有褐点型小病斑,病斑面积占整个豆荚面积的5%以下;3级:豆荚上出现典型病斑,病斑面积占整个豆荚面积的6%~10%;5级:豆荚上出现典型病斑,病斑面积占整个豆荚面积的11%~25%;7级:豆荚上出现典型病斑,病斑面积占整个豆荚面积的26%~50%;9级:豆荚上出现典型病斑,病斑面积占整个豆荚面积的50%以上。
病情指数=100×∑(各级病荚数×各级代表值)/(调查总荚数×9)
1.2.4 吡唑醚菌酯与不同杀菌剂间的交互抗性
采用1.2.1所述菌丝生长速率法,分别测定2个亲本菌和5个抗性突变体对多菌灵、苯醚甲环唑、咪鲜胺和啶氧菌酯的敏感性。多菌灵的质量浓度为0.01~0.16 µg·mL−1,苯醚甲环唑的质量浓度为0.1~0.8 µg·mL−1,咪鲜胺的质量浓度为0.01~0.08 µg·mL−1,啶氧菌酯的质量浓度为3~48 µg·mL−1。为减少旁路氧化途径的干扰,在啶氧菌酯的含药平板中额外添加质量浓度为50 µg·mL−1的SHAM。啶氧菌酯处理组以加入等体积二甲基亚砜和SHAM的PDA平板作为对照,苯醚甲环唑和咪鲜胺处理组以加入等体积二甲基亚砜的PDA平板作为对照,多菌灵处理组以加入等体积0.1 mol·L−1盐酸的PDA平板作为对照,每处理3次重复。根据亲本菌株和抗性突变体对多菌灵及其他药剂敏感性变化情况,判断交互抗性关系[19]。
1.3 数据分析
使用 Excel软件计算大豆炭疽病菌对杀菌剂的敏感性,包括毒力回归方程和有效中浓度的确定,并绘制敏感性频率分布图。采用Duncan氏新复极差法进行差异显著性检验;采用SPSS26.0软件进行Shapiro-Wilk正态性检验和相关性分析。
2. 结果与分析
2.1 大豆胶孢炭疽菌对吡唑醚菌酯的敏感性测定
供试菌株对吡唑醚菌酯的敏感性测定结果表明(表1),吡唑醚菌酯对112株大豆胶孢炭疽菌的毒力(EC50)值分布在
0.0682 ~1.0309 µg·mL−1,平均值为(0.2036 ±0.1215) µg·mL−1,菌株间变异系数为15.12;从地区上看,闽东、闽南、闽西、闽北和闽中5个地域内的大豆胶孢炭疽菌菌株对吡唑醚菌酯的毒力响应(EC50平均值)分别为0.1662 、0.1845 、0.2451 、0.2387 、0.1933 µg·mL−1,5个地区菌株群体间敏感性差异不显著;5个地区区域内菌株间变异系数分别为5.54、4.60、8.02、8.03和4.15。表 1 福建不同地区大豆胶孢炭疽菌对吡唑醚菌酯的敏感性Table 1. Sensitivity to pyraclostrobin of C. gloeosporioides isolated from regions in Fujian采集地区
Sampling region菌株数
Number of isolates吡唑醚菌酯EC50值
EC50 of Pyraclostrobin/(µg·mL−1)菌株间变异系数
Variation factor范围 Range 平均值 Mean 闽东地区 Eastern Fujian 24 0.0682 ~0.3777 0.1662 ±0.0633 a5.54 闽南地区 Southern Fujian 31 0.0763 ~0.3506 0.1845 ±0.0751 a4.60 闽西地区 Western Fujian 27 0.0801 ~0.6428 0.2451 ±0.1359 a8.02 闽北地区 Northern Fujian 15 0.1284 ~1.0309 0.2387 ±0.2269 a8.03 闽中地区 Central Fujian 15 0.0725 ~0.3007 0.1933 ±0.0670 a4.15 总计 Total 112 0.0682 ~1.0309 0.2036 ±0.1215 a15.12 表中数据为平均数±标准差。同列数据后不同小写字母分别表示经Duncan氏新复极差法检验差异显著(P<0.05)。下同。
Data are mean±SD; those with different lowercase letters on same column indicate significant difference at P<0.05 in Duncan's new multiple range test. Same for below.2.2 大豆胶孢炭疽菌对吡唑醚菌酯的敏感性分析
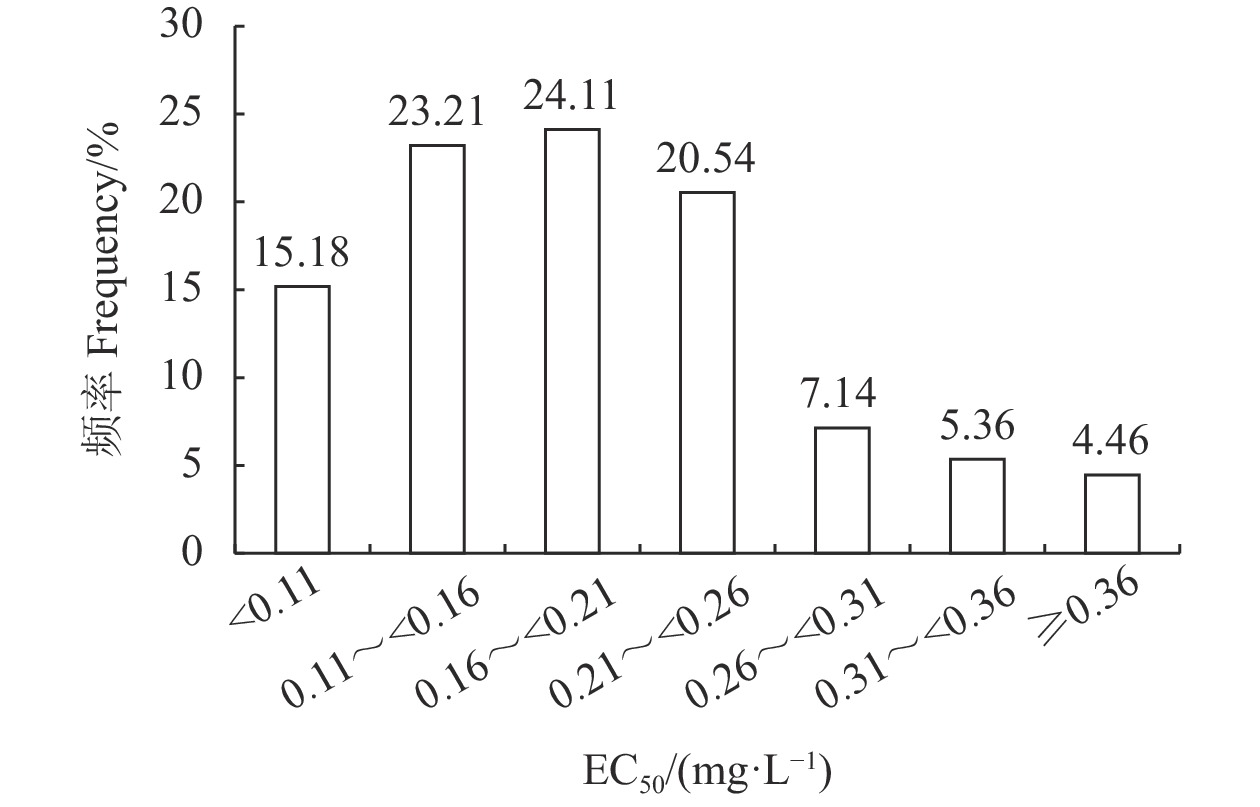
大豆胶孢炭疽菌对吡唑醚菌酯的敏感性分析表明(图1),112株测试菌株的敏感性频率分布呈连续性单峰曲线,且符合偏正态分布特征(skew=3.592, kurt=20.271, W=0.712, P<0.05)。在95%的显著性水平下,未观察到敏感性下降的亚群体。因此,确定EC50平均值为(
0.2036 ±0.1215) µg·mL−1作为福建省大豆胶孢炭疽菌对吡唑醚菌酯的敏感基线。比较各菌株的EC50值与敏感基线,发现1株为低抗菌株,抗性比值为5.06;111株为敏感菌株,抗性比值低于5。2.3 抗性突变体的获得及抗性水平测定
经过药剂驯化,成功筛选出5株抗性突变体(表2),这些突变体的突变频率为8.3×10−4,其中4株突变体的抗性倍数分别为13.10、14.29、18.71、16.84,表现为中抗水平,1株突变体抗性倍数为4.95,表现为低抗水平。
表 2 吡唑醚菌酯抗性突变体连续转代培养后EC50和抗性倍数的变化Table 2. Changes on EC50 and resistance multiple of pyraclostrobin-resistant C. gloeosporioides mutants after continuous generational transference菌株
Strain第一代
1st generation第三代
3rd generation第五代
5th generation第七代
7th generationEC50 /(µg·mL−1) RM EC50/(µg·mL−1) RM EC50/(µg·mL−1) RM EC50/(µg·mL−1) RM CG23017 0.1349 / 0.1396 / 0.1369 / 0.1344 / CG23017-1 1.7673 13.10 1.7823 12.77 1.7121 12.5 1.6661 12.39 CG23017-2 0.6674 4.95 0.5275 3.78 0.4891 3.57 0.4376 3.26 CG23017-3 1.9268 14.29 1.9084 13.67 1.8966 13.85 1.8612 13.85 CG23052 0.1611 / 0.1647 / 0.1623 / 0.1580 / CG23052-1 3.0151 18.71 3.0198 18.34 2.9742 18.33 2.9574 18.72 CG23052-2 2.7140 16.84 2.7191 16.51 2.7200 16.76 2.6425 16.73 RM为抗性倍数。
RM: resistance multiple.2.4 抗性突变体生物学性状
2.4.1 抗药稳定性
连续培养7代后,抗药突变体CG23017-1、CG23017-2、CG23017-3、CG23052-1和CG23052-2的EC50值分别为
1.6661 、0.4376 、1.8612 、2.9574 、2.6425 µg·mL−1(表2),抗性水平分别为12.39、3.26、13.85、18.72和16.73,抗性倍数保持在中抗和低抗水平,大豆胶孢炭疽菌对吡唑醚菌酯的抗性水平能稳定遗传。2.4.2 对温度的敏感性
对抗性突变体及其亲本菌株在不同温度条件下的生长特性测定结果发现,两者在温度敏感性上存在显著差异(表3)。抗性突变体与其亲本菌株的菌落直径均在28 ℃时达最大值,35 ℃时达最小值;在16 ℃时,突变体CG23017-3和CG23052-1与亲本菌株在菌落直径上未见显著差异,而突变体CG23017-1、CG23017-2和CG23052-2则表现出显著的差异;在20 ℃条件下,突变体CG23017-1和CG23052-2与亲本菌株的菌落直径相近,但突变体CG23017-2、CG23017-3和CG23052-1则呈现出显著差异;在25 ℃时,突变体CG23017-1、CG23017-2和CG23017-3与亲本菌株的菌落直径差异不明显,而突变体CG23052-1和CG23052-2则显示出显著差异。然而,值得注意的是,在28 ℃和35 ℃条件下,所有抗性突变体与其亲本菌株的菌落直径均未见显著差异。
表 3 抗性突变体及其亲本菌株对温度的敏感性测定Table 3. Mycelial growth of resistant mutants and parents under different temperatures菌株 Strain 菌落直径 Colony diameter/mm 16 ℃ 20 ℃ 25 ℃ 28 ℃ 35 ℃ CG23017 31.33±0.58 cd 43.33±1.53 c 59.33±2.31 c 63.67±1.53 b 20.67±1.53 a CG23017-1 28.67±0.58 e 41.33±1.15 cd 58.33±1.15 c 60.67±1.53 b 18.67±3.06 ab CG23017-2 25.33±1.15 f 37.67±1.15 e 56.67±1.53 c 60.33±2.31 b 19.33±1.53 ab CG23017-3 29.67±1.53 de 39.33±1.53 de 57.33±1.53 c 60.67±2.31 b 19.67±1.15 ab CG23052 35.67±2.08 a 48.33±1.15 a 72.67±0.58 a 74.67±1.53 a 17.67±1.53 ab CG23052-1 34.33±1.53 ab 45.67±1.15 b 69.67±1.15 b 71.67±1.53 a 18.33±0.58 ab CG23052-2 32.33±1.53 bc 46.33±0.58 ab 68.33±1.53 b 71.33±2.52 a 16.67±2.52 b 2.4.3 抗性突变体的适生性
经对抗性突变体的适生性测定发现(表4),5个抗性突变体的菌丝生长速率和产孢能力均略低于其亲本菌株;CG23017-1、CG23017-3和CG23052-2 3个抗性突变体接种后大豆的病情指数与其亲本菌株相比,无显著性差异;CG23017-2和CG23052-1抗性突变体接种后大豆的病情指数显著低于其亲本菌株。
表 4 抗性突变体及其亲本菌株菌丝生长速率、产孢能力、致病力测定Table 4. Mycelial growth rate, sporulation per area, and disease index of resistant mutants and parents菌株
Strain菌丝生长速率
Mycelium growth rate/(mm·d−1)单位面积产孢量
Sporulation per area/(×103个·mm−2)病情指数
Disease indexCG23017 9.1±0.22 b 4.58±0.27 ab 47.52±2.34 a CG23017-1 8.67±0.22 b 4.55±0.19 ab 40.37±4.56 a CG23017-2 8.62±0.33 b 4.32±0.08 b 27.08±4.83 b CG23017-3 8.67±0.33 b 4.50±0.26 ab 42.48±10.06 a CG23052 10.67±0.22 a 4.77±0.25 a 41.48±8.82 a CG23052-1 10.24±0.22 a 4.74±0.23 a 26.63±6.32 b CG23052-2 10.19±0.36 a 4.61±0.2 ab 37.43±0.89 ab 5株抗性突变体在整体的生存适应度方面略低于亲本菌株。其中3株中抗突变体的菌丝生长速度、产孢能力、致病力等生存适合度与其亲本菌株无显著性差异;1株中抗突变体、1株低抗突变体菌丝生长速度、产孢能力与其亲本菌株无显著性差异,致病力显著低于其亲本菌株。
2.5 抗性突变体交互抗性
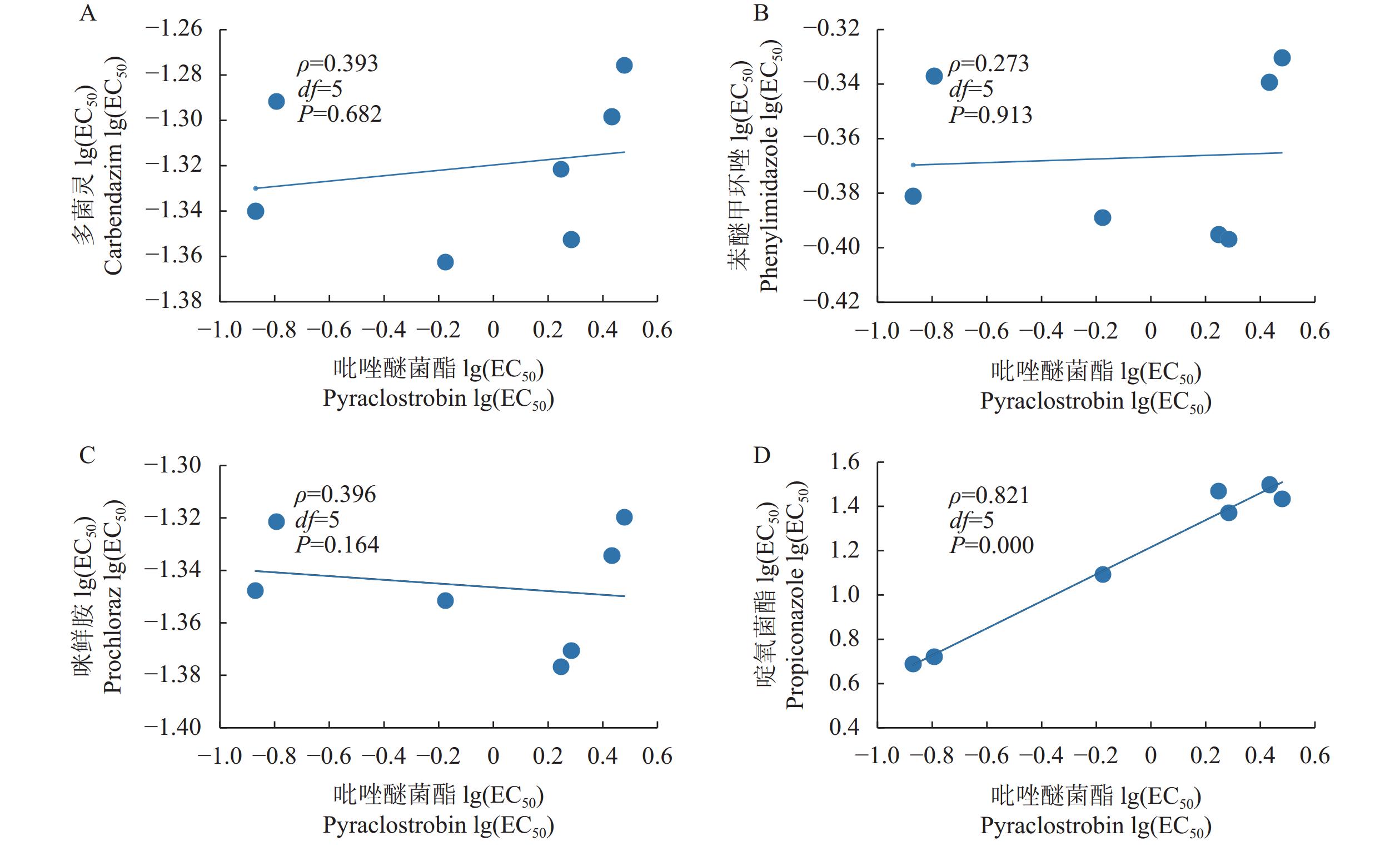
交互抗性分析结果表明,吡唑醚菌酯与多菌灵、苯醚甲环唑、咪鲜胺和啶氧菌酯的相关性方程分别为y=−
1.3197 +0.0119 x(ρ=0.393,P=0.682,图2A)、y=−0.3668 +0.0033 x(ρ=0.273,P=0.913,图2B)、y=−1.3465 −0.0071 x(ρ=0.396,P=0.164,图2C)和y=1.2159 +0.6111 x(ρ=0.821,P=0.000,图2D),说明吡唑醚菌酯与不同类杀菌剂多菌灵、苯醚甲环唑、咪鲜胺之间不存在交互抗性,与同类杀菌剂啶氧菌酯存在交互抗性。3. 讨论与结论
大豆炭疽病是南方大豆生产中的重要病害。吡唑醚菌酯作为一种甲氧基丙烯酸酯类杀菌剂,已被广泛用于作物炭疽病的防治。研究表明,吡唑醚菌酯对大豆、辣椒、草莓等作物炭疽病菌均具有较好的防治效果[13,14,21],25%吡唑醚菌酯26.67 g·hm−2对大豆炭疽病的田间防效达75.8%,草莓炭疽病菌的敏感基线为(0.36±0.162) µg·mL−1,辣椒炭疽病菌的敏感基线为(
0.2272 ±0.2027) µg·mL−1。吡唑醚菌酯对大豆炭疽病具有较好的防治效果,且其保健增产作用还能显著提高大豆的产量和品质[13]。本研究分析了福建省大豆胶孢炭疽菌对吡唑醚菌酯的敏感性特征。结果显示,其EC50值分布于0.0682 ~1.0309 µg·mL−1,敏感性频率分布呈现为连续的单峰曲线,符合连续的偏正态分布。据此,确立的敏感性基线值为(0.2036 ±0.1215 ) µg·mL−1,经比对发现,低抗菌株仅1株,而敏感菌株高达111株,这一数据有力验证了福建省大豆胶孢炭疽菌对吡唑醚菌酯的显著敏感性,吡唑醚菌酯用于大豆胶孢炭疽病菌的防治潜力较大。通过药剂驯化,从2株大豆胶孢炭疽菌野生菌株中诱导获得4株中抗吡唑醚菌酯的突变体,1株低抗吡唑醚菌酯的突变体。抗性突变体生物学性状测定发现,抗性突变体继代培养能稳定遗传;抗性突变体相较于亲本菌株,在温度敏感性上表现出差异性,并且在生长速率、产孢能力和致病性方面存在轻微的适应度劣势,但抗性突变体具有一定的自然竞争优势,在特定条件下,也可能形成优势菌群,此结果与孙东晗等[25]研究的西瓜蔓枯病菌抗吡唑醚菌酯突变体的结论一致,因此,大豆胶孢炭疽菌对吡唑醚菌酯存在中等抗性风险。交互抗性研究发现,吡唑醚菌酯与常用不同类杀菌剂多菌灵、苯醚甲环唑、咪鲜胺之间不存在交互抗性,与同类杀菌剂啶氧菌酯存在交互抗性,这与姚锦爱[21]、孙东晗[25]、董国然[27]等研究报道结果一致。因此,混合或交替使用吡唑醚菌酯与不同类别的杀菌剂,如多菌灵、苯醚甲环唑、咪鲜胺,不仅可以提高大豆胶孢炭疽病防控效果,还有助于延缓大豆胶孢炭疽菌抗药性的产生。吡唑醚菌酯对大豆炭疽病菌具有较好的抑制效果,在田间的防治中,应对吡唑醚菌酯的合理使用进行指导,应与多菌灵、苯醚甲环唑、咪鲜胺混合或交替使用,以延缓大豆胶孢炭疽菌抗药性的产生,同时要加强田间抗药性监测。
-
表 1 福建不同地区大豆胶孢炭疽菌对吡唑醚菌酯的敏感性
Table 1 Sensitivity to pyraclostrobin of C. gloeosporioides isolated from regions in Fujian
采集地区
Sampling region菌株数
Number of isolates吡唑醚菌酯EC50值
EC50 of Pyraclostrobin/(µg·mL−1)菌株间变异系数
Variation factor范围 Range 平均值 Mean 闽东地区 Eastern Fujian 24 0.0682 ~0.3777 0.1662 ±0.0633 a5.54 闽南地区 Southern Fujian 31 0.0763 ~0.3506 0.1845 ±0.0751 a4.60 闽西地区 Western Fujian 27 0.0801 ~0.6428 0.2451 ±0.1359 a8.02 闽北地区 Northern Fujian 15 0.1284 ~1.0309 0.2387 ±0.2269 a8.03 闽中地区 Central Fujian 15 0.0725 ~0.3007 0.1933 ±0.0670 a4.15 总计 Total 112 0.0682 ~1.0309 0.2036 ±0.1215 a15.12 表中数据为平均数±标准差。同列数据后不同小写字母分别表示经Duncan氏新复极差法检验差异显著(P<0.05)。下同。
Data are mean±SD; those with different lowercase letters on same column indicate significant difference at P<0.05 in Duncan's new multiple range test. Same for below.表 2 吡唑醚菌酯抗性突变体连续转代培养后EC50和抗性倍数的变化
Table 2 Changes on EC50 and resistance multiple of pyraclostrobin-resistant C. gloeosporioides mutants after continuous generational transference
菌株
Strain第一代
1st generation第三代
3rd generation第五代
5th generation第七代
7th generationEC50 /(µg·mL−1) RM EC50/(µg·mL−1) RM EC50/(µg·mL−1) RM EC50/(µg·mL−1) RM CG23017 0.1349 / 0.1396 / 0.1369 / 0.1344 / CG23017-1 1.7673 13.10 1.7823 12.77 1.7121 12.5 1.6661 12.39 CG23017-2 0.6674 4.95 0.5275 3.78 0.4891 3.57 0.4376 3.26 CG23017-3 1.9268 14.29 1.9084 13.67 1.8966 13.85 1.8612 13.85 CG23052 0.1611 / 0.1647 / 0.1623 / 0.1580 / CG23052-1 3.0151 18.71 3.0198 18.34 2.9742 18.33 2.9574 18.72 CG23052-2 2.7140 16.84 2.7191 16.51 2.7200 16.76 2.6425 16.73 RM为抗性倍数。
RM: resistance multiple.表 3 抗性突变体及其亲本菌株对温度的敏感性测定
Table 3 Mycelial growth of resistant mutants and parents under different temperatures
菌株 Strain 菌落直径 Colony diameter/mm 16 ℃ 20 ℃ 25 ℃ 28 ℃ 35 ℃ CG23017 31.33±0.58 cd 43.33±1.53 c 59.33±2.31 c 63.67±1.53 b 20.67±1.53 a CG23017-1 28.67±0.58 e 41.33±1.15 cd 58.33±1.15 c 60.67±1.53 b 18.67±3.06 ab CG23017-2 25.33±1.15 f 37.67±1.15 e 56.67±1.53 c 60.33±2.31 b 19.33±1.53 ab CG23017-3 29.67±1.53 de 39.33±1.53 de 57.33±1.53 c 60.67±2.31 b 19.67±1.15 ab CG23052 35.67±2.08 a 48.33±1.15 a 72.67±0.58 a 74.67±1.53 a 17.67±1.53 ab CG23052-1 34.33±1.53 ab 45.67±1.15 b 69.67±1.15 b 71.67±1.53 a 18.33±0.58 ab CG23052-2 32.33±1.53 bc 46.33±0.58 ab 68.33±1.53 b 71.33±2.52 a 16.67±2.52 b 表 4 抗性突变体及其亲本菌株菌丝生长速率、产孢能力、致病力测定
Table 4 Mycelial growth rate, sporulation per area, and disease index of resistant mutants and parents
菌株
Strain菌丝生长速率
Mycelium growth rate/(mm·d−1)单位面积产孢量
Sporulation per area/(×103个·mm−2)病情指数
Disease indexCG23017 9.1±0.22 b 4.58±0.27 ab 47.52±2.34 a CG23017-1 8.67±0.22 b 4.55±0.19 ab 40.37±4.56 a CG23017-2 8.62±0.33 b 4.32±0.08 b 27.08±4.83 b CG23017-3 8.67±0.33 b 4.50±0.26 ab 42.48±10.06 a CG23052 10.67±0.22 a 4.77±0.25 a 41.48±8.82 a CG23052-1 10.24±0.22 a 4.74±0.23 a 26.63±6.32 b CG23052-2 10.19±0.36 a 4.61±0.2 ab 37.43±0.89 ab -
[1] 刘勇, 叶鹏盛, 曾华兰, 等. 豆类炭疽病病原物种类及其发生研究进展 [J]. 微生物学通报, 2021, 48(11):4296−4305. LIU Y, YE P S, ZENG H L, et al. Research progress on pathogen species and occurrence of bean anthracnose [J]. Microbiology China, 2021, 48(11): 4296−4305. (in Chinese)
[2] 孙志峰. 大豆豆荚炭疽病的发病因子及其防治研究[D]. 杭州: 浙江大学, 2008. SUN Z F. Study on disease factors of soybean pod anthracnose and its control [D]. Hangzhou: Zhejiang University, 2008. (in Chinese)
[3] 冯乐乐, 竹龙鸣, 谢华, 等. 浙江省鲜食大豆炭疽病病原分离及抗性鉴定 [J]. 植物病理学报, 2021, 51(6):840−849. FENG L L, ZHU L M, XIE H, et al. Identification of the pathogen of vegetable soybean anthracnose in Zhejiang Province and evaluation of soybean cultivars for resistance to Colletotrichum truncatum [J]. Acta Phytopathologica Sinica, 2021, 51(6): 840−849. (in Chinese)
[4] 李月, 林剑浩, 年海, 等. 南方大豆品种炭疽病抗性鉴定及抗病相关基因表达分析 [J]. 大豆科学, 2023, 42(1):12−22. DOI: 10.11861/j.issn.1000-9841.2023.01.0012 LI Y, LIN J H, NIAN H, et al. Resistance identification of southern soybean varieties to anthracnose and expression analysis of resistance-related genes [J]. Soybean Science, 2023, 42(1): 12−22. (in Chinese) DOI: 10.11861/j.issn.1000-9841.2023.01.0012
[5] 李建飞, 王肖肖, 舒跃, 等. 大豆炭疽病的分类、流行监测与防治研究进展 [J]. 浙江大学学报(农业与生命科学版), 2023, 49(4):463−471. LI J F, WANG X X, SHU Y, et al. Advances in the pathogenic classification, epidemiological monitoring and control of soybean anthracnose [J]. Journal of Zhejiang University (Agriculture and Life Sciences), 2023, 49(4): 463−471. (in Chinese)
[6] 许媛, 肖婷, 褚姝频, 等. 江苏省句容市葡萄炭疽病菌多样性及对苯并咪唑类杀菌剂的抗药性分析 [J]. 南京农业大学学报, 2022, 45(1):78−85. DOI: 10.7685/jnau.202104019 XU Y, XIAO T, CHU S P, et al. The diversity and resistance to benzimidazole fungicides of the Colletotrichum spp. causing grape anthracnose in Jurong City of Jiangsu Province [J]. Journal of Nanjing Agricultural University, 2022, 45(1): 78−85. (in Chinese) DOI: 10.7685/jnau.202104019
[7] WRATHER A, KOENNING S. Effects of diseases on soybean yields in the United States 1996 to 2007 [J]. Plant Health Progress, 2009, 10(1): 24−30. DOI: 10.1094/PHP-2009-0401-01-RS
[8] DIAS M D, PINHEIRO V F, CAFÉ-FILHO A C. Impact of anthracnose on the yield of soybean subjected to chemical control in the north region of Brazil [J]. Summa Phytopathologica, 2016, 42(1): 18−23. DOI: 10.1590/0100-5405/2114
[9] 刘娜, 范翘楚, 周佳, 等. 菜用大豆炭疽病病原菌的分离鉴定与防治 [J]. 浙江农业学报, 2022, 34(12):2682−2688. DOI: 10.3969/j.issn.1004-1524.2022.12.11 LIU N, FAN Q C, ZHOU J, et al. Identification and control of anthracnose in vegetable soybean [J]. Acta Agriculturae Zhejiangensis, 2022, 34(12): 2682−2688. (in Chinese) DOI: 10.3969/j.issn.1004-1524.2022.12.11
[10] 石妞妞, 阮宏椿, 揭宇琳, 等. 福建省大豆炭疽病病原菌的分离与鉴定 [J]. 植物保护学报, 2022, 49(2):539−546. SHI N N, RUAN H C, JIE Y L, et al. Isolation and identification of Colletotrichum species associated with soybean anthracnose in Fujian Province [J]. Journal of Plant Protection, 2022, 49(2): 539−546. (in Chinese)
[11] 孙伟, 陈淑宁, 闫晓静, 等. 我国防治炭疽病杀菌剂的应用现状 [J]. 现代农药, 2022, 21(2):1−6. DOI: 10.3969/j.issn.1671-5284.2022.02.001 SUN W, CHEN S N, YAN X J, et al. Application status of fungicides to control anthracnose disease in China [J]. Modern Agrochemicals, 2022, 21(2): 1−6. (in Chinese). DOI: 10.3969/j.issn.1671-5284.2022.02.001
[12] YPEMA H L, GOLD R E. Kresoxim - methyl: Modification of a naturally occurring compound to produce a new fungicide [J]. Plant Disease, 1999, 83(1): 4−19. DOI: 10.1094/PDIS.1999.83.1.4
[13] 陈雨, 张爱芳, 夏本勇, 等. 吡唑醚菌酯对大豆炭疽病防效及保健增产作用 [J]. 农药, 2011, 50(9):697−699. DOI: 10.3969/j.issn.1006-0413.2011.09.025 CHEN Y, ZHANG A F, XIA B Y, et al. Efficacy of pyraclostrobin in controlling soybean anthracnose and their effects on the health protection and yield increase [J]. Agrochemicals, 2011, 50(9): 697−699. (in Chinese) DOI: 10.3969/j.issn.1006-0413.2011.09.025
[14] 陈鹏宇. 吉林省及内蒙古东部地区辣椒炭疽病的病原鉴定及Colletotrichum scovillei对3种杀菌剂的抗性风险评估[D]. 长春: 吉林农业大学, 2023. CHEN P Y. Pathogen identification of capsicum anthracnose and risk assessment of resistance of Colletotrichum scovillei to three fungicides in Jilin province and eastern Iner Mongolia [D]. Changchun: Jilin Agricultural University, 2023. (in Chinese)
[15] USMAN H M, TAN Q, KARIM M M, et al. Sensitivity of Colletotrichum fructicola and Colletotrichum siamense of peach in China to multiple classes of fungicides and characterization of Pyraclostrobin-resistant isolates [J]. Plant Disease, 2021, 105(11): 3459−3465. DOI: 10.1094/PDIS-04-21-0693-RE
[16] 慕立义. 植物化学保护研究方法[M]. 北京: 中国农业出版社, 1994: 79-81. [17] 周明国, 王建新. 禾谷镰孢菌对多菌灵的敏感性基线及抗药性菌株生物学性质研究 [J]. 植物病理学报, 2001, 31(4):365−370. DOI: 10.3321/j.issn:0412-0914.2001.04.014 ZHOU M G, WANG J X. Study on sensitivity base-line of Fusarium graminearum to carbendazim and biological characters of mbc-resistant strains [J]. Acta Phytopathologica Sinica, 2001, 31(4): 365−370. (in Chinese) DOI: 10.3321/j.issn:0412-0914.2001.04.014
[18] SONG Y Y, XU D T, LU H B, et al. Baseline sensitivity and efficacy of the sterol biosynthesis inhibitor triflumizole against Botrytis cinerea [J]. Australasian Plant Pathology, 2016, 45(1): 65−72. DOI: 10.1007/s13313-015-0384-1
[19] 毕秋艳, 马志强, 韩秀英, 等. 不同机制杀菌剂对小麦白粉病的敏感性及与三唑酮的交互抗性 [J]. 植物保护学报, 2017, 44(2):331−336. BI Q Y, MA Z Q, HAN X Y, et al. Sensitivity of diverse fungicides on powdery mildew of wheat and cross resistance with triadimefon [J]. Journal of Plant Protection, 2017, 44(2): 331−336. (in Chinese)
[20] 李宝燕, 栾炳辉, 石洁, 等. 胶东地区葡萄白腐病菌对吡唑醚菌酯的敏感性及与其他4种药剂的敏感性比较 [J]. 农药学学报, 2020, 22(6):959−966. LI B Y, LUAN B H, SHI J, et al. Sensitivity of Coniella diplodiella to pyraclostrobin in Jiaodong Area and comparison with four other fungicides [J]. Chinese Journal of Pesticide Science, 2020, 22(6): 959−966. (in Chinese)
[21] 姚锦爱, 赖宝春, 黄鹏, 等. 福建省草莓炭疽病菌对吡唑醚菌酯的敏感性及与其他药剂的交互抗性 [J]. 植物保护学报, 2022, 49(4):1263−1268. YAO J A, LAI B C, HUANG P, et al. Sensitivity to pyraclostrobin and cross-resistance against six fungicides in strawberry anthracnose pathogen Colletotrichum gloeosporioides from Fujian Province [J]. Journal of Plant Protection, 2022, 49(4): 1263−1268. (in Chinese)
[22] 乐默怡, 王蓉, 李勇, 等. 人参灰霉病菌对咪鲜胺敏感性基线的建立及抗药性风险评估 [J]. 中国中药杂志, 2023, 48(3):636−641. LE M Y, WANG R, LI Y, et al. Sensitivity baseline establishment and resistance risk assessment of Botrytis cinerea from Panax ginseng to prochloraz [J]. China Journal of Chinese Materia Medica, 2023, 48(3): 636−641. (in Chinese)
[23] 鲜菲, 刘顺涛, 李雨, 等. 西南地区稻瘟病菌对戊唑醇的敏感性基线建立及抗性监测 [J]. 农药学学报, 2015, 17(6):753−756. DOI: 10.3969/j.issn.1008-7303.2015.06.017 XIAN F, LIU S T, LI Y, et al. Sensitivity base-line and resistance detection of Magnaporthe grisea to tebuconazole in southwest of China [J]. Chinese Journal of Pesticide Science, 2015, 17(6): 753−756. (in Chinese) DOI: 10.3969/j.issn.1008-7303.2015.06.017
[24] 范昆, 付丽, 李晓军, 等. 苹果轮纹病菌对戊唑醇的敏感性及其抗性突变体的致病力 [J]. 植物保护, 2017, 43(1):140−147. DOI: 10.3969/j.issn.0529-1542.2017.01.024 FAN K, FU L, LI X J, et al. Susceptibility of Botryosphaeria dothidea to tebuconazole and virulence of its resistant mutants [J]. Plant Protection, 2017, 43(1): 140−147. (in Chinese) DOI: 10.3969/j.issn.0529-1542.2017.01.024
[25] 孙东晗, 陈悦, 田文学, 等. 吉林省西瓜蔓枯病菌对吡唑醚菌酯的抗性监测及抗性风险评估 [J]. 植物保护学报, 2022, 49(6):1663−1672. SUN D H, CHEN Y, TIAN W X, et al. Monitoring and risk evaluation of the resistance to pyraclostrobin in gummy stem blight pathogen Stagonosporopsis citrulli from watermelon in Jilin Province [J]. Journal of Plant Protection, 2022, 49(6): 1663−1672. (in Chinese)
[26] 福建省质量技术监督局. 大豆抗炭疽病鉴定技术规范: DB35/T 1574—2016[S]. 2016. [27] 董国然. 芒果蒂腐病菌可可毛色二孢对吡唑醚菌酯抗性机制研究[D]. 海口: 海南大学, 2021. DONG G R. Resistance of Botryodiplodia theobromae caused mango stem end rot to pyraclostrobin in Hainan [D]. Haikou: Hainan University, 2021. (in Chinese)
-
期刊类型引用(1)
1. 刘勉,肖玉辉,勾朝金,古旭,芦俊佳. 大花海棠炭疽病病原菌鉴定、生物学特性测定及防治药剂室内毒力测定. 南方农业学报. 2025(02): 508-519 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载: