Differentiate Transcriptomes of Aerial and Creepy Agaricus bisporus Hyphae
-
摘要:目的
挖掘双孢蘑菌落形态变化可能涉及的重要基因,为双孢蘑菇种质资源评价、新品种选育提供科学依据。
方法以双孢蘑菇主栽品种As2796为试验菌株,收集同一平板上生长的贴生与气生菌丝,提取样品的RNA进行转录组测序分析。
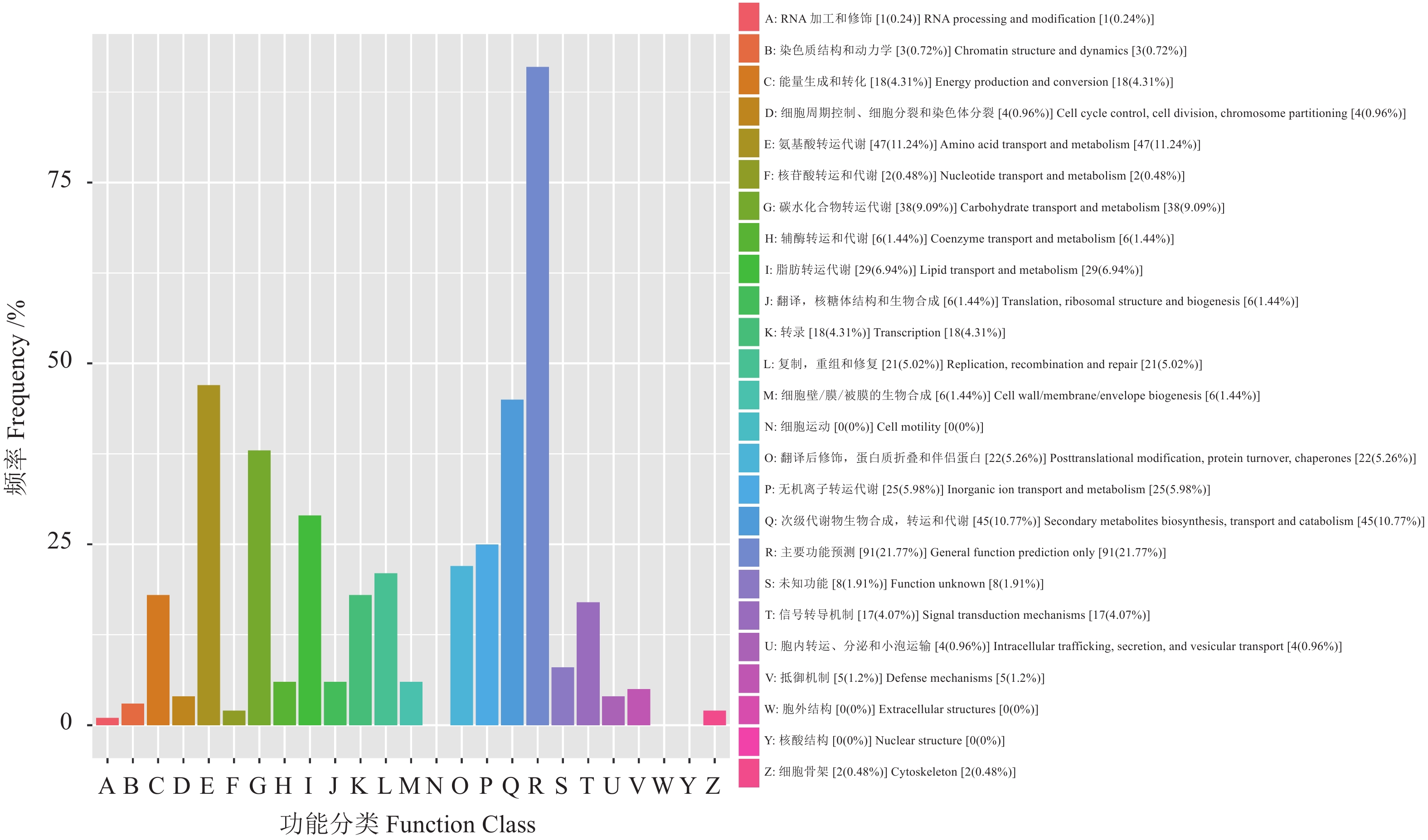
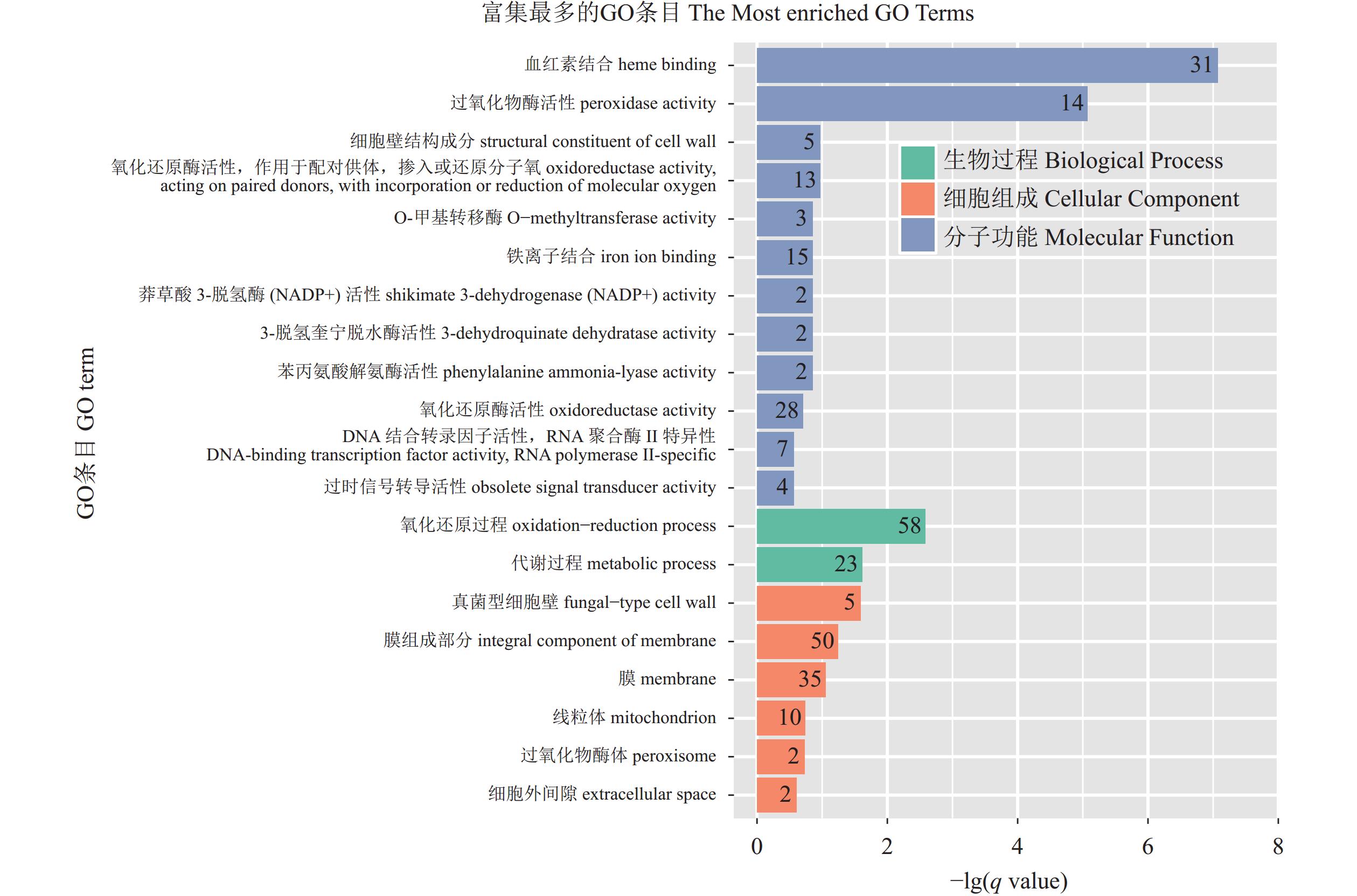
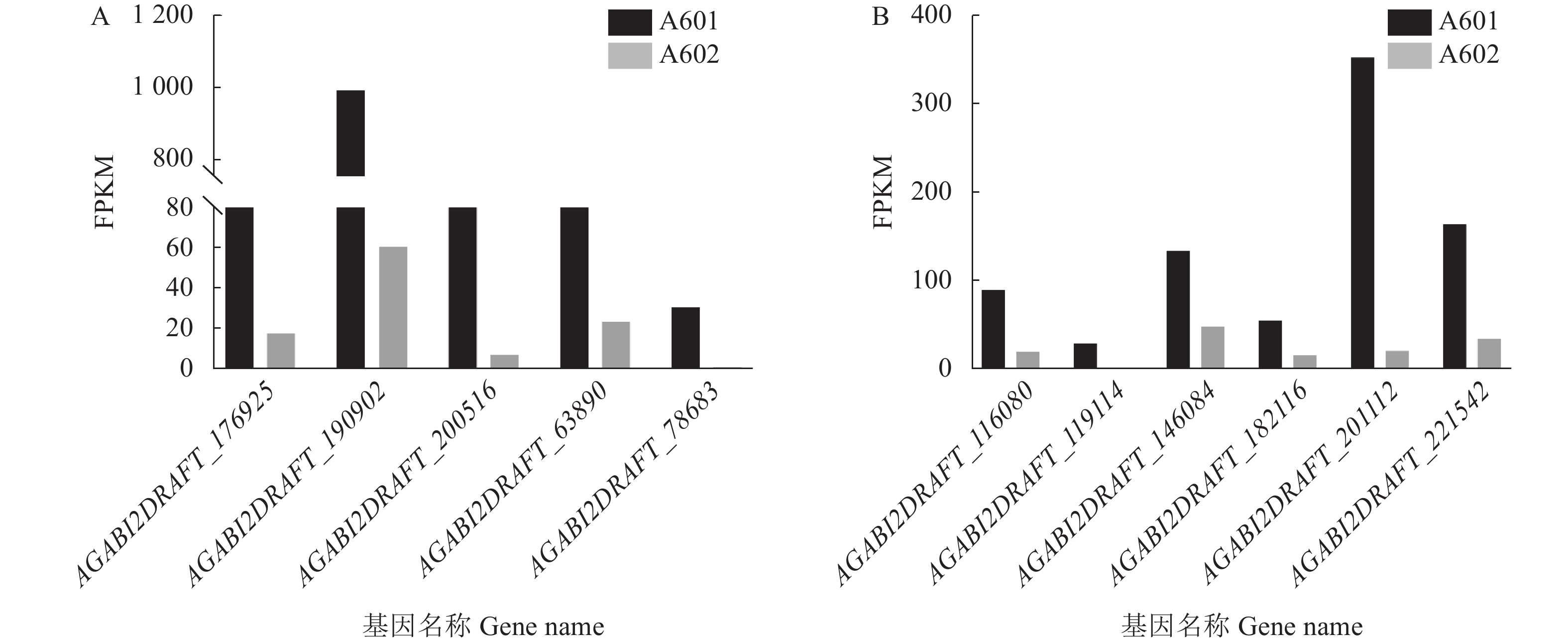
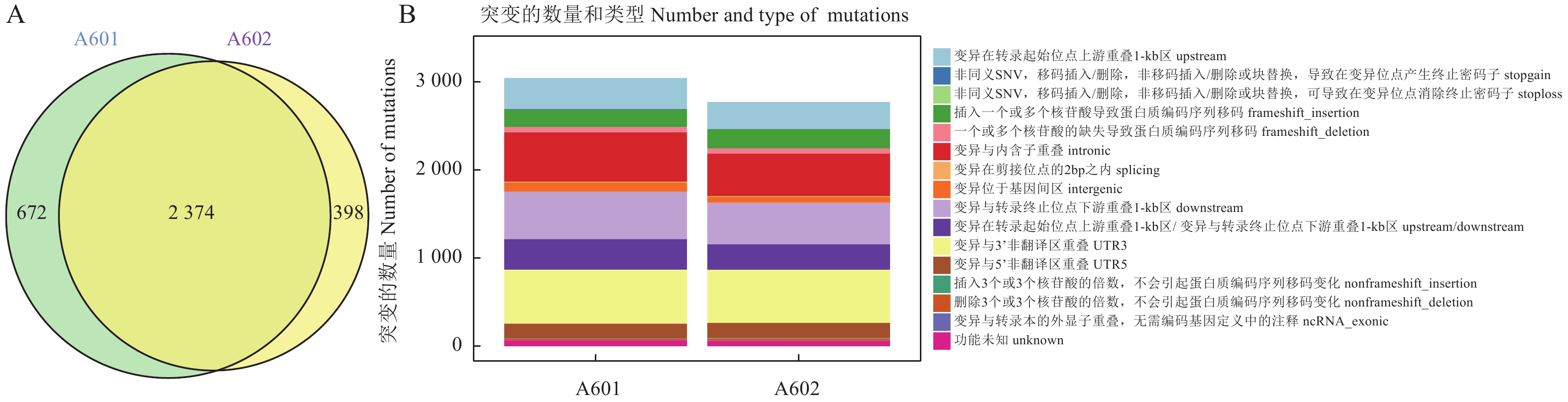
结果通过转录组分析,A601(As2796气生组)与A602(As2796贴生组)共鉴定出965个差异表达基因(DEGs)。GO富集分析结果表明,在真菌细胞壁组成方面有疏水蛋白相关的DEGs富集,其中AGABI2DRAFT_13655、AGABI2DRAFT_136569、AGABI2DRAFT_193057属于ABH3蛋白基因家族,在气生菌丝的表达水平显著高于贴生菌丝,可能与气生菌丝的产生有关。研究还发现了疏水表面结合蛋白A(HsbA)相关基因AGABI2DRAFT_194662在气生菌丝中FPKM表达水平为0,在贴生菌丝中为10.24。通过对DEGs进一步分析,富集到8个可能与脂酶同工酶相关的DEGs,气生菌丝中这些基因的表达水平显著高于贴生菌丝。SNP/InDel分析结果表明,As2796气生组SNP数为110 601,贴生组SNP数为111 188,单核苷酸变异中,C:G>T:A的变异次数较多,共筛选出2 374个共同InDel。
结论成功获得双孢蘑菇不同形态菌丝的转录组数据,并从中挖掘出潜在的相关基因和SNP位点,为双孢蘑菇相关分子标记开发及辅助育种提供参考。
Abstract:ObjectiveKey genes associated with Agaricus bisporus of different mycelial morphology were analyzed. [Methods] As 2796, the main cultivated variety of A. bisporus, with aerial or creepy hyphae grown on same plate were collected for RNA transcriptome sequencing and comparison with reference.
ResultsThere were 965 differentially expressed genes (DEGs) between the aerial hyphae-A601 and the creepy hyphae-A602. According to the GO enrichment analysis, the hydrophobic DEGs were enriched in the fungal cell wall, such as AGABI2DRAFT_13655, AGABI2DRAFT_136569, and AGABI2DRAFT_193057 that belonged to the ABH3 protein gene family, with expressions significantly higher in A601 than in A602. Thus, they were postulated to be related to the production of aerial hyphae. In addition, the hydrophobic surface binding protein A (HsbA)-related gene, AGABI2DRAFT_194662, showed a FPKM expression of 0 in A601, but 10.24 in A602. Furthermore, 8 enriched DEGs related to lipase isoenzymes exhibited a FPKM expression significantly higher in A601 than in A602. The SNP/InDel analysis indicated that the SNPs in A601 was 110 601 as opposed to 111 188 in A602, the most frequent mutation in SNPs was C:G>T:A, and that 2 374 common InDels were identified.
ConclusionThe transcriptomes and possibly associated genes and SNP sites in A. bisporus with different mycelial morphology obtained in this study would be of value for the mushroom germplasm evaluation and breeding.
-
0. 引言
【研究意义】 番鸭细小病毒病又称“番鸭三周病”,其病原是番鸭细小病毒(Muscovy duck parvovirus, MDPV)[1],仅侵害番鸭,感染鸭出现张口呼吸和腹泻等症状,病死鸭出现肺出血、胰腺出血或(和)白色坏死点、十二指肠黏膜出血。该病原主要引起3周龄内雏番鸭发病死亡[2]。2008年,在福建地区的雏半番鸭出现“短喙、生长迟缓”的疫病,通过对该类病例开展流行病学调查和病原学研究,确定其病原为与MDPV在基因组、感染宿主范围、抗原性和致病性上存在较大差异的新型番鸭细小病毒(New-genotype muscovy duck parvovirus, N-MDPV)[3]。在宿主选择上,该病毒不仅侵害番鸭,还侵害半番鸭和白改鸭;在致病性上,不仅引起经典番鸭细小病毒所致病变,还引起感染鸭短喙和生长迟缓,对我国养鸭业能造成巨大的危害以及经济损失。因此建立针对该病原的快速检测方法对疫病防控具有重要意义。【前人研究进展】 目前番鸭细小病毒病的检测方法有常规PCR法、荧光定量PCR法、环介导等温扩增(LAMP)法、分离鉴定法等。PCR与荧光定量PCR技术作为传统检测病原体的方法,能够在极低病原核酸量的情况下检测出疫病,从而作为常用的检测手段推广。但所需的仪器设备往往存在基层缺乏或过于贵重、不易操作等问题。LAMP检测方法则需要多对引物、更高的温度(63 ℃)和更长的运行时间[4],在基层实际中需要花费大量的时间与人力,也存在检测中由于气溶胶污染假阳性高等问题。重组酶聚合酶扩增(RPA)技术所需的酶主要是链置换 DNA 聚合酶、结合单链核酸的重组酶和单链结合蛋白,3种酶之间进行紧密合作能快速扩增目的片段,在常温条件下反应30 min即可完成对目的片段的扩增,在反应过程时模拟生物体内 DNA 复制流程,使反应更为精确稳定,操作简单便捷,尤其适用于基层[5]。在实地检测中使用冻干酶粉可以有效解决传统酶活性降解导致反应效率下降或气溶胶污染导致假阳性高等问题。目前,RPA 技术已经在多种病原的检测上得到了应用,如鸭腺病毒3型(DAdV-3)[6]、猪流行性腹泻病毒(Porcine epidemic diarrhea virus, PEDV)[7]、口蹄疫病毒(Foot-and-mouth disease virus, FMDV)[8]、非洲猪瘟病毒(Infection with african swine fever virus, ASFV)[9]等。RPA 扩增技术在37~42 ℃条件下进行核酸快速扩增,可在极短时间内观察到结果。极低核酸浓度下RPA体系仍能进行大量扩增,具有恒温、快速、便携、灵敏度高、特异性强和操作简单等优点[10],有较大的市场应用前景。【本研究切入点】 目前已有基于环介导等温扩增(LAMP)的番鸭细小病毒VP3高度保守基因的检测方法[4],说明以该基因作为检测靶标切实可行,但尚未见应用RPA 技术检测N-MDPV的报道。【拟解决的关键问题】本研究基于N-MDPV的VP3基因,建立荧光RPA检测方法,该方法可以应用于N-MDPV的大规模临床样本检测,为N-MDPV的快速检测提供技术支撑。
1. 材料与方法
1.1 试验材料
1.1.1 试验毒株
新型番鸭细小病毒 FJM3株(N-MDPV)、鸭腺病毒3型(Duck adenovirus type 3, DAdV-3)、禽腺病毒4型(Fowl adenovirus serotype 4, FAdV-4)、鸭圆环病毒(Duck circovirus, DuCV)、鸭瘟病毒(Duck plague virus, DPV)、鸭病毒性肝炎病毒(Duck hepatitis virus, DHV)、鸭坦布苏病毒(Duck tembusu virus, DTMUV)和新型鸭呼肠孤病毒(Novel duck reovirus, NDRV)均由福建省农业科学院禽病研究中心分离、鉴定和保存。
1.1.2 主要试剂
FJM3全基因组质粒[11];动物病毒DNA/RNA快速提取试剂盒5.0购自西安天隆科技有限公司;RPA引物购自生工生物工程(上海)股份有限公司;RPA扩增试剂及EXO探针购自深圳易致生物有限公司;核酸Marker DL2000购自Thermo(美国)公司;离心管购自Corning(美国)公司。
1.2 试验方法
1.2.1 荧光RPA 恒温检测引物和探针设计
在GenBank上查找N-MDPV 的VP3基因序列以供筛选,根据 RPA 引物设计原则,使用Primer premier 5.0设计N-MDPV VP3 基因的特异性引物和探针(表1),由上海生工生物工程技术有限公司合成。
表 1 N-MDPV的RPA引物和探针Table 1. RPA primers and probes of N-MDPV引物和探针
Primers and probes序列(5′-3′)
Sequence(5′-3′)N-MDPV-228F AGGCGCTTATGGCACCATGGGCCGCAATTGG N-MDPV-228R CCTAAAATATTTTGGGCTGGGATGCTGGAAG N-MDPV-193F ACTCACACAGAAGCAGAGGCTTCCAGCATCC N-MDPV-193R TAGTGTTTTGTTCATTCGTTACAGTCTTGCC N-MDPV-230R CCAAGAACATCAAGATCTGAACTCGTAGGAG N-MDPV-250R AAACCATTCCTGGTAAAGCTCCAAGAACATC N-MDPV-probe 5′ACAGATCTGGCAGCACTGCAGCAGGAATAA
AFGHQATTATGGTAACGGACG -C3 Spacer1.2.2 核酸的提取
使用动物病毒DNA/RNA快速提取试剂盒5.0(天隆科技,中国)提取N-MDPV、鸭腺病毒3型、禽腺病毒4型、圆环病毒、鸭瘟病毒、鸭病毒性肝炎病毒、鸭坦布苏病毒和新型鸭呼肠孤病毒的核酸,使用NanoDrop-2000分光光度计进行病毒核酸的浓度测定,为保证数值精确,重复3次取平均值。
1.2.3 RPA反应体系的建立
荧光 RPA恒温扩增反应体系为:Reaction Buffer(2×)10 μL,E-mix(2×)2 μL,P-mix(2×) 2 μL,探针(4 μmol·L−1)0.6 μL,上游引物(10 μmol·L−1)0.84 μL,下游引物(10 μmol·L−1) 0.84 μL,DNA模板 1 μL。加去离子水补齐至18 μL;最后向反应管盖内侧滴入2 μL激活剂,避免激活剂提前进入反应管内,否则会导致反应提前。轻弹数次混匀或者上下倒置甩混匀,瞬时离心,重复3次(需确保混匀,避免剧烈震荡涡旋),将反应管放入荧光仪中开始读数。反应时间30 min。
1.2.4 最优反应温度确定
共设 5个孵育温度:26、35、39、42、45 ℃。根据最优引物配置反应体系,配出5管完全相同的扩增试剂,在设计温度下孵育30 min后立即取出,在蓝光切胶仪下进行观察。
1.2.5 最优反应时间确定
共设5个孵育时间:10、20、30、40、50 min。配制相同的扩增试剂与阴性对照,置于确定的最优反应温度下, 按设计时间进行孵育,反应结束后立即取出。先完成反应的在–20 ℃下冻存,待全部处理完成反应后,在蓝光切胶仪下进行观察。
1.2.6 敏感性试验
为测定建立的检测方法的敏感性,将已构建的重组质粒进行连续的十倍倍比稀释,并以单个梯度稀释重组质粒作为检测方法敏感性试验的标准品。梯度稀释的重组质粒DNA作为反应模板,进行RPA反应扩增以确定该方法的最低检测核酸浓度。
1.2.7 特异性试验
以常见禽病的不同病原体基因组核酸作为模板进行扩增,验证检测方法的特异性。采用优化后的检测方法分别对鸭腺病毒3型、禽腺病毒4型、鸭圆环病毒、鸭瘟病毒、鸭病毒性肝炎病毒、鸭坦布苏病毒和新型鸭呼肠孤病毒进行DNA检测,加入去离子水的反应体系作为阴性对照,加入VP3阳性质粒的反应体系为阳性对照,根据检测结果检验该方法的特异性。
1.2.8 RPA和PCR的敏感性比较
对已建立的N-MDPV PCR检测方法与RPA检测方法进行敏感性比较。提取N-MDPV的基因组核酸,用去离子水进行十倍倍比稀释,采用两种检验方式进行测定,并依据所测定到的最低核酸扩增含量对比两种方式的灵敏度。
1.2.9 临床病料的检测
收集38份疑似组织、血液样本,使用核酸快速提取试剂盒提取核酸,利用建立的RPA方法、传统PCR方法和病毒分离鉴定法进行检测,分析3种方法的符合率。
2. 结果与分析
2.1 N-MDPV VP3 基因 RPA 扩增
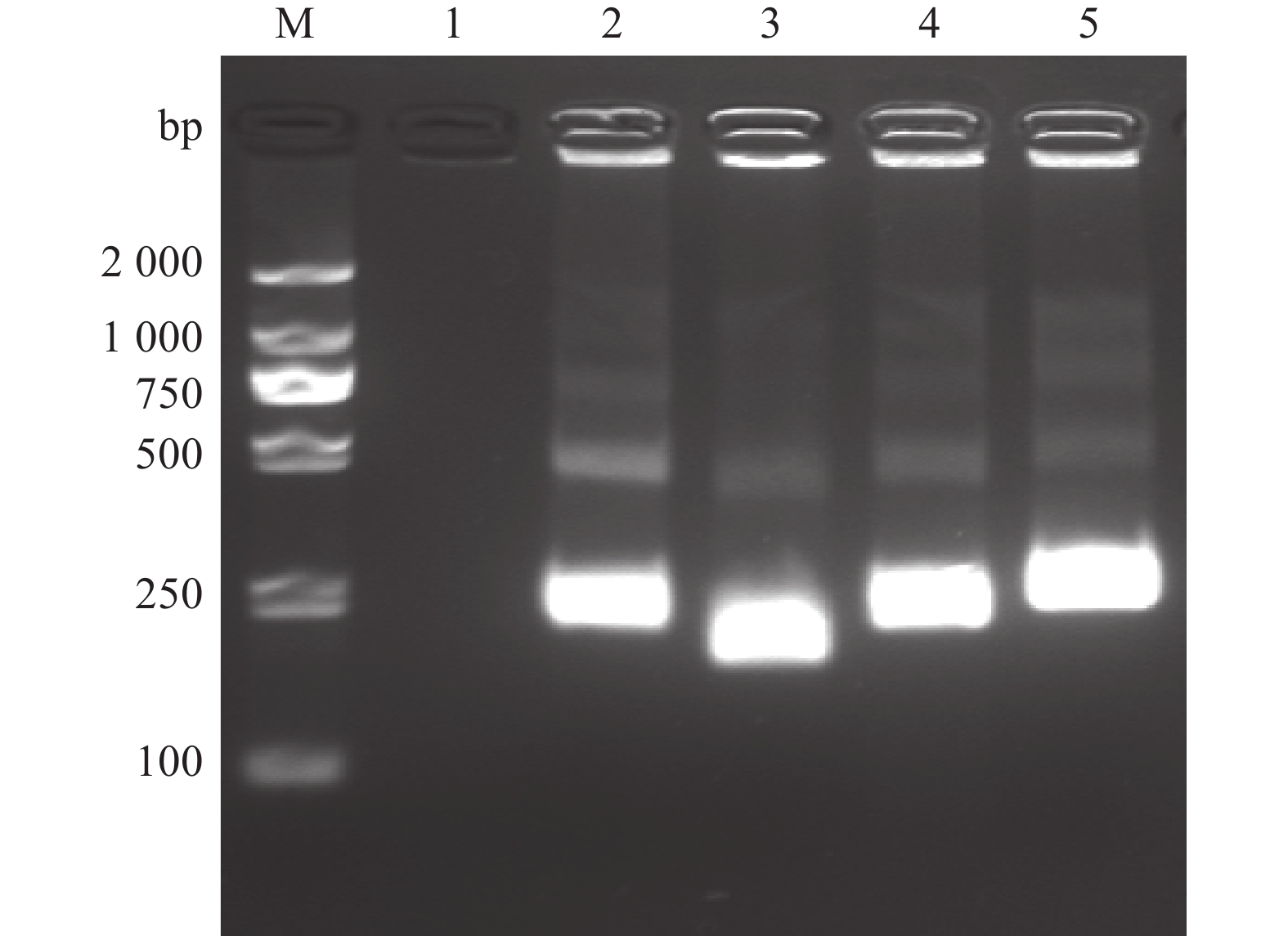
以ddH2O作为阴性对照,采用4对引物分别进行RPA扩增目的基因,并对扩增产物凝胶电泳成像(图1),结果显示阴性对照未见条带,RPA扩增技术成功扩增出目的基因,基因片段在193~250 bp,符合预期设计条带大小。
2.2 RPA扩增引物的筛选
如图2所示,所有设计的N-MDPV引物组合均有荧光,不同探针浓度对荧光效率存在影响,本研究发现4 μmol·L−1组的荧光效果相对较好,其中N- MDPV-193F和N-MDPV-250R组合所得的荧光效果最佳,且不同引物阴性对照未见荧光,故确定最佳引物组合为N-MDPV-193F和N-MDPV-250R。
![]() 图 2 N-MDPV荧光RPA检测不同引物扩增结果1~4(探针浓度4 μmol·L−1):N-MDPV-228F-228R、N-MDPV-193F-193R、N-MDPV-193F-230R、N-MDPV-193F-250R;5~8(探针浓度2 μmol·L−1):N-MDPV-228F-228R、N-MDPV-193F-193R、N-MDPV-193F-230R、N-MDPV-193F-250R;9~12(阴性对照):N-MDPV-228F-228R、N-MDPV-193F-193R、N-MDPV-193F-230R、N-MDPV-193F-250R。Figure 2. Amplification of primers of RPA for N-MDPV1–4 (with probe concentration at 4 μmol·L−1): N-MDPV-228F-228R, N-MDPV-193F-193R, N-MDPV-193F-230R, N-MDPV-193F-250R, respectively; 5–8 (with probe concentration at 2 μmol·L−1): N-MDPV-228F-228R, N-MDPV-193F-193R, N-MDPV-193F-230R, N-MDPV-193F-250R, respectively; 9–12 (negative control): N-MDPV-228F-228R, N-MDPV-193F-193R, N-MDPV-193F-230R, N-MDPV-193F-250R, respectively.
图 2 N-MDPV荧光RPA检测不同引物扩增结果1~4(探针浓度4 μmol·L−1):N-MDPV-228F-228R、N-MDPV-193F-193R、N-MDPV-193F-230R、N-MDPV-193F-250R;5~8(探针浓度2 μmol·L−1):N-MDPV-228F-228R、N-MDPV-193F-193R、N-MDPV-193F-230R、N-MDPV-193F-250R;9~12(阴性对照):N-MDPV-228F-228R、N-MDPV-193F-193R、N-MDPV-193F-230R、N-MDPV-193F-250R。Figure 2. Amplification of primers of RPA for N-MDPV1–4 (with probe concentration at 4 μmol·L−1): N-MDPV-228F-228R, N-MDPV-193F-193R, N-MDPV-193F-230R, N-MDPV-193F-250R, respectively; 5–8 (with probe concentration at 2 μmol·L−1): N-MDPV-228F-228R, N-MDPV-193F-193R, N-MDPV-193F-230R, N-MDPV-193F-250R, respectively; 9–12 (negative control): N-MDPV-228F-228R, N-MDPV-193F-193R, N-MDPV-193F-230R, N-MDPV-193F-250R, respectively.2.3 反应温度优化
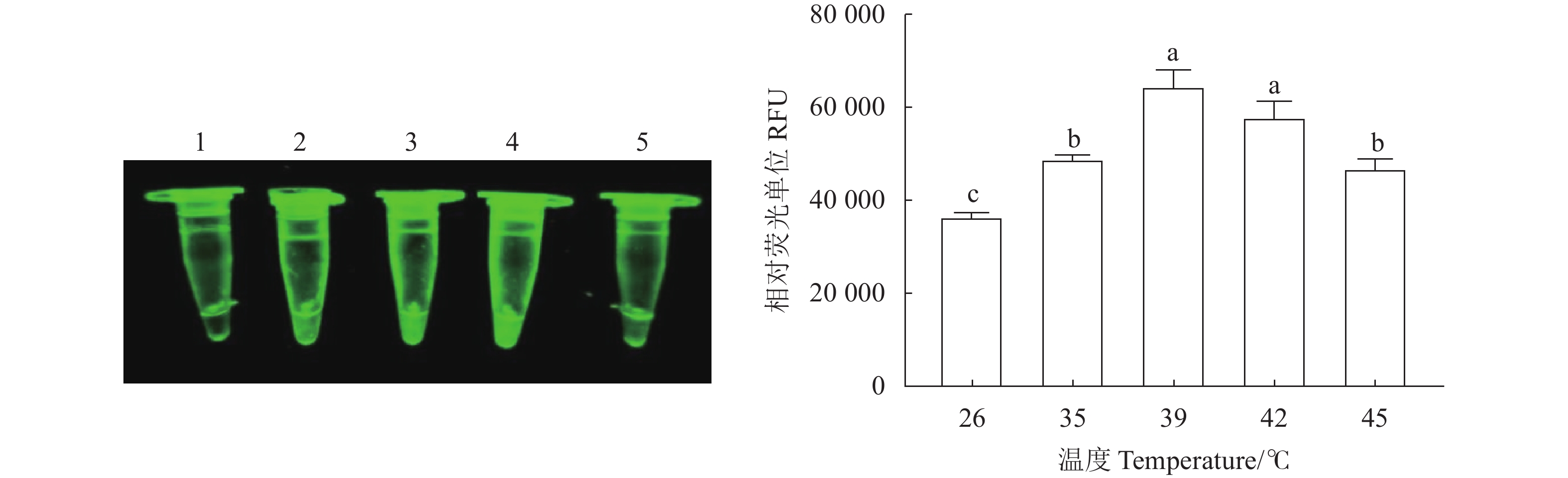
对N- MDPV RPA检测方法反应温度优化结果(图3)表明,反应温度26 ℃、35 ℃时荧光温度较弱,可能是酶在较低温度下活性不佳,45 ℃时荧光强度也见明显下降,可能是高温导致反应酶温度失活。39 ℃时反应荧光均值最高,为
63655 RFU(图3),故最佳反应温度确定为39 ℃。![]() 图 3 N- MDPV荧光RPA检测方法不同反应温度的扩增结果1~5分别为26、35、39、42、45 ℃。不同小写字母表示不同温度之间差异显著(P<0.05)。Figure 3. Amplifications at varied reaction temperature of RPA for N-MDPV1–5: 26, 35, 39, 42, and 45 ℃, respectively. Different lowercase letters indicate significant differences between different temperatures at P<0.05.
图 3 N- MDPV荧光RPA检测方法不同反应温度的扩增结果1~5分别为26、35、39、42、45 ℃。不同小写字母表示不同温度之间差异显著(P<0.05)。Figure 3. Amplifications at varied reaction temperature of RPA for N-MDPV1–5: 26, 35, 39, 42, and 45 ℃, respectively. Different lowercase letters indicate significant differences between different temperatures at P<0.05.2.4 反应时间优化
由图4可知,不同反应时间处理的扩增结果总体差异较小,但当反应时间超过30 min 后,可能由于出现非特异性扩增,反应体系的荧光强度随着时间的延长而下降。推测是反应时间过长导致反应体系内错配概率上升,引起大量非特异性扩增。由图4可知,在30 min 时反应体系的荧光值最高,均值达到
64071 RFU。由此确定最优反应时间为30 min,满足快速检测需求。2.5 敏感性试验结果
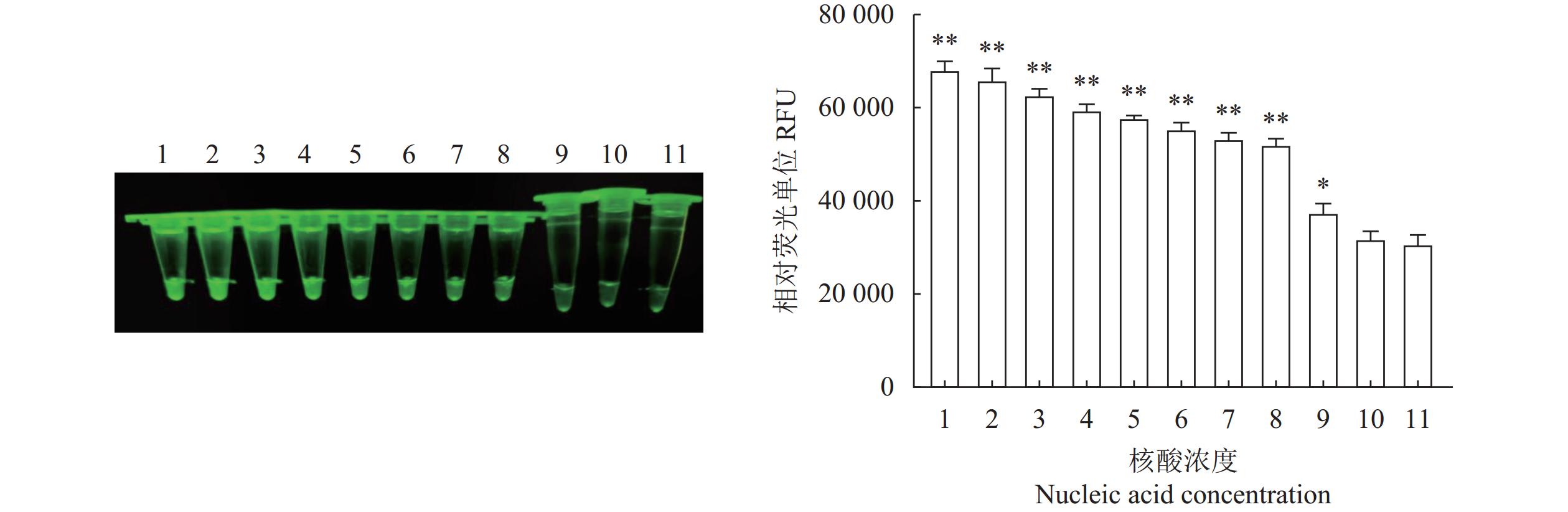
经测定,设计质粒浓度1 μg·μL−1,以10倍系列稀释成100 ng·μL−1、10 ng·μL−1、1 ng·μL−1、100 pg·μL−1、10 pg·μL−1、1 pg·μL−1、100 fg·μL−1、10 fg·μL−1、1 fg·μL−1 、1 ag·μL−1进行 RPA 敏感性试验,结果(图5)显示在10 fg·μL−1时还有较强荧光,在核酸浓度1 fg·μL−1时荧光强度呈现显著差异(图5),说明建立的荧光 RPA 检测方法最低检测限度为10 fg·μL−1 。
![]() 图 5 N-MDPV荧光RPA检测方法的敏感性1:100 ng·μL−1;2:10 ng·μL−1;3:1 ng·μL−1;4:100 pg·μL−1;5:10 pg·μL−1;6:1 pg·μL−1;7:100 fg·μL−1;8:10 fg·μL−1;9:1 fg·μL−1;10:1 ag·μL−1;11:阴性对照。*、**:与阴性对照相比,差异显著(P<0.05)或极显著(P<0.01)。Figure 5. Sensitivity of constant temperature fluorescent RPA assay1: 100 ng·μL−1; 2: 10 ng·μL−1; 3: 1 ng·μL−1; 4: 100 pg·μL−1; 5: 10 pg·μL−1; 6: 1 pg·μL−1; 7: 100 fg·μL−1; 8: 10 fg·μL−1; 9: 1 fg·μL−1; 10: 1 ag·μL−1; 11: negative control; * and **: significant difference from negative control at P<0.05 and extremely significant difference from negative control at P<0.01, respectively.
图 5 N-MDPV荧光RPA检测方法的敏感性1:100 ng·μL−1;2:10 ng·μL−1;3:1 ng·μL−1;4:100 pg·μL−1;5:10 pg·μL−1;6:1 pg·μL−1;7:100 fg·μL−1;8:10 fg·μL−1;9:1 fg·μL−1;10:1 ag·μL−1;11:阴性对照。*、**:与阴性对照相比,差异显著(P<0.05)或极显著(P<0.01)。Figure 5. Sensitivity of constant temperature fluorescent RPA assay1: 100 ng·μL−1; 2: 10 ng·μL−1; 3: 1 ng·μL−1; 4: 100 pg·μL−1; 5: 10 pg·μL−1; 6: 1 pg·μL−1; 7: 100 fg·μL−1; 8: 10 fg·μL−1; 9: 1 fg·μL−1; 10: 1 ag·μL−1; 11: negative control; * and **: significant difference from negative control at P<0.05 and extremely significant difference from negative control at P<0.01, respectively.2.6 特异性分析
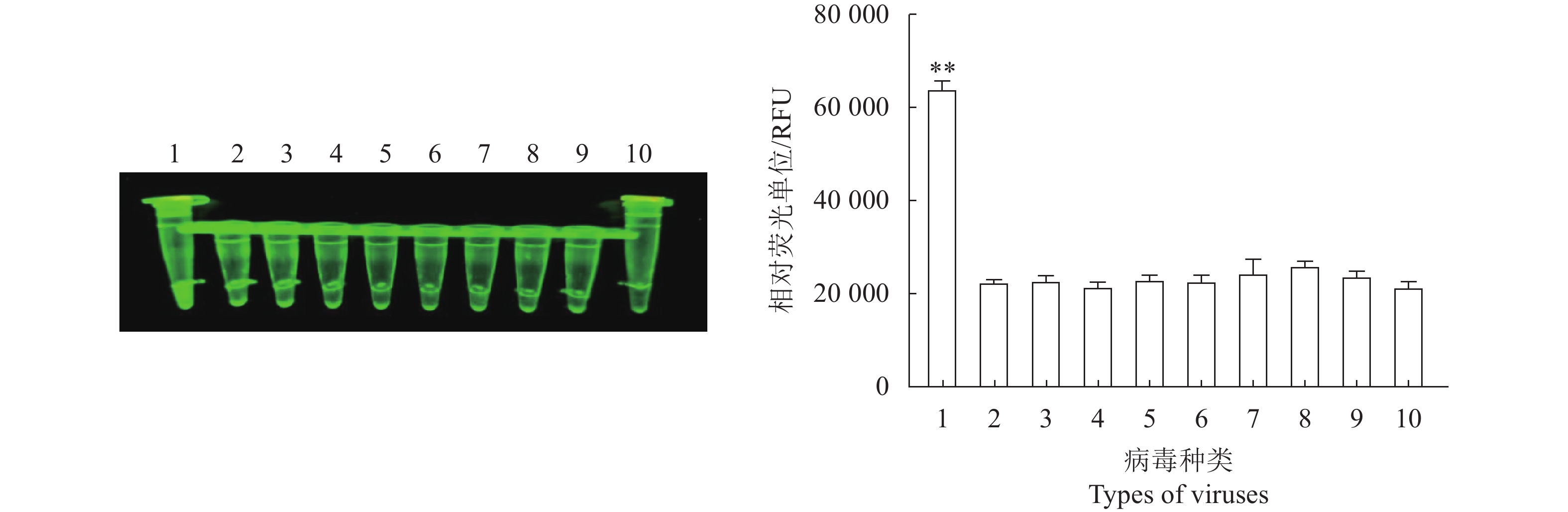
利用建立的RPA检测方法对不同病毒的核酸进行检测,并设置阴性对照。结果(图6)显示N-MDPV RPA检测方法只扩增出N-MDPV核酸,其他病毒的核酸和去离子水样品均为阴性,无交叉反应,图6显示以N-MDPV病毒质粒为模板的检测体系测得的荧光值与其他病毒样品有显著差异,说明该方法具有很好的特异性。
![]() 图 6 N- MDPV荧光RPA检测方法的特异性1:新型番鸭细小病毒;2:鸭腺病毒3型;3:禽腺病毒4型;4:鸭腺病毒3型+鸭坦布苏病毒;5:鸭瘟病毒;6:鸭病毒性肝炎病毒;7:鸭圆环病毒;8:鸭坦布苏病毒;9:新型鸭呼肠孤病毒;10:阴性对照。**:与阴性对照相比,差异极显著(P<0.01)。Figure 6. Specificity of constant temperature fluorescent RPA assay1: new-genotype muscovy duck parvovirus ; 2: duck adenovirus type 3; 3: fowl adenovirus serotype 4; 4: duck adenovirus type 3 + duck tembusu virus; 5: duck plague virus; 6: duck hepatitis virus; 7: duck circovirus; 8: duck tembusu virus; 9: novel duck reovirus; 10: negative control. **: extremely significant difference from negative control at P<0.01.
图 6 N- MDPV荧光RPA检测方法的特异性1:新型番鸭细小病毒;2:鸭腺病毒3型;3:禽腺病毒4型;4:鸭腺病毒3型+鸭坦布苏病毒;5:鸭瘟病毒;6:鸭病毒性肝炎病毒;7:鸭圆环病毒;8:鸭坦布苏病毒;9:新型鸭呼肠孤病毒;10:阴性对照。**:与阴性对照相比,差异极显著(P<0.01)。Figure 6. Specificity of constant temperature fluorescent RPA assay1: new-genotype muscovy duck parvovirus ; 2: duck adenovirus type 3; 3: fowl adenovirus serotype 4; 4: duck adenovirus type 3 + duck tembusu virus; 5: duck plague virus; 6: duck hepatitis virus; 7: duck circovirus; 8: duck tembusu virus; 9: novel duck reovirus; 10: negative control. **: extremely significant difference from negative control at P<0.01.2.7 RPA和PCR的敏感性对比
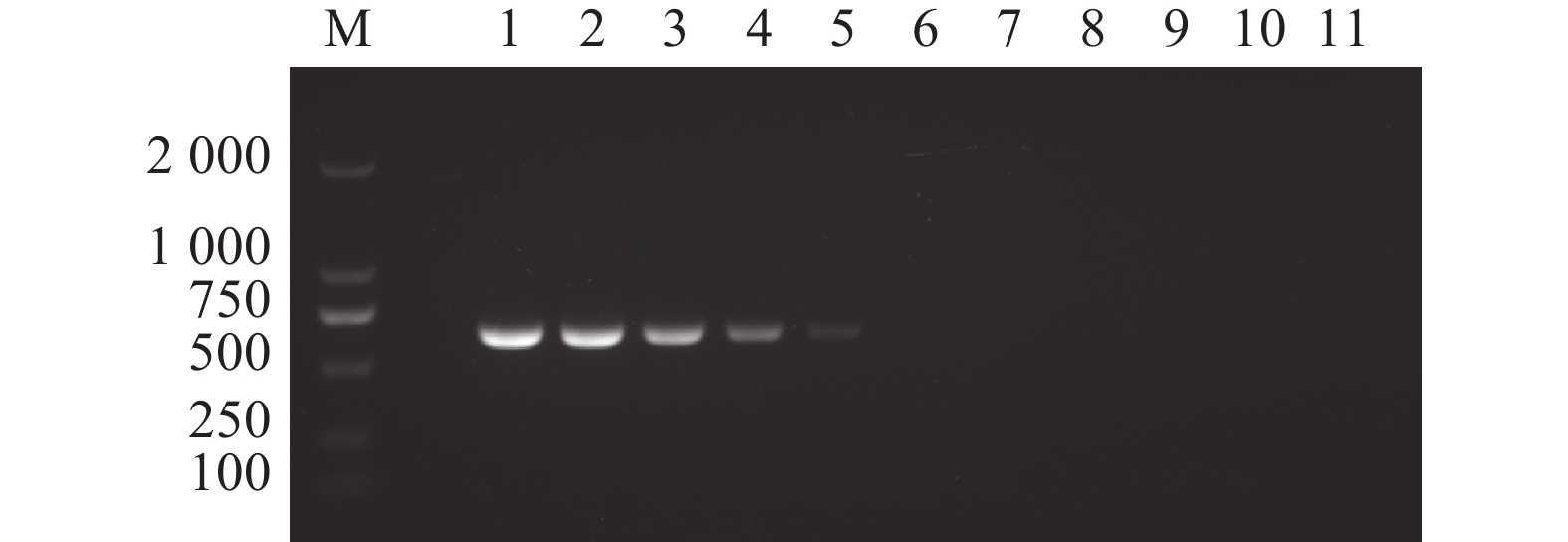
按照优化后的反应条件,同时使用PCR和RPA两种检测方法以相同稀释倍数的核酸作为模板进行检测对比。结果显示RPA检测方法较PCR检测方法的检测下限更低,PCR检测方法检测限为核酸稀释倍数10 pg·μL−1(图7),而RPA检测方法检测限为核酸稀释倍数10 fg·μL−1(图8)。
![]() 图 7 N-MDPV PCR 检测方法的敏感性M:DL 2000 DNA分子质量标准;1:100 ng·μL−1;2:10 ng·μL−1;3:1 ng·μL−1;4:100 pg·μL−1;5:10 pg·μL−1;6:1 pg·μL−1;7:100 fg·μL−1;8:10 fg·μL−1;9:1 fg·μL−1;10:1 ag·μL−1;11:阴性对照。Figure 7. Sensitivity of constant temperature fluorescent RPA assayM: DL 2000 DNA marker; 1: 100 ng·μL−1; 2: 10 ng·μL−1; 3: 1 ng·μL−1; 4: 100 pg·μL−1; 5: 10 pg·μL−1; 6: 1 pg·μL−1; 7: 100 fg·μL−1; 8: 10 fg·μL−1; 9: 1 fg·μL−1; 10: 1 ag·μL−1; 11: negative control.
图 7 N-MDPV PCR 检测方法的敏感性M:DL 2000 DNA分子质量标准;1:100 ng·μL−1;2:10 ng·μL−1;3:1 ng·μL−1;4:100 pg·μL−1;5:10 pg·μL−1;6:1 pg·μL−1;7:100 fg·μL−1;8:10 fg·μL−1;9:1 fg·μL−1;10:1 ag·μL−1;11:阴性对照。Figure 7. Sensitivity of constant temperature fluorescent RPA assayM: DL 2000 DNA marker; 1: 100 ng·μL−1; 2: 10 ng·μL−1; 3: 1 ng·μL−1; 4: 100 pg·μL−1; 5: 10 pg·μL−1; 6: 1 pg·μL−1; 7: 100 fg·μL−1; 8: 10 fg·μL−1; 9: 1 fg·μL−1; 10: 1 ag·μL−1; 11: negative control.![]() 图 8 N-MDPV荧光RPA检测方法的敏感性1:100 ng·μL−1;2:10 ng·μL−1;3:1 ng·μL−1;4:100 pg·μL−1;5:10 pg·μL−1;6:1 pg·μL−1;7:100 fg·μL−1;8:10 fg·μL−1;9:1 fg·μL−1;10:1 ag·μL−1;11:阴性对照。*、**:与阴性对照相比,差异显著(P<0.05)或极显著(P<0.01)。Figure 8. Sensitivity of constant temperature fluorescent RPA assay1: 100 ng·μL−1; 2: 10 ng·μL−1; 3: 1 ng·μL−1; 4: 100 pg·μL−1; 5: 10 pg·μL−1; 6: 1 pg·μL−1; 7: 100 fg·μL−1; 8: 10 fg·μL−1; 9: 1 fg·μL−1; 10: 1 ag·μL−1; 11: negative control; * and **: significant difference from negative control at P<0.05 and extremely significant difference from negative control at P<0.01. respectively.
图 8 N-MDPV荧光RPA检测方法的敏感性1:100 ng·μL−1;2:10 ng·μL−1;3:1 ng·μL−1;4:100 pg·μL−1;5:10 pg·μL−1;6:1 pg·μL−1;7:100 fg·μL−1;8:10 fg·μL−1;9:1 fg·μL−1;10:1 ag·μL−1;11:阴性对照。*、**:与阴性对照相比,差异显著(P<0.05)或极显著(P<0.01)。Figure 8. Sensitivity of constant temperature fluorescent RPA assay1: 100 ng·μL−1; 2: 10 ng·μL−1; 3: 1 ng·μL−1; 4: 100 pg·μL−1; 5: 10 pg·μL−1; 6: 1 pg·μL−1; 7: 100 fg·μL−1; 8: 10 fg·μL−1; 9: 1 fg·μL−1; 10: 1 ag·μL−1; 11: negative control; * and **: significant difference from negative control at P<0.05 and extremely significant difference from negative control at P<0.01. respectively.2.8 临床病料的检测结果
对收集的38个临床样本采用已建立的RPA方法、常规PCR方法和病毒分离鉴定法同时进行检测,结果显示(表2),RPA 方法N-MDPV阳性率为 36.8%(14/38),病毒分离鉴定法检测N-MDPV阳性率为 31.6%(12/38),PCR方法检测N-MDPV阳性率为36.8%(14/38)。其中,病毒分离鉴定法的12份阳性样品与常规 PCR 法检测出的14份阳性样品与 RPA 检测的14份阳性样品结果一致,均来自同一份临床样品。表明建立的 RPA 方法与常规PCR方法的检测结果完全相同,可在基层应用于N- MDPV的检测。
表 2 N-MDPV RPA 与 PCR 方法、病毒分离法临床样本检测结果比较Table 2. Comparison between detections by constant temperature fluorescent RPA assay and PCR on clinical samples检测方法
Detecting
Method样品数
No. of
samples阳性样品数
No. of
positive阴性样品数
No. of
negative阳性率
Positive
rate%RPA恒温检测
RPA constant
temperature detection38 14 24 36.8 常规 PCR
Conventional PCR38 14 24 36.8 病毒分离鉴定法
Virus isolation and
identification method38 12 26 31.6 3. 讨论
RPA 是近年来新兴的一种常温扩增技术,检测原理是在扩增目的靶标片段过程中,重组酶与引物结合形成的复合物与DNA结合,并沿核酸链寻找同源序列,引物定位同源序列后,发生链交换反应形成并启动 DNA 合成,采用的扩增酶在一定条件温度下就具有核酸扩增作用。相较于PCR等现有分子诊断技术,RPA恒温扩增具有以下优点:首先,RPA 快速检测方法对于温度的要求并不苛刻,在偏远地区有便携式发热设备即可开展检测,在不具备昂贵设备的基层环境具有明显优势,成本相对较低。其次,RPA试剂使用冻干粉的形式制备,可长期在室温下保存且不失去活性,与其他液体试剂相比,反应体系于一管内配置不易受气溶胶污染且稳定。第三,PCR 扩增时核苷酸的非正常配对会导致探针失效或失去灵敏度,最终导致检测结果不理想,RPA扩增反应则容许微量错配,不影响最终结果。因此RPA具有良好的应用前景。
得益于酶体系和单链结合蛋白的协作,RPA无需变性即可在常温条件下快速扩增目标序列,相较于PCR也具有更好的扩增敏感性。在此基础上,荧光探针法RPA加入了EXO酶和EXO荧光探针,酶对底物的识别与切割保证了反应的特异性。本研究针对N-MDPV保守性序列VP3设计多对引物,通过试验筛选到最佳扩增引物对,并优化反应温度和反应时间,最佳反应条件为39 ℃孵育30 min。在灵敏性方面,本研究建立的RPA检测方法最低检测核酸限度可达10 fg·μL−1,相较常规PCR敏感性提高了100倍[12]。该方法特异性强,与鸭腺病毒3型(DAdV-3)、禽腺病毒4型(FAdV-4)、鸭圆环病毒(DuCV)、鸭瘟病毒(DPV)、鸭病毒性肝炎病毒(DHV)、鸭坦布苏病毒(DTMUV)和新型鸭呼肠孤病毒(NDRV)均无交叉反应。临床病料RPA检测结果与PCR方法的阳性检出率完全一致,高于病毒分离鉴定法。此外,与LAMP检测方法相比,RPA 检测方法仅需要一对引物和一个探针,操作简单便捷快速,有效填补了LAMP检测技术假阳性高的问题,为基层快检提供了新的技术[4]。该方法在基层检测试验流程可控制在1 h内,相较LAMP检测时间缩短一半以上,更加方便快捷。随着生物制造产业的不断发展,引物探针和试剂生产成本的下降,该类技术必然会得到更大的推广与应用。
综上所述,本研究成功建立了一种N-MDPV的RPA恒温检测方法,对N-MDPV现场检测试剂盒的开发和疫病防控具有重要意义。
-
表 1 样品测序数据及与参考基因组的序列比对结果
Table 1 Statistics of experimental data and alignment with reference on genome sequences
编号
ID样品
Sample总Read数
Total clean reads比对到参考基因组的Reads数目
Mapped reads比对到参考基因组的Reads百分比
Mapped reads/%GC含量
GC content/%≥Q30的百分比
≥Q30/%A601 As2796气生菌丝 42 155 674 25 410 008 60.28 49.12 92.00 A602 As2796贴生菌丝 45 225 288 28 324 702 62.63 49.28 92.37 表 2 新基因功能注释结果统计
Table 2 Number of new genes with functional annotation
用于功能注释的数据库
Annotated database获得注释的新基因数目
Annotated gene number长度在≥300~ 1000 的新基因数目
Gene number (300≤gene length<1000 )长度≥ 1000 的新基因数目
Gene number (gene length≥1000 )COG 15 12 3 GO 21 13 7 KEGG 38 21 14 KOG 20 12 8 Pfam 34 20 12 Swissprot 24 15 8 nr 132 70 57 All 139 76 57 表 3 部分差异表达基因
Table 3 Partial DEGs
编号
No.基因ID
Gene ID相对表达量FPKM
Relative expression FPKMLog2FC Pfam蛋白注释
Pfam protein annotation基因注释
Gene annotationA601 A602 1 AGABI2DRAFT_194497 15.6653 0.0000 −6.78 — — 2 AGABI2DRAFT_177536 20.5777 0.0000 −4.47 — 假设蛋白OH76DRAFT_1359727 3 AGABI2DRAFT_120985 1.0452 0.0000 −3.64 — 假设蛋白AN958_00580 4 AGABI2DRAFT_203489 2.3380 0.0001 −3.85 — 假设蛋白 AN958_02967 5 AGABI2DRAFT_44066 6.2585 0 −3.75 HhH-GPD超家族碱基
切除DNA修复蛋白假设蛋白 AN958_02739 6 AGABI2DRAFT_113583 0.0000 4.2489 4.73 — 假设蛋白 AN958_04089 7 AGABI2DRAFT_117617 0.0008 6.9437 3.30 — 假设蛋白 AN958_03520 8 AGABI2DRAFT_179131 0.0010 2.5569 4.28 — 假设蛋白 AN958_00324 9 AGABI2DRAFT_194662 0 10.2374 4.66 疏水表面结合蛋白A 假设蛋白AN958_09554 10 AGABI2DRAFT_136569 196.301 32.0293 −2.58 真菌疏水蛋白 假定的疏水蛋白 [双孢蘑菇] 11 AGABI2DRAFT_193057 999.26 189.163 −2.38 真菌疏水蛋白 假定的疏水蛋白 [双孢蘑菇] 12 AGABI2DRAFT_136557 19733 3086.17 −2.67 真菌疏水蛋白 假定的疏水蛋白 [双孢蘑菇] 13 AGABI2DRAFT_143464 100.031 896.356 3.21 真菌疏水蛋白 假定的疏水蛋白 [双孢蘑菇] 14 AGABI2DRAFT_178707 31.7555 666.848 4.35 真菌疏水蛋白 假定的疏水蛋白 [双孢蘑菇] 表 5 SNP突变统计表
Table 5 SNP mutation statistics
编号 ID T∶A>G∶C C∶G>G∶C T∶A>A∶T C∶G>T∶A C∶G>A∶T T∶A>C∶G 转化 Ts 颠换 Tv 转换/颠换比 ts/tv A601 6312 5221 7641 42864 6405 42158 85022 25579 3.32 A602 6276 5239 7586 43273 6338 42476 85749 25439 3.37 表 6 全基因组和编码区InDel长度分布表
Table 6 Length distribution of genome-wide and coding region InDel sites
编号
ID区域
Region−10 −9 −8 −7 −6 −5 −4 −3 −2 −1 1 2 3 4 5 6 7 8 9 10 A601 基因组
Genome11 2 0 0 1 2 0 6 106 1235 1559 121 1 0 0 2 0 0 0 0 A601 外显子
Exonic7 1 0 0 1 0 0 3 2 99 221 14 1 0 0 2 0 0 0 0 A602 基因组
Genome14 3 0 0 1 2 0 11 100 1080 1434 121 3 0 0 3 0 0 0 0 A602 外显子
Exonic9 1 0 0 1 0 0 7 2 100 229 15 3 0 0 3 0 0 0 0 -
[1] BERNAŚ E, JAWORSKA G. Vitamins profile as an indicator of the quality of frozen Agaricus bisporus mushrooms [J]. Journal of Food Composition and Analysis, 2016, 49: 1−8. DOI: 10.1016/j.jfca.2016.03.002
[2] OWAID M N, BARISH A, ALI SHARIATI M. Cultivation of Agaricus bisporus (button mushroom) and its usages in the biosynthesis of nanoparticles [J]. Open Agriculture, 2017, 2(1): 537−543. DOI: 10.1515/opag-2017-0056
[3] MUSZYŃSKA B, KAŁA K, ROJOWSKI J, et al. Composition and biological properties of Agaricus bisporus fruiting bodies- a review [J]. Polish Journal of Food and Nutrition Sciences, 2017, 67(3): 173−181. DOI: 10.1515/pjfns-2016-0032
[4] 王翠, 郭仲杰, 尤洁, 等. 双孢蘑菇产、质量性状相关分子标记的初步研究 [J]. 福建农业科技, 2018, 49(7):1−5. WANG C, GUO Z J, YOU J, et al. A preliminary study on molecular markers related to yield and quality traits of Agaricus bisporus [J]. Fujian Agricultural Science and Technology, 2018, 49(7): 1−5. (in Chinese)
[5] DAS B, DE B, CHETREE R, et al. Medicinal aspect of mushrooms: A view point[J]. Herbal Medicine in India: Indigenous Knowledge, Practice, Innovation and its Value, 2020: 509-532.
[6] ZHANG M, ZHAO L, TANG F, et al. Chemical structures, biological activities, and biosynthetic analysis of secondary metabolites from Agaricus mushrooms: A review [J]. Journal of Agricultural and Food Chemistry, 2024, 72(22): 12387−12397. DOI: 10.1021/acs.jafc.4c01861
[7] 柯斌榕, 兰清秀, 卢政辉, 等. 福建省双孢蘑菇栽培技术的变革与发展 [J]. 食药用菌, 2017, 25(1):12−19. KE B R, LAN Q X, LU Z H, et al. Innovation and development of Agaricus bisporus cultivation techniques in Fujian province [J]. Edible and Medicinal Mushrooms, 2017, 25(1): 12−19. (in Chinese)
[8] 林杰, 林莫翎. 蘑菇异型菌丝与栽培技术的相关性 [J]. 福建农业, 2007(11):20−21. LIN J, LIN M L. Correlation between heteromorphic hyphae of mushrooms and cultivation techniques [J]. Fujian Agriculture, 2007(11): 20−21. (in Chinese)
[9] 詹才新, 凌霞芬. 双孢蘑菇菌落形态和产质量性状间相关性研究 [J]. 食用菌学报, 1997, 4(3):7−12. ZHAN C X, LING X F. Studies on correlation between colonial morphology and characters of productivity and quality of Agaricus bisporus [J]. Acta Edulis Fungi, 1997, 4(3): 7−12. (in Chinese)
[10] 李洪荣. 双孢蘑菇不同菌落形态的同工酶分析 [J]. 福建轻纺, 2011(4):43−45. LI H R. Isozyme analysis of different colony morphology of Agaricus bisporus [J]. The Light & Textile Industries of Fujian, 2011(4): 43−45. (in Chinese)
[11] CAI Z X, CHEN M Y, LU Y P, et al. Metabolomics and transcriptomics unravel the mechanism of browning resistance in Agaricus bisporus [J]. PLoS One, 2022, 17(3): e0255765. DOI: 10.1371/journal.pone.0255765
[12] LU Y P, GUO Z J, KE B R, et al. Genome-wide association study and transcriptome analysis provide candidate genes for agronomic traits of Agaricus bisporus [J]. Horticulturae, 2024, 10(7): 691. DOI: 10.3390/horticulturae10070691
[13] YANG X M, YANG K X, WANG X H, et al. Transcriptomic analysis reveals the mechanism of bacterial disease resistance of postharvest button mushroom (Agaricus bisporus) [J]. Physiological and Molecular Plant Pathology, 2022, 122: 101903. DOI: 10.1016/j.pmpp.2022.101903
[14] 秦煜, 郑向丽, 林钟员. 基于转录组测序的红萍SSR和SNP特征分析 [J]. 福建农业科技, 2023, 54(6):44−48. QIN Y, ZHENG X L, LIN Z Y. Characteristic analysis of SSR and SNP in Azolla imbircata based on transcriptome sequencing [J]. Fujian Agricultural Science and Technology, 2023, 54(6): 44−48. (in Chinese)
[15] 陈美元. 双孢蘑菇As2796全长cDNA文库的构建及鉴定 [J]. 福建农业学报, 2012, 27(11):1201−1204. CHEN M Y. Construction and identification of full-length cDNA library of Agaricus bisporus As2796 [J]. Fujian Journal of Agricultural Sciences, 2012, 27(11): 1201−1204. (in Chinese)
[16] 王泽生. 蘑菇杂交株As2796的种性与栽培技术要点 [J]. 食用菌, 1993, 15(5):9. WANG Z S. Characteristics and cultivation techniques of mushroom hybrid strain As2796 [J]. Edible Fungi, 1993, 15(5): 9. (in Chinese)
[17] KIM D, PERTEA G, TRAPNELL C, et al. TopHat2: Accurate alignment of transcriptomes in the presence of insertions, deletions and gene fusions [J]. Genome Biology, 2013, 14(4): R36. DOI: 10.1186/gb-2013-14-4-r36
[18] 顾鑫, 杨晓贺, 姚亮亮, 等. 大豆灰斑病菌Race15的全基因组测序分析 [J]. 大豆科学, 2021, 40(4):466−475. GU X, YANG X H, YAO L L, et al. Whole-genome sequencing and analysis of Cercospora sojina race 15 [J]. Soybean Science, 2021, 40(4): 466−475. (in Chinese)
[19] JIANG H, WONG W H. Statistical inferences for isoform expression in RNA-Seq [J]. Bioinformatics, 2009, 25(8): 1026−1032. DOI: 10.1093/bioinformatics/btp113
[20] ANDERS S, HUBER W. Differential expression analysis for sequence count data[J]. Nature Precedings, 2010.
[21] MCKENNA A, HANNA M, BANKS E, et al. The Genome Analysis Toolkit: A MapReduce framework for analyzing next-generation DNA sequencing data [J]. Genome Research, 2010, 20(9): 1297−1303. DOI: 10.1101/gr.107524.110
[22] WANG K, LI M, HAKONARSON H. ANNOVAR: Functional annotation of genetic variants from next-generation sequencing data Nucleic Acids Research[J]. ANNOVAR: Functional annotation of genetic variants from next-generation sequencing data Nucleic Acids Research, 2010: 38.
[23] 王秉峰. 匍匐型与气生型双孢蘑菇菌株品比试验 [J]. 中国食用菌, 2010, 29(5):19−20. WANG B F. The comparison test of different strains of prostrate and aerial-type Agaricus bisporas [J]. Edible Fungi of China, 2010, 29(5): 19−20. (in Chinese)
[24] WANG H C, WANG Z S. The prediction of strain characteristecs of Agaricus bisporus by the application of isozyme electrophoresis [J]. Fujian Mushroom, 1991(1): 38−48. (in Chinese).
[25] WANG Z S, WANG H C. Isozyme patterns and characteristics of hybrid strains of Agaricus bisporus [J]. Microl. Neotrop. Apl, 1990(3): 19−29.
[26] 金建康, 徐鹤林. 双孢蘑菇气生型与匍匐型的比较研究 [J]. 中国食用菌, 1990, 9(5):3−4. JIN J K, XU H L. Comparative study on aerial type and creeping type of Agaricus bisporus [J]. Edible Fungi of China, 1990, 9(5): 3−4. (in Chinese)
[27] 杜炫星, 牛敏敏, 赵清, 等. 李白盾蚧转录组分析及 SSR 位点开发 [J]. 环境昆虫学报, 2023, 45(5):1318−1332. DU X X, NIU M M, ZHAO Q, et al. Analysis of the transcriptome and development of SSR Loci in Pseudaulacaspis prunicola (Maskell) [J]. Journal of Environmental Entomology, 2023, 45(5): 1318−1332. (in Chinese).
[28] MORIN E, KOHLER A, BAKER A R, et al. Genome sequence of the button mushroom Agaricus bisporus reveals mechanisms governing adaptation to a humic-rich ecological niche [J]. Proceedings of the National Academy of Sciences of the United States of America, 2012, 109(43): 17501−17506.
[29] LINDER M B, SZILVAY G R, NAKARI-SETÄLÄ T, et al. Hydrophobins: The protein-amphiphiles of filamentous fungi [J]. FEMS Microbiology Reviews, 2005, 29(5): 877−896. DOI: 10.1016/j.femsre.2005.01.004
[30] LUGONES L G, BOSSCHER J S, SCHOLTMEYER K, et al. An abundant hydrophobin (ABH1) forms hydrophobic rodlet layers in Agaricus bisporus fruiting bodies[J]. Microbiology, 1996, 142 ( Pt 5): 1321-1329.
[31] LUGONES L G, WÖS H A B, WESSELS J G H. A hydrophobin (ABH3) specifically secreted by vegetatively growing hyphae of Agaricus bisporus (common white button mushroom)[J]. Microbiology, 1998, 144 ( Pt 8): 2345-2353.
[32] OHTAKI S, MAEDA H, TAKAHASHI T, et al. Novel hydrophobic surface binding protein, HsbA, produced by Aspergillus oryzae [J]. Applied and Environmental Microbiology, 2006, 72(4): 2407−2413. DOI: 10.1128/AEM.72.4.2407-2413.2006
[33] 张烨. 球孢白僵菌疏水表面结合蛋白HsbA的克隆及功能研究[D]. 北京: 中国农业科学院, 2013 ZHANG Y. cDNA clone and functional research on hydrophobic surface binding protein HsbA in Beauveria bassiana [D]. Beijing: Chinese Academy of Agricultural Sciences, 2013. (in Chinese)
[34] PARK J, LEE S, CHOI J, et al. Fungal cytochrome P450 database [J]. BMC Genomics, 2008, 9: 402. DOI: 10.1186/1471-2164-9-402
[35] HLAVICA P. Evaluation of structural features in fungal cytochromes P450 predicted to rule catalytic diversification [J]. Biochimica et Biophysica Acta, 2013, 1834(1): 205−220. DOI: 10.1016/j.bbapap.2012.09.012
[36] SMIDA A D, VALDERRAMA X P, AGOSTINI M C, et al. Cadmium stimulates transcription of the cytochrome p450 side chain cleavage gene in genetically modified stable porcine granulosa cells [J]. Biology of Reproduction, 2004, 70(1): 25−31. DOI: 10.1095/biolreprod.103.019000
[37] ZHANG M, LIU X C, YUAN L Y, et al. Transcriptional profiling in cadmium-treated rice seedling roots using suppressive subtractive hybridization [J]. Plant Physiology and Biochemistry, 2012, 50: 79−86. DOI: 10.1016/j.plaphy.2011.07.015
[38] WANG L L, LI H B, WEI H L, et al. Identification of cadmium-induced Agaricus blazei genes through suppression subtractive hybridization [J]. Food and Chemical Toxicology, 2014, 63: 84−90. DOI: 10.1016/j.fct.2013.10.036
[39] 宋媛, 胡秋辉, 苏安祥, 等. 转录组学解析茉莉酸甲酯对双孢蘑菇个体大小的影响机制 [J]. 食品科学, 2021, 42(4):130−137. SONG Y, HU Q H, SU A X, et al. Transcriptomic analysis of the mechanism underlying the effect of methyl jasmonate on the size of Agaricus bisporus [J]. Food Science, 2021, 42(4): 130−137. (in Chinese)
[40] 刘俊敏. 镉胁迫对双孢蘑菇抗氧化系统的影响及耐受性相关基因的筛选与鉴定[D]. 厦门: 厦门大学, 2018. LIU J M. Cadmium stress on the effect of antioxidant system in Agaricus bisporus and the identification of differentially expressed genes [D]. Xiamen: Xiamen University, 2018. (in Chinese)
[41] XU K H, ZHAO Y, ZHAO Y, et al. Soybean F-box-like protein GmFBL144 interacts with small heat shock protein and negatively regulates plant drought stress tolerance [J]. Frontiers in Plant Science, 2022, 13: 823529. DOI: 10.3389/fpls.2022.823529
[42] MÜLLER-STARCK G. Isozymes[M]//Molecular Tools for Screening Biodiversity. Dordrecht: Springer Netherlands, 1998: 75-81.
[43] 时如霞, 曾琴, 赵丹. 基于楠木转录组的SSR、SNP、Indel分子标记技术特征分析 [J]. 山地农业生物学报, 2023, 42(4):83−87. SHI R X, ZENG Q, ZHAO D. SSR, SNP and InDel characterization of Phoebe zhennan based on the transcriptome sequence [J]. Journal of Mountain Agriculture and Biology, 2023, 42(4): 83−87. (in Chinese)
[44] 贾定洪, 王波, 何晓兰, 等. 基于基因组重测序发掘金针菇 InDel, SV 及丰度 SNP 标记 [J]. 菌物学报, 2024, 43(7):230228. JIA D H, WANG B, HE X L, et al. Exploitation of InDel, SV and abundance SNP markers in Flammulina filiformis based on genome resequencing [J]. Mycosystema, 2024, 43(7): 23022. (in Chinese).
[45] 施肖堃, 蔡志欣, 郭仲杰, 等. 18个双孢蘑菇核心种质的重测序初步分析 [J]. 福建农业学报, 2019, 34(10):1167−1172. SHI X K, CAI Z X, GUO Z J, et al. A preliminary report on resequencing 18 representative strains of Agaricus bisporus [J]. Fujian Journal of Agricultural Sciences, 2019, 34(10): 1167−1172. (in Chinese).
-
期刊类型引用(2)
1. 赵卓,刘晨阳,瓮青芬,王保海,翟卿. 茶六斑褐锦斑蛾Sorita pulchella线粒体基因组特征与系统发育分析. 河南农业大学学报. 2023(02): 277-287 .  百度学术
百度学术
2. 韦春梦,陈亚珍,刘静,邓维安,李晓东. 云南瘤蚱线粒体基因组特征与蚱总科系统发育分析. 南方农业学报. 2023(05): 1303-1316 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载: