Optimizing Culture Medium and Antioxidant Activity of Extracellular Polysaccharides in Liquid Fermentation of Flammulina velutipes
-
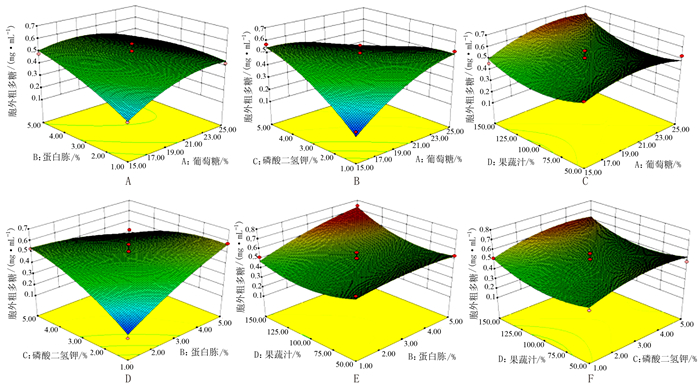
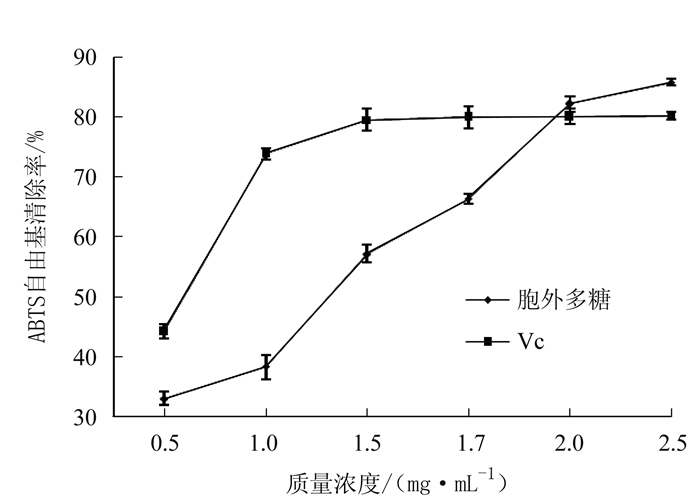
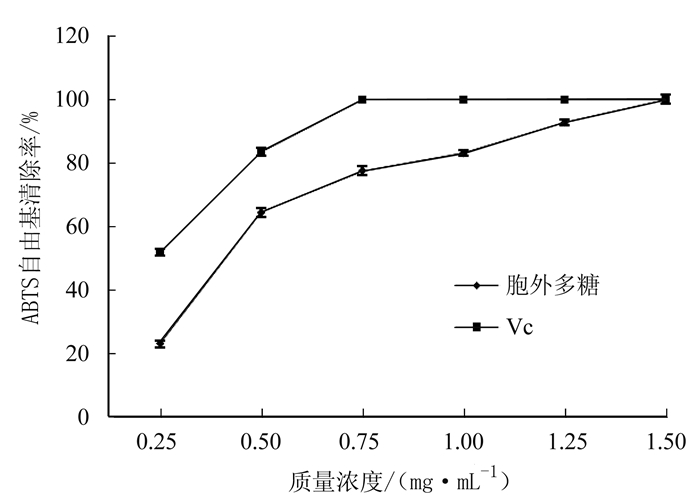
摘要: 应用响应面分析法考查葡萄糖、蛋白胨、KH2PO4、果蔬汁用量对金针菇液体发酵胞外多糖的影响,分析胞外多糖抗氧化活性。试验结果表明,对金针菇胞外多糖影响大小依次为:蛋白胨> KH2PO4 >果蔬汁>葡萄糖,所确定的最优培养基质量分数为:葡萄糖2.46%,蛋白胨0.5%,KH2PO4 0.1%,果蔬汁15%,在此条件下胞外多糖质量浓度为0.83 mg·mL-1。通过测定金针菇液体发酵胞外多糖的抗氧化活性,证明金针菇胞外多糖对DPPH自由基和ABTS自由基都具有较强的清除作用,当胞外多糖质量浓度大于2 mg·mL-1时,其对DPPH自由基的清除率相比同质量浓度下的Vc要高;当胞外多糖质量浓度大于1.5 mg·mL-1时,其对ABTS自由基的清除率与同质量浓度下的Vc的清除率相近,达到99.87%。Abstract: A response surface experiment was conducted to optimize the fermentation of Flammulina velutipes for the extracellular polysaccharides (EPS). Liquid media with varied amounts of glucose, peptone, KH2PO4, fruit and vegetable juices were used for the experimentation. At end of the process, the antioxidant activity of EPS in each liquid suspension was determined as the criterion for optimization. The results showed that (a) the effect of ingredients in medium on the antioxidant activity ranked as peptone > KH2PO4 > fruit/vegetable juices > glucose; (b) the medium containing 2.46% glucose, 0.5% peptone, 0.1% KH2PO4 and 15% fruit/vegetable juices produced the highest EPS in the suspension at 0.83 mg·mL-1; (c) at concentrations exceeding 2 mg·mL-1, EPS obtained from the fermentation exhibited a strong scavenging effect on DPPH and ABTS free radicals; (d) at a same concentration level, EPS had a greater DPPH free radical scavenging rate than Vc; and, (e) at concentrations higher than 1.5 mg·mL-1, EPS exhibited a scavenging rate on ABTS free radicals similar to Vc, reaching 99.87%.
-
0. 引言
【研究意义】猪是重要的经济畜禽之一,而脂肪沉积是影响猪肉质量和风味等的关键因素之一[1]。脂肪沉积不仅受到环境因素的影响,例如饲养方式、生长环境等,还与控制目标性状功能基因的表达和调控等遗传因素有着密切关系。此外,饲料营养水平的调节也可以影响猪的脂肪沉积。对于猪的脂肪沉积的研究不仅有利于提高猪肉质量和营养价值,还可以为猪的养殖提供理论依据和技术支持。有研究表明,脂肪代谢相关基因如ACACA和FASN等,它们表达量的差异对猪的脂肪沉积具有影响[2,3],包括影响猪肉中的饱和、不饱和脂肪酸含量。此外,研究表明,猪的品种、遗传背景和基因多态性等因素也会影响猪的脂肪沉积性状[4,5]。【前人研究进展】脂肪酸结合蛋白3(Fat acid binding proteins 3,FABP3),又称为心脏型脂肪酸结合蛋白[6],定位于猪第6号染色体区域,相对分子质量为15 kDa,主要参与脂肪酸的转运和利用等,FABP3是编码肌肉细胞内脂肪酸结合蛋白的基因,在畜禽的脂肪代谢中发挥着重要作用[7]。研究表明FABP3基因多态性与猪脂肪性状具有相关性,与猪肌内脂肪(Intramuscular fat,IMF)含量呈正相关[8,9]。有研究发现FABP3基因的表达水平与IMF含量同样显著相关[10]。LI等[11]通过分析猪体外成脂分化过程中FABP3基因的表达水平,发现该基因表达水平在分化过程中呈上调的趋势,表明FABP3可能在脂肪细胞功能中发挥重要作用。FABP3基因是影响猪肌内脂肪含量的候选基因[12]。研究表明,FABP3基因参与前脂肪细胞分化和脂肪沉积等过程,对提高棕色脂肪组织的耐寒性和脂肪酸氧化非常重要[13]。张敏[14]对FABP3在奶牛乳腺上皮细胞脂质合成中的研究表明,FABP3通过调节固醇调节元件结合蛋白1(SREBP1)、过氧化物酶体增殖物激活受体(PPARG)基因的mRNA及蛋白表达水平控制脂滴的形成;JIANG等[15]同样发现miR-3-4789p可通过抑制FABP3基因表达来抑制前脂肪细胞分化和脂滴沉积;CHMURZYNSKA等[16]、BLECHA等[17]、LI等[18]、WANG等[19]通过挖掘FABP3基因的多态性位点发现该基因与脂肪性状相关。【本研究切入点】藏猪是我国唯一的高原、高寒放牧猪种,具有耐粗饲、耐寒以及沉脂能力强等生物学特性[20,21]。这些特征使得藏猪的脂肪沉积方式可能与低海拔生态区域的猪不同,研究藏猪的脂肪沉积可以为高海拔地区的畜牧业发展提供科学依据。FABP3基因在脂肪沉积过程中发挥重要作用,对功能基因的深入了解对提高畜禽肉品质具有重要价值,目前关于FABP3基因的多态性和表达水平对藏猪肉品质的影响鲜有报道。【拟解决的关键问题】为加快对藏猪肉品质改良进程,本研究以饲养在西藏林芝(平均海拔2900 m)的藏猪和大约克猪为研究对象,采用一代测序技术对FABP3基因的5'侧翼区和CDS区进行测序和多态性分析,并利用RT-qPCR技术,比较FABP3基因在藏猪和大约克猪肝脏、背最长肌以及背脂中的表达情况,以期为猪FABP3基因调控脂肪代谢的分子机制奠定基础。
1. 材料与方法
1.1 试验材料
采集西藏农牧学院教学实习牧场180日龄的藏猪(n=28)和大约克猪(n=39)耳组织用于进行DNA提取。挑选无血缘关系的藏猪和大约克猪各10头同期饲养至180日龄进行屠宰,取其肝脏、背脂和背最长肌组织置于注有RNA保存液的样品管中,−80 ℃保存,用于RNA提取。
1.2 组织DNA、RNA提取及cDNA的制备
采用苯酚-氯仿抽提法提取DNA[22],使用Trizol法提取藏猪与大约克猪组织总RNA[23];用NanoDrop One超微量分光光度计检测所提DNA和RNA的纯度和浓度;1%琼脂糖凝胶电泳检测RNA的完整性。后采用FastKing cDNA第一链合成试剂盒(天根)制备cDNA,−20 ℃保存,用于后续荧光定量试验。
1.3 DNA引物设计与合成
登录NCBI(htttp://www.ncbi.nlm.nih.gov)网站下载猪FABP3基因(登录号:NC_010448.4)起始密码子上游3000 bp区域DNA序列与CDS区(登录号NM_001099931.1)序列,根据序列信息进行引物设计(Primer 5),并由上海生工生物工程有限公司进行引物合成,引物信息如表1所示。
表 1 FABP3基因5'侧翼区和CDS区引物序列Table 1. Primer sequence of 5' flanking region and CDS region in FABP3引物
Primer扩增区域
Amplified region引物序列(5′-3′)
Primer sequences退火温度
Annealing temperature/℃产物大小
Product length/bp5′−FABP3-1 356 bp至−460 bp F: TCAGCCCAAGAGTGAGTTTC
R: CCTTCTTCCTCGAAAGCG56 817 5′−FABP3-2 −430 bp至−1365 bp F: TCTGCTGGCTCAAGTTCAGT
R: GAGAGGAGAAAGGAAACTCACT58 953 5′−FABP3-3 −1342 bp至−2197 bp F: TAGGAGTCAACTTTGGTGAGC
R: CCAACTGAACTTGAGCCAGCA59 856 5′−FABP3-4 −2195 bp至−3033 bp F: CTGGGAACCTCCATATGTCG
R: CTAAGCCACAATCTATCACCT57 849 FABP3-CDS 34 bp至445 bp F:CCTGTTCTGTCGTCTCTTTCTCA
R:TGCCTCTTTCTCGTAAGTGCG60 440 1.4 荧光定量PCR引物设计与合成
在NCBI(htttp://www.ncbi.nlm.nih.gov/)下载猪FABP3基因(登录号NM_001099931.1)mRNA序列,选取GAPDH作为内参基因,利用软件Primer Premier 5.0设计引物(引物信息见表2),用于组织表达分析,并由上海生工生物工程有限公司进行合成。
表 2 FABP3基因定量PCR引物序列Table 2. Primer sequence of FABP3 for quantitative PCR基因名称
Gene name登录号
GeneBank number引物序列(5′-3′)
Primer sequences退火温度
Annealing temperature/℃产物大小
Product length/bpFABP3 NM_001099931.1 F: ATGACCAAGCCTACCACAA
R: AAGTTTGCCTCCATCCAGT57 171 GAPDH NM_001206359.1 F: CACCATCTTCCAGGAGCGAG
R: CCCTTCAAGTGAGCCCCG57 120 1.5 SNPs筛选与转录因子预测
对FABP3基因起始密码子上游3000 bp区域的DNA序列进行PCR扩增,经琼脂糖凝胶电泳检测后选取藏猪和大约克猪各10个合格的PCR产物进行混池测序,利用Chromas Pro软件对测序结果进行分析、筛选SNPs位点。针对筛选的SNPs进一步送扩大个体再次进行测序。综合两次测序结果计算各突变位点的基因型频率与基因频率。登录JASPAR(htttp://jaspar.binf.ku.dk/)转录因子预测网站进行突变位点转录因子预测。
1.6 荧光定量PCR
以cDNA为模板,选取藏猪与大约克猪各10个个体进行RT-qPCR,每个个体设置3个重复,反应体系为20 μL。并使用2−△△ct法计算FABP3基因在组织中的相对表达量。
1.7 统计分析
使用SPSS 26.0软件对FABP3基因mRNA相对表达量进行单因素方差分析,测定结果以P值(P value)表示;对FABP3基因的基因型频率和基因频率进行卡方检验。P <0.05为差异显著,P < 0.01为差异极显著。
2. 结果与分析
2.1 藏猪与大约克猪组织DNA检测
从琼脂糖凝胶电泳检测结果(图1)可以看出,所提DNA样品条带比较清晰完整,可以用于后续扩增试验。
2.2 FABP3基因SNPs筛选
对测序结果分析发现FABP3基因在5’侧翼区共有2个突变位点C-635A和T-114C(图2)。突变位点C-635A在藏猪中存在AA基因型,在大约克猪中存在CC、CA和AA基因型,等位基因A为优势基因。突变位点T-114C在藏猪中存在TC、CC基因型,在大约克猪中存在TT和TC基因型,等位基因C为优势基因(表3)。藏猪和大约克猪FABP3基因CDS区均未发现突变。
表 3 FABP3基因SNPs位点基因型频率及卡方检验Table 3. Genotype frequency and chi-square test of SNPs on FABP3位点
Loci品种
Species样本量
Sample size基因型频率(个体数/频率)
Genotype frequency (Individuals/Frequency)基因频率
Gene frequencyχ2值
CardinalityP值
P valueCC CA AA C A C-635A 大约克猪 39 16/0.410 16/0.410 7/0.179 0.615 0.385 0.693 0.707 藏猪 28 15/0.520 12/0.410 28/1.000 0.000 1.000 0.000 1.000 藏猪 vs 大约克猪 χ2=43.979;P<0.01 T-114C TT TC CC T C 大约克猪 39 33/0.846 6/0.154 0/0 0.923 0.077 0.271 0.873 藏猪 28 0/0.000 1/0.036 27/0.964 0.018 0.982 0.009 0.995 藏猪 vs 大约克猪 χ2=63.476;P<0.01 2.3 FABP3基因的基因频率与基因型频率
由表3可知,FABP3基因的突变位点在藏猪和大约克猪种内均符合哈迪-温伯格平衡定律(P>0.05)。藏猪和大约克猪在C-635A、T-114C位点呈极显著差异(P<0.01)。
2.4 转录因子预测
如表4所示,通过对转录因子预测发现SNPs位点碱基突变前后有部分转录因子结合位点消失和新转录因子产生。FABP3基因起始密码子上游3000 bp区域中存在2个SNPs位点(C-635A和T-114C),其中C-635A位点上C向A的突变导致ARNT2、SUMO2、 RB1、 CTCF、SMAD4、LF11、CHD1、SUZ12、YY1结合位点消失,并出现了新的转录因子STAT5B、TCF7L2、TCF12、SREBP1、MYH11、SPI1、TP53、TBX21、HOXA9;T-114C位点上T向C的突变导致E4F1结合位点消失,并出现了新的转录因子HES5、CLOCK、WT1、EP300、THAP11、KLF5。
表 4 FABP3基因SNPs位点转录因子预测结果Table 4. Predicted transcription factors in FABP3 SNPs突变位点
Mutation Loci突变前序列
Pre-mutation sequence突变后序列
Post-mutation sequence消失转录因子
Disappearance of transcription factors新增转录因子
Addition of transcription factorsC-635A TGGGGCGGGGG TGGGGAGGGGG ARNT2、 SUMO2、 RB1、 CTCF、SMAD4、LF11、CHD1、SUZ12、YY1 STAT5B、TCF7L2、TCF12、SREBP1、MYH11、SPI1、TP53、TBX21、HOXA9 T-114C ACGCCTCGTCA ACGCCCCGTCA E4F1 HES5、CLOCK、WT1、EP300、THAP11、KLF5 2.5 藏猪与大约克猪组织RNA电泳检测
从图3可以看出,RNA电泳图中28S、18S和5S条带清晰完整,表明本次提取的RNA完整无降解,满足后续反转录试验要求。
![]() 图 3 组织总RNA琼脂糖凝胶电泳M:Marker;1~3分别为藏猪肝脏、背脂、背最长肌组织;4~6分别为大约克猪肝脏、背脂、背最长肌组织。Figure 3. Agarose gel electrophoresis of total RNA in tissueM:Marker; 1–3: Liver, dorsal fat, and longest dorsal muscle tissues of Tibetan pig, respectively; 4–6: liver, dorsal fat, and longest dorsal muscle tissues of Yorkshire pig, respectively.
图 3 组织总RNA琼脂糖凝胶电泳M:Marker;1~3分别为藏猪肝脏、背脂、背最长肌组织;4~6分别为大约克猪肝脏、背脂、背最长肌组织。Figure 3. Agarose gel electrophoresis of total RNA in tissueM:Marker; 1–3: Liver, dorsal fat, and longest dorsal muscle tissues of Tibetan pig, respectively; 4–6: liver, dorsal fat, and longest dorsal muscle tissues of Yorkshire pig, respectively.2.6 FABP3基因在不同组织中的mRNA表达量
利用RT-qPCR技术分别对FABP3基因在藏猪和大约克猪两猪种肝脏、背脂和背最长肌3个组织中的表达水平进行检测(图4)。FABP3基因在藏猪的肝脏和背最长肌组织中的mRNA表达水平极显著高于大约克猪(P < 0.01),在背脂组织中的mRNA表达水平显著高于大约克猪(P < 0.05)。
![]() 图 4 FABP3基因在藏猪、大约克猪肝脏、背脂和背最长肌中的mRNA相对表达量TP为藏猪,YY为大约克猪;*为显著差异(P < 0.05),**为极显著差异(P < 0.01)。Figure 4. Relative expressions of FABP3 in liver, back fat, and longissimus dorsi muscle of TP and YYTP: Tibetan pig; YY: Yorkshire pig; *: significant difference at P<0.05;**: extremely significant difference at P<0.01.
图 4 FABP3基因在藏猪、大约克猪肝脏、背脂和背最长肌中的mRNA相对表达量TP为藏猪,YY为大约克猪;*为显著差异(P < 0.05),**为极显著差异(P < 0.01)。Figure 4. Relative expressions of FABP3 in liver, back fat, and longissimus dorsi muscle of TP and YYTP: Tibetan pig; YY: Yorkshire pig; *: significant difference at P<0.05;**: extremely significant difference at P<0.01.3. 讨论与结论
本研究在FABP3基因起始密码子上游3 kb区域发现2个SNPs位点(C-635A和T-114C),在藏猪和大约克猪中,这两个SNP位点的等位基因频率和基因型频率差异极显著(P < 0.01)。后续对2个位点突变前后转录因子进行预测,发现在C-635A位点,当C突变为A后,转录因子CTCF消失,CTCF(CCCTC位点结合蛋白)在调控动物生长发育过程中发挥重要作用[24,25]。肖成等[26]在对小寒尾羊的研究中发现S100钙结合蛋白A1(S100 Calcium Binding Protein A1,S100A1)的表达量随着脂肪组织中新细胞的增大而出现显著升高,而CTCF可以抑制S100A1的活性[27]。因此,推测CTCF对脂肪的生成可能起到负调控的作用。当C突变为A后,在该位点结合产生新的转录因子——胆固醇调节元件结合蛋白1(SREBP1)。SREBP1是脂肪合成酶的主要调节剂[28],是控制脂肪合成的关键转录因子,降低SPRBP1的表达可以降低脂肪沉积[29,30]。在T-114C位点,当T突变为C,转录因子ZnF蛋白E4F转录因子1(E4F1)消失。E4F1是早期胚胎发育过程中必需的多功能蛋白,在不同细胞类型增殖中发挥重要作用[31],包括干细胞。该转录因子可以与PARP-1基因共同作用来减少前体脂肪细胞的形成[32]。当T突变为C后,在该位点结合产生新的转录因子KLF5。CERVANTE等[33]在对山羊前体脂肪细胞的诱导试验中发现,KLF5在前体脂肪细胞的诱导分化中发挥着正向调控作用。KLF5(锌指蛋白转录因子5)可能调控脂肪细胞的生长和分化[34,35]。综上所述,该位点突变前后转录因子的变化可能对猪脂肪沉积产生影响 。
SCHAAP等[36]对小鼠的研究发现,敲除FABP3会降低小鼠对脂肪酸的吸收,使得小鼠体内脂肪量减少。YI 等[37]研究发现FABP3的过表达可以促进莱芜猪前脂肪细胞增殖;CHO K H等[38]通过对FABP3基因与大约克猪肌内脂肪含量的相关性研究发现,该基因与猪肌内脂肪含量呈正相关。本试验采用RT-qPCR技术分别对藏猪和大约克猪的背脂、肝脏和背最长肌3个组织中FABP3基因的表达水平进行检测,发现在肝脏和背最长肌组织上藏猪FABP3基因的mRNA相对表达量均极显著高于大约克猪;在背脂组织中,藏猪FABP3基因的mRNA相对表达量显著高于大约克猪。FABP3基因在藏猪中呈现高表达的趋势,而藏猪是典型的脂肪沉积型猪种,肌内脂肪含量较高,推测FABP3基因的高表达是藏猪脂肪能力强以及肌内脂肪含量高的原因之一,同时推测FABP3基因对猪的脂肪沉积有一定正向调控作用。
综上,藏猪FABP3基因5'侧翼区存在的2个突变位点C-635A和T-114C可能是参与脂肪生成和沉积的重要调控位点,FABP3基因的高表达可能正向调控藏猪脂肪沉积并对其肉品质产生重要影响。研究结果为后续阐明FABP3基因在猪脂肪沉积过程中的分子作用机制与分子标记辅助育种提供新思路和理论依据。
-
表 1 试验因素水平及编码
Table 1 Experimental factors and codes
因素 编码符号 编码水平 -1 0 1 葡萄糖/% A 1.5 2 2.5 蛋白胨/% B 0.1 0.3 0.5 KH2PO4/% C 0.1 0.3 0.5 果蔬汁/% D 5 10 15 表 2 响应面中心组合设计试验及结果
Table 2 Response surface central composite design and results
组别 因素 胞外多糖/(mg·mL-1) A B C D 1 0 -1 0 -1 0.53 2 0 1 1 0 0.42 3 -1 0 -1 0 0.15 4 1 -1 0 0 0.42 5 1 0 1 0 0.3 6 0 -1 -1 0 0.1 7 1 0 0 -1 0.53 8 0 0 0 0 0.57 9 -1 0 1 0 0.57 10 0 1 0 -1 0.54 11 0 0 -1 1 0.52 12 0 0 0 0 0.51 13 -1 1 0 0 0.48 14 1 0 -1 0 0.53 15 0 0 1 -1 0.49 16 -1 0 0 1 0.46 17 -1 0 0 -1 0.48 18 1 1 0 0 0.39 19 0 0 0 0 0.48 20 0 0 0 0 0.5 21 0 1 -1 0 0.58 22 -1 -1 0 0 0.21 23 0 0 1 1 0.61 24 0 1 0 1 0.74 25 0 0 -1 -1 0.41 26 1 0 0 1 0.62 27 0 -1 1 0 0.53 28 0 0 0 0 0.45 29 0 -1 0 1 0.52 表 3 胞外多糖方差分析结果
Table 3 Variance analysis on EPS content
方差来源 平方和 自由度 均方和 F P 模型 0.50 14 0.04 19.70 < 0.0001 A-葡萄糖 0.02 1 0.02 8.89 0.0099 B-蛋白胨 0.06 1 0.06 32.39 < 0.0001 C-磷酸二氢钾 0.03 1 0.03 18.22 0.0008 D-果蔬汁 0.02 1 0.02 11.02 0.0051 AB 0.02 1 0.02 12.39 0.0034 AC 0.11 1 0.11 58.18 < 0.0001 AD 0.0030 1 0.0030 1.67 0.2177 BC 0.09 1 0.09 47.93 < 0.0001 BD 0.01 1 0.01 6.07 0.0273 CD 0.00 1 0.00 0.014 0.9083 A2 0.03 1 0.03 18.44 0.0007 B2 0.007 1 0.007 3.62 0.0777 C2 0.03 1 0.03 14.23 0.0021 D2 0.05 1 0.05 30.17 < 0.0001 残差 0.03 14 0.002 失拟项 0.02 10 0.02 0.82 0.6360 纯误差 0.008 4 0.002 总离差 0.53 28 确定系数R-Squared 0.9517 调整系数Adj R-Squared 0.9034 -
[1] 魏金康.智慧之菇金针菇[J].北京农业, 2015, 35(10):37. http://d.wanfangdata.com.cn/Periodical/beijny201510018 [2] YAHAYA N F M, RAHMAN M A, ABDULLAH N. Therapeutic potential of mushrooms in preventing and ameliorating hypertension[J]. Trends in Food Science & Technology, 2014, 39(2):104-115. http://repository.um.edu.my/94771/
[3] LIN L, CUI F, ZHANG J, et al. Antioxidative and renoprotective effects of residue polysaccharides from Flammulina velutipes[J]. Carbohydrate Polymers, 2016, 146:388. DOI: 10.1016/j.carbpol.2016.03.071
[4] 柴新义, 向玉勇, 万美娟, 等.金针菇液体发酵培养工艺的优化研究[J].文山学院学报, 2012, 25(3):12-15. http://d.wanfangdata.com.cn/Periodical/wssfgdzkxxxb201203005 [5] 蒋冬花, 张萍华.深层培养诸因素对金针菇菌丝体生长的影响[J].食用菌学报, 1997, 4(3):40-44. http://www.cqvip.com/QK/98175X/199703/2676989.html [6] 姜宁, 刘晓鹏, 杨洪, 等.金针菇液体培养基优化研究[J].安徽农业科学, 2007, 35(21):6429-6430. DOI: 10.3969/j.issn.0517-6611.2007.21.045 [7] FIDLER G, RODINO S, BUTU A, et al. Optimization of submerged culture conditions for Flammulina velutipes on SBD culture medium[J]. Journal of Biotechnology, 2015, 208:S103.
[8] 李春红.金针菇高产栽培技术[J].河南农业, 2014, 25(1):47. http://d.wanfangdata.com.cn/Periodical/nykjtx201009092 [9] ZHANG Z, LV G, HE W, et al. Effects of extraction methods on the antioxidant activities of polysaccharides obtained from Flammulina velutipes[J]. Carbohydrate polymers, 2013, 98(2):1524-1531. DOI: 10.1016/j.carbpol.2013.07.052
[10] KHURI A I, MUKHOPADHYAY S. Response surface methodology[J]. Wiley Interdisciplinary Reviews:Computational Statistics, 2010, 2(2):128-149. DOI: 10.1002/wics.v2:2
[11] 何轩辉, 廖森泰, 刘吉平, 等.应用Box-Behnken组合设计优化金针菇粗多糖提取条件[J].食用菌学报, 2008, 15(3):64-67. http://d.wanfangdata.com.cn/Periodical/syjxb200803012 [12] CHEHREGHANI S, NOAPARAST M, REZAI B, et al. Bonded-particle model calibration using response surface methodology[J]. Particuology, 2017, 32:141-152. DOI: 10.1016/j.partic.2016.07.012
[13] 傅明辉, 洪梅达.金针菇子实体多糖的抗氧化活性的研究[J].食品研究与开发, 2011, 32(12):20-22. DOI: 10.3969/j.issn.1005-6521.2011.12.006 [14] 张丽霞, 赵丽娟.金针菇多糖的抗氧化活性研究[J].西南农业学报, 2014, 27(1):240-243. http://d.wanfangdata.com.cn/Periodical/xnnyxb201401046 [15] HUA D, ZHANG D, HUANG B, et al. Structural characterization and DPPH路radical scavenging activity of a polysaccharide from Guara fruits[J]. Carbohydrate polymers, 2014, 103:143-147. DOI: 10.1016/j.carbpol.2013.12.009
[16] SHI M, ZHANG Z, YANG Y. Antioxidant and immunoregulatory activity of Ganoderma lucidum polysaccharide (GLP)[J]. Carbohydrate polymers, 2013, 95(1):200-206. DOI: 10.1016/j.carbpol.2013.02.081
[17] ZHAO J Q, WANG Y M, YANG Y L, et al. Isolation and identification of antioxidant and α-glucosidase inhibitory compounds from fruit juice of Nitraria tangutorum[J]. Food Chemistry, 2017, 227(1):93. http://www.sciencedirect.com/science/article/pii/S0308814617300328
[18] 赵光远, 陈美丽, 许艳华, 等.超高压微射流对石榴汁微生物及抗氧化活性的研究[J].食品科技, 2017, 43(2):89-93. [19] GAO T, MA S, SONG J, et al. Antioxidant and immunological activities of water-soluble polysaccharides from Aconitum kusnezoffii Reichb[J]. International Journal of Biological Macromolecules, 2011, 49(4):580. DOI: 10.1016/j.ijbiomac.2011.06.017




 下载:
下载: