Biological Characteristics of Colletotrichum gloeosporioides and Fungicides for Disease Control on Honey Pomelo in Fujian
-
摘要:目的 明确蜜柚炭疽病病原菌(Colletotrichum gloeosporioides)的生物学特性,筛选高效安全杀菌剂,以期指导蜜柚种植生产。方法 采用十字交叉法和血球计数法分别测定温度、pH和光照对菌丝生长及产孢量的影响,以及菌丝的致死温度;利用菌丝生长速率法,测定4种杀菌剂对蜜柚炭疽病菌的室内毒力。结果 蜜柚炭疽病菌的菌丝生长最适温度为25 ℃,产孢最适温度为30 ℃、菌丝生长和产孢最适pH值均为7、光照条件对菌丝生长影响有限,但光照有利于产孢,菌丝生长致死温度为51 ℃,10 min。室内毒力测定结果表明,4种杀菌剂对蜜柚炭疽病菌菌丝生长均具有不同程度的抑制作用,其中咪鲜胺抑菌效果最好,EC50为0.017 1 mg·L−1,其次为苯醚甲环唑和吡唑醚菌酯,EC50分别为0.023 7和0.034 5 mg·L−1,而多菌灵相比之下效果偏差,为0.258 6 mg·L−1。结论 温度和pH能影响蜜柚炭疽病菌生长及产孢,但光照条件对菌丝生长影响有限。咪鲜胺对蜜柚炭疽病病原菌具有较好的室内毒力。Abstract:Objective Biological characteristics of the pathogen, Colletotrichum gloeosporioides, that infects the honey pomelos in Fujian were studied, and effective antifungal agents evaluated.Method Effects of temperature, light, and pH on the mycelial growth, lethality, and sporulation of C. gloeosporioides were determined by crisscrossing and cell count methods. An in vitro toxicity test based on the mycelial growth rate was conducted to examine the efficacy of 4 fungicides against the anthracnose.Result The optimum conditions for the pathogenic development included 25 ℃ for mycelial growth and 30 ℃ for sporulation at pH 7 and light exposure for sporulation. The mycelia died at 51 ℃ in 10 m. The indoor virulence test on the fungicides showed prochloraz with the lowest EC50 at 0.0171 mg·L−1, followed by difenoconazole at 0.0237 mg·L−1, pyraclostrobin at 0.0345 mg·L−1, and carbendazim at 0.2586 mg·L−1.Conclusion Temperature and pH exerted significant effects on the growth and sporulation of C. gloeosporioides. Limited effect was observed the mycelial growth by light exposure. Among the tested fungicides, prochloraz exhibited the greatest potential for controlling C. gloeosporioides.
-
0. 引 言
【研究意义】琯溪蜜柚(Guanxi honey pomelo)又名香抛,是芸香科(Rutaceae)柑橘属(Citrus Linn)多年生木本植物,原产于福建省漳州市平和县,是我国柚类主栽良种之一,在福建省平和县种植面积达4.3万hm2 [1]。近年来,随着蜜柚单一的种植模式及品种抗病性减弱,使蜜柚炭疽病的发生逐年加重,严重影响了蜜柚的品质和产量,据统计2016年平和县蜜柚炭疽病发生面积达2.1万 hm2,对当地蜜柚产业造成极大经济损失,因此蜜柚炭疽病的有效防治已迫在眉睫[2]。【前人研究进展】本课题组曾对琯溪蜜柚炭疽病进行分离鉴定,其病原菌鉴定为胶孢炭疽菌(Colletotrichum gloeosporioides),该菌是一种世界性的植物病原菌,在适宜的环境下扩散迅速,在琯溪蜜柚的整个生长期和采后果实保鲜期均可为害[3]。目前,国内对蜜柚炭疽病的研究主要集中在炭疽病症状的识别与诊断、发生规律和简单防治措施等方面[4]。【本研究切入点】由胶孢炭疽菌引起的蜜柚炭疽病是蜜柚上的重要病害之一,但关于蜜柚炭疽病菌的生物学特性及高效安全杀菌剂筛选有待深入研究。【拟解决的关键问题】通过菌丝生长和产孢量探明蜜柚炭疽病菌胶孢炭疽菌的生物学特性,同时测定常用化学杀菌剂对该病原菌的室内毒力,以明确该菌的生长条件及安全高效杀菌剂,为蜜柚炭疽病提供有效防治措施及技术支持。
1. 材料与方法
1.1 供试材料
供试药剂:96.5%咪鲜胺原药(Prochloraz,咪唑类,辉丰农化股份有限公司)、95% 苯醚甲环唑(Difenoconazole,三唑类,山东东泰农化有限公司)、96%吡唑醚菌酯原药(Pyraclostrobin,甲氧基丙烯酸酣类,江苏耘农化工有限公司)、98.1%多菌灵原药(Carbendazim,苯并咪唑类,辉丰农化股份有限公司)。
供试菌株:蜜柚炭疽病菌(C. gloeosporioides),由漳州市农业科学研究所分离、鉴定及保藏。
供试培养基:①马铃薯葡萄糖琼脂(PDA)培养基:新鲜去皮马铃薯200 g、葡萄糖20 g、琼脂粉16 g、去离子水1000 mL;②察氏(Czapek)培养基:硝酸钠3 g、磷酸氢二钾1 g、硫酸镁0.5 g、氯化钾0.5 g、硫酸亚铁0.01 g、蔗糖30 g、琼脂粉16 g、蒸馏水1000 mL。
1.2 病原菌生物学特性
1.2.1 温度对病原菌菌丝生长及产孢量的影响
参考刘行风等的方法[5-6],取直径5 mm的病原菌菌饼接种于PDA平板(d=9.0 cm,下同)中央,分别置于10、15、20、25、30、35和40 ℃恒温培养箱中培养,6 d后采用十字交叉法测量菌落直径,每处理3个重复;后用 10 mL 无菌水洗下菌落表面孢子,制成孢子悬浮液,用纽鲍尔(Neubauer)血球计数板测定孢子含量,每处理3次重复。
1.2.2 光照对病原菌菌丝生长及产孢量的影响
取直径5 mm的病原菌菌饼接种于PDA平板中央,依次置于全黑暗、全光照和12 h光照/12 h黑暗的25 ℃培养箱内培养,6 d后测定菌落直径和产孢量,测定方法同1.2.1,每处理3次重复。
1.2.3 pH值对病原菌菌丝生长及产孢量的影响
取直径为5 mm的菌饼接种于用0.1 mol·L−1 HCl和0.1 mol·L−1 NaOH调配pH为4、5、6、7、8、9、10、11的PDA平板中央,在25 ℃培养箱中培养,6 d后测定菌落直径和产孢量,测定方法同1.2.1,每处理3次重复。
1.2.4 菌丝致死温度的测定
取直径为5 mm的菌饼置于装有5 mL 无菌水的5 mL冻存管中,分别置于45~55 ℃的恒温水浴锅中,10 min后将菌饼转接至PDA平板中央,在25 ℃培养箱中培养,每处理3次重复,6 d后观察有无菌丝生长,最终确定菌丝的致死温度。
1.3 4种供试药剂对蜜柚炭疽病菌的室内毒力
采用菌丝生长速率法测定4种杀菌剂对蜜柚炭疽病菌的室内毒力[7]。无菌条件下,在PDA培养基中加入咪鲜胺、苯醚甲环唑、吡唑醚菌酯和多菌灵母液,将其配置成0.002、0.01、0.05、0.25、1.25 和6.25 mg·L−1的含药培养基。取直径5 mm的病原菌菌饼接种于上述含药PDA平板中央,每处理3皿,重复3次,后置于25 ℃恒温培养,6 d后采用十字交叉法测量每个培养基的菌落直径,计算抑制率,菌丝生长抑制率/%=[(对照组菌落直径−药剂处理组菌落直径)/(对照组菌落直径−菌饼直径)]×100。
1.4 数据统计与分析
在DPS 7.05数据处理软件上,计算4种杀菌剂对供试菌株的有效抑制中浓度EC50,并利用Duncan’s新复极差法对生物学特性,如温度、光照和pH等结果进行单因素方差分析。
2. 结果与分析
2.1 病原菌生物学特性
2.1.1 温度对病原菌菌丝生长及产孢量的影响
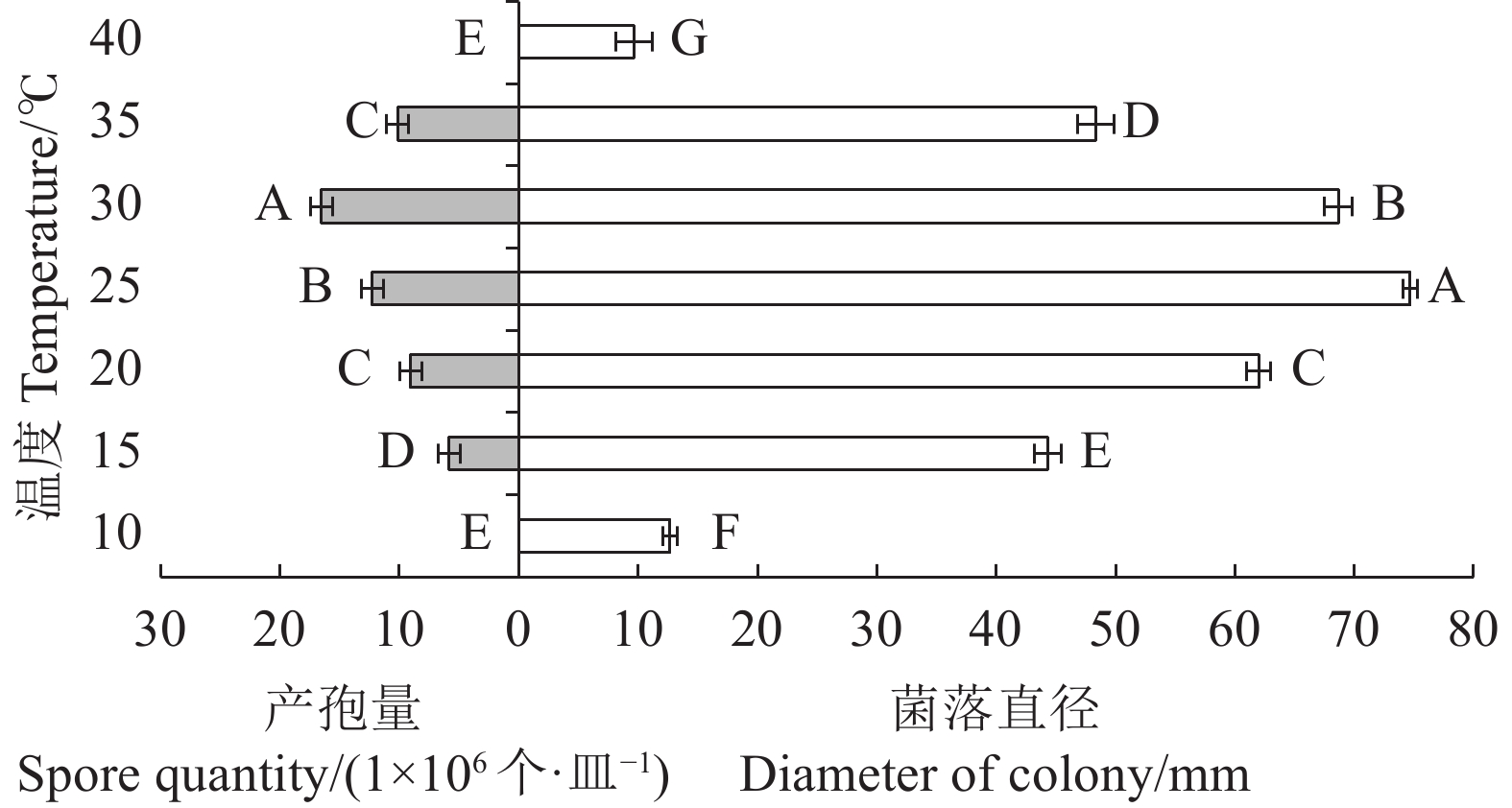
从图1可看出,在10~25 ℃时,菌落直径随温度的升高而增加,25 ℃时菌落直径最大,为74.66 mm,在30~40 ℃时,菌落直径随温度的升高而减少。在15~30 ℃时,病原菌产孢量随温度的升高而增加,30 ℃时产孢量最大,为16.53×105个·皿−1,温度升至35 ℃时,产孢量下降,在10 ℃和40 ℃时,病原菌无法产孢。结果表明,蜜柚炭疽病菌菌落生长最适温度为25 ℃,产孢最适温度为30 ℃。
2.1.2 pH值对病原菌菌丝生长及产孢量的影响
由图2可看出,蜜柚炭疽病菌在pH为4~10时均能产孢和生长,在pH为4~7时,菌落直径和产孢量随温度的升高而增加,在pH为7时菌落直径和产孢量最大,分别为70.67 mm和13.33×105个·皿−1 ,且差异极显著。在pH为8~10时,菌落直径和产孢量随温度的升高而减少。结果表明,蜜柚炭疽病菌菌落生长和产孢的最适pH均为7。
2.1.3 光照条件对病原菌菌丝生长及产孢量的影响
由图3可看出,在全黑暗、半光照和全光照 3种条件下,蜜柚炭疽病菌菌丝能正常生长,均能产孢。3个光照条件下菌丝均生长旺盛,3个处理间差异不显著。但不同光照条件下的产孢量不同,全光照条件下产孢量最高,为11.73×105个·皿−1,显著高于其他2个处理。结果表明,不同光照条件对蜜柚炭疽病菌菌丝生长影响不大,但光照有利于产孢。
2.1.4 病原菌菌丝致死温度
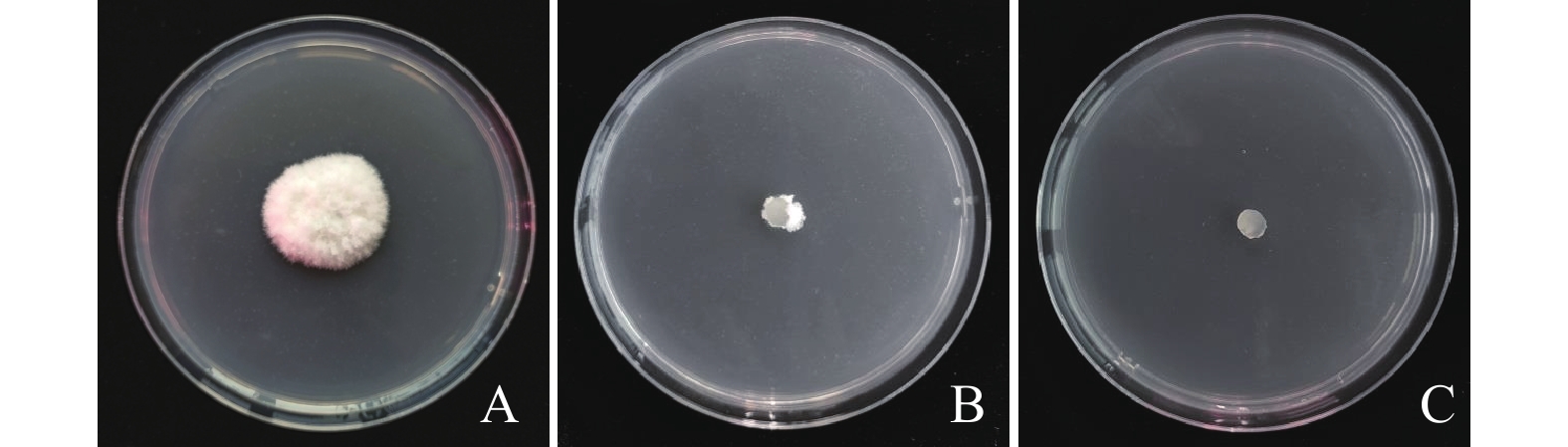
蜜柚炭疽病菌菌落在45~55 ℃水浴处理10 min,再于28 ℃培养箱培养6 d后进行观察,结果表明经45~50 ℃水浴处理10 min的菌碟均能生长并形成新菌落,而51 ℃水浴处理10 min的菌碟不能生长并形成新菌落(图4),表明蜜柚炭疽病菌菌丝生长的致死温度为51 ℃、10 min。
2.2 蜜柚炭疽病防治药剂筛选
室内毒力测定结果(表1)表明,供试的4种杀菌剂对蜜柚炭疽病菌菌丝生长均具有不同程度的抑制作用,其中咪鲜胺的抑菌效果最好,EC50为0.0171 mg·L−1;其次为苯醚甲环唑和吡唑醚菌酯,EC50分别为0.0237 mg·L−1和0.0345 mg·L−1;多菌灵的抑菌效果最低,EC50为0.2586 mg·L−1。结果表明,相较于多菌灵,咪鲜胺、苯醚甲环唑和吡唑醚菌酯可能更适用于蜜柚炭疽病的防治。而多菌灵对蜜柚炭疽病菌抑制效果较弱的原因,可能与多菌灵的长期施用,病原菌抗药性的产生等原因有关。
表 1 4种供试药剂对蜜柚炭疽病的毒力Table 1. Toxicities of 4 fungicides against C. gloeosporioides供试药剂
Fungicides毒力回归方程
Toxicity regression equationEC50/(mg·L−1) 95% 置信区间
95% Confidence interval/(mg·L−1)相关系数r
Correlation coefficient r咪鲜胺
Prochlorazy=5.8060+0.4563x 0.0171 0.0127~0.0232 0.9957 苯醚甲环唑
Difenoconazoley=5.5791+0.4206x 0.0237 0.0173~0.0324 0.9949 吡唑醚菌酯
Pyraclostrobiny=5.6197+0.4238x 0.0345 0.0228~0.0521 0.9902 多菌灵
Carbendazimy=5.2430+0.4136x 0.2586 0.1705~0.3921 0.9892 3. 讨论与结论
炭疽病是琯溪蜜柚生产中的重要病害之一,主要为害蜜柚果实、叶片、花和枝梢等部位。笔者从福建漳州琯溪蜜柚炭疽病病株中分离到的病原菌为胶孢炭疽菌C. gloeosporioides[1],胶孢炭疽菌最早于1882年在意大利的柑橘上被发现[8],此外还在柑橘上发现尖孢炭疽菌C. acutatum和平头炭疽菌C. truncatum[9-10],说明炭疽病的致病菌具有多样性。但是福建地区蜜柚炭疽病是否还存在其他病原菌,仍需进一步扩大采集病样进行分离、鉴定。该病原菌的生物学特性研究结果表明,其菌丝生长和产孢量均受温度、pH值和光照等条件的影响,产孢最适温度为30 ℃,与胡永亮等[11]报道的铁皮石斛炭疽病菌产孢最适温度一致;菌落生长最适温度为25 ℃,与李戌清等[12]报道的三叶青炭疽病原菌的最适菌丝生长温度一致;产孢和菌落生长的最适pH均为7,其中菌丝生长最适pH与杨子祥等[13]的报道一致,但产孢量最适pH高于报道中的pH值4,存在显著差异,这可能与寄主差异有关;光照条件对蜜柚炭疽病菌菌丝生长影响不大,与程勋东等[14]报道的结果一致,但光照利于产孢,黑暗抑制产孢。菌丝生长致死温度为51 ℃,10 min。
化学防治是防治作物病害的主要手段,因此,防治药剂的筛选十分关键,科学精准用药不仅可以提高杀菌剂的防治效果,还可以减少用药量和用药次数,延缓病原菌的抗药性[15]。目前,对药剂防控蜜柚炭疽病的研究较少。本研究测定了4种不同化学结构和作用机制的杀菌剂对琯溪蜜柚炭疽病菌的室内毒力,测定结果表明供试的4种杀菌剂对蜜柚炭疽病病原菌均具有不同程度的抑制作用,其中咪鲜胺的抑菌效果最好,EC50为0.0171 mg·L−1;其次为苯醚甲环唑和吡唑醚菌酯,EC50分别为0.0237 mg·L−1和0.0345 mg·L−1;多菌灵的抑菌效果最低,EC50为0.2586 mg·L−1。本试验测得的EC50均低于郑金龙等[16]报道中柱花草胶孢炭疽病菌的EC50,这可能是因为寄主的差异性导致的。试验结果说明,咪鲜胺、苯醚甲环唑和吡唑醚菌酯更适用于蜜柚炭疽病的防治,多菌灵对蜜柚炭疽病病原菌抑制效果较差,可能是由于多菌灵是常见的广谱杀菌剂,在长期的使用过程中,蜜柚炭疽病菌对其产生了一定的抗药性。本研究采用菌丝生长速率法测定4种杀菌剂对蜜柚炭疽病菌的室内毒力,但室内环境与田间存在一定差异,后续将对药剂的田间应用、药剂残留和对非靶标生物的影响等方面开展研究,为蜜柚炭疽病的防治药剂的选择提供参考,同时为合理地使用化学药剂、延缓抗药性的发展提供理论依据。
-
表 1 4种供试药剂对蜜柚炭疽病的毒力
Table 1 Toxicities of 4 fungicides against C. gloeosporioides
供试药剂
Fungicides毒力回归方程
Toxicity regression equationEC50/(mg·L−1) 95% 置信区间
95% Confidence interval/(mg·L−1)相关系数r
Correlation coefficient r咪鲜胺
Prochlorazy=5.8060+0.4563x 0.0171 0.0127~0.0232 0.9957 苯醚甲环唑
Difenoconazoley=5.5791+0.4206x 0.0237 0.0173~0.0324 0.9949 吡唑醚菌酯
Pyraclostrobiny=5.6197+0.4238x 0.0345 0.0228~0.0521 0.9902 多菌灵
Carbendazimy=5.2430+0.4136x 0.2586 0.1705~0.3921 0.9892 -
[1] 赖宝春, 吴顺章, 郑春明, 等. 琯溪蜜柚炭疽病病原鉴定 [J]. 果树学报, 2017, 34(9):1178−1184. LAI B C, WU S Z, ZHENG C M, et al. Identification of pathogen causing Guanxi honey pomelo anthracnose in Pinghe County of Fujian Province [J]. Journal of Fruit Science, 2017, 34(9): 1178−1184.(in Chinese)
[2] 曾保忠. 琯溪蜜柚主要病害的发生规律与防治措施 [J]. 福建热作科技, 2017, 42(3):46−50. DOI: 10.3969/j.issn.1006-2327.2017.03.011 ZENG B Z. Occurrence regularity and control measures of main diseases of Guanxi honey pomelo [J]. Fujian Science & Technology of Tropical Crops, 2017, 42(3): 46−50.(in Chinese) DOI: 10.3969/j.issn.1006-2327.2017.03.011
[3] 赖宝春, 吴振强, 戴瑞卿, 等. 琯溪蜜柚炭疽病拮抗放线菌的筛选和鉴定 [J]. 热带作物学报, 2020, 41(9):1876−1882. DOI: 10.3969/j.issn.1000-2561.2020.09.022 LAI B C, WU Z Q, DAI R Q, et al. Screening and identification of antagonistic actinomycete against anthracnose disease of guanxi honey pomelo cultivar [J]. Chinese Journal of Tropical Crops, 2020, 41(9): 1876−1882.(in Chinese) DOI: 10.3969/j.issn.1000-2561.2020.09.022
[4] 张顺金. 蜜柚病虫害的发生特点及防治技术 [J]. 现代农业科技, 2019(20):112,115. ZHANG S J. Occurrence chracteristics and control technique of pests and diseases of honey pomelo [J]. Modern Agricultural Science and Technology, 2019(20): 112,115.(in Chinese)
[5] 刘行风, 刘东, 陶磊, 等. 黑龙江省黄瓜链格孢叶斑病病原鉴定及生物学特性研究 [J]. 中国蔬菜, 2021(8):80−86. LIU X F, LIU D, TAO L, et al. Pathogen identification and biological characteristics of cucumber Alternaria leaf spot in Heilongjiang Province [J]. China Vegetables, 2021(8): 80−86.(in Chinese)
[6] 黎肇家, 李汶晋, 毛跃彦, 等. 栾树枝枯病病原菌鉴定及其生物学特性研究 [J]. 西北农林科技大学学报(自然科学版), 2020, 48(9):53−63. LI Z J, LI W J, MAO Y Y, et al. Identification and biological characteristics of branch withered disease causing pathogen to Koelreuteria paniculata Laxm [J]. Journal of Northwest A & F University (Natural Science Edition), 2020, 48(9): 53−63.(in Chinese)
[7] 中华人民共和国农业部. 农药室内生物测定试验准则 杀菌剂 第2部分: 抑制病原真菌菌丝生长试验 平皿法: NY/T 1156.2—2006[S]. 北京: 中国标准出版社, 2006. [8] WEIR B S, JOHNSTON P R, DAMM U. The Colletotrichum gloeosporioides species complex [J]. Studies in Mycology, 2012, 73(1): 115−180.
[9] MARQUES J P R, AMORIM L, SPÓSITO M B, et al. Infection of Citrus pollen grains by Colletotrichum acutatum [J]. European Journal of Plant Pathology, 2013, 136(1): 35−40. DOI: 10.1007/s10658-012-0078-2
[10] BAHRI B A, SAADANI M, MECHICHI G, et al. Genetic diversity of Colletotrichum gloeosporioides species complex associated with Citrus withertip of twigs in Tunisia using microsatellite markers [J]. Journal of Phytopathology, 2019, 167(6): 351−362. DOI: 10.1111/jph.12806
[11] 胡永亮, 白学慧, 陈玉芹, 等. 铁皮石斛炭疽病病原鉴定及其生物学特性研究 [J]. 中国森林病虫, 2019, 38(2):11−16,21. HU Y L, BAI X H, CHEN Y Q, et al. Identification and biological characteristics of Colletotrichum gloeosporioides on Dendrobium officinale [J]. Forest Pest and Disease, 2019, 38(2): 11−16,21.(in Chinese)
[12] 李戌清, 严建立, 阮松林. 三叶青炭疽病病原菌的鉴定与生物学特性 [J]. 浙江农业学报, 2020, 32(11):2009−2019. DOI: 10.3969/j.issn.1004-1524.2020.11.11 LI X Q, YAN J L, RUAN S L. Identification and biological characteristics of anthracnose pathogen on Tetrastigma hemsleyanum [J]. Acta Agriculturae Zhejiangensis, 2020, 32(11): 2009−2019.(in Chinese) DOI: 10.3969/j.issn.1004-1524.2020.11.11
[13] 杨子祥, 苏银玲, 白明第, 等. 干热河谷地区芒果炭疽病菌生物学特性 [J]. 热带农业科学, 2019, 39(4):62−66. YANG Z X, SU Y L, BAI M D, et al. Biological characteristics of Colletotrichum gloeosporioides causing mango anthracnose in the dry hot valley area of Yunnan Province [J]. Chinese Journal of Tropical Agriculture, 2019, 39(4): 62−66.(in Chinese)
[14] 程勋东, 隋益虎. 辣椒炭疽病原菌生物学特性研究 [J]. 安徽科技学院学报, 2015, 29(1):34−38. DOI: 10.3969/j.issn.1673-8772.2015.01.008 CHENG X D, SUI Y H. Biological characteristics of anthracnose pathogen in chilli pepper [J]. Journal of Anhui Science and Technology University, 2015, 29(1): 34−38.(in Chinese) DOI: 10.3969/j.issn.1673-8772.2015.01.008
[15] 张怡, 沈迎春. 防治火龙果炭疽病安全用药技术初探 [J]. 农药科学与管理, 2020, 41(7):47−54. ZHANG Y, SHEN Y C. APreliminary study on the safe application technology for the prevention and treatment of pitaya Gloeosporium sp [J]. Pesticide Science and Administration, 2020, 41(7): 47−54.(in Chinese)
[16] 郑金龙, 李秋洁, 易克贤, 等. 9种杀菌剂对柱花草胶孢炭疽病菌的室内毒力测定 [J]. 热带农业科学, 2015, 35(2):66−69. DOI: 10.3969/j.issn.1009-2196.2015.02.013 ZHENG J L, LI Q J, YI K X, et al. Toxicity test of nine kinds of fungicides for collectotrichum gloeosporioides on Stylosanthes anthracnose in laboratory [J]. Chinese Journal of Tropical Agriculture, 2015, 35(2): 66−69.(in Chinese) DOI: 10.3969/j.issn.1009-2196.2015.02.013
-
期刊类型引用(0)
其他类型引用(2)




 下载:
下载: